题目内容
 某品牌化肥尿素包装袋上部分信息见如图,请根据相关信息计算回答:
某品牌化肥尿素包装袋上部分信息见如图,请根据相关信息计算回答:(1)尿素(化学式CO(NH2)2的化学式量为
(2)一个尿素分子中所含原子数为
(3)尿素中碳元素:氧元素:氮元素:氢元素的质量比为
(4)尿素中氮元素的质量分数是多少?
(写出计算过程,计算结果精确到0.1%)
(5)判断该化肥属于
(6)某农田计划施用上述品牌的尿素(化学式CO(NH2)2)100kg,但由于货源短缺,现改用硝酸铵(化学式NH4NO3),为保证含氮量相当,所需硝酸铵的质量是多少kg?写出计算过程.(注明:该小问属于附加题,可选做.)
考点:相对分子质量的概念及其计算,纯净物和混合物的判别,元素质量比的计算,元素的质量分数计算,化合物中某元素的质量计算
专题:化学式的计算
分析:(1)根据尿素的化学式可知,它的相对分子质量=(碳的相对原子质量×碳原子个数)+(氧的相对原子质量×氧原子个数)+(氮的相对原子质量×氮原子个数)+(氢的相对原子质量×氢原子个数);
(2)根据尿素(化学式CO(NH2)2,求一个尿素分子中所含原子数;
(3)根据尿素(化学式CO(NH2)2,求尿素中碳元素:氧元素:氮元素:氢元素的质量比;
(4)尿素中氮元素的质量分数=
×100%;
(5)根据“60克×尿素中氮元素的质量分数”计算即可;CO(NH2)2
(6)先计算出碳酸氢铵中氮元素的质量分数,再根据所含的氮元素质量相等进行计算即可.
(2)根据尿素(化学式CO(NH2)2,求一个尿素分子中所含原子数;
(3)根据尿素(化学式CO(NH2)2,求尿素中碳元素:氧元素:氮元素:氢元素的质量比;
(4)尿素中氮元素的质量分数=
| 氮元素的相对原子质量×氮原子个数 |
| 尿素的相对分子质量 |
(5)根据“60克×尿素中氮元素的质量分数”计算即可;CO(NH2)2
(6)先计算出碳酸氢铵中氮元素的质量分数,再根据所含的氮元素质量相等进行计算即可.
解答:解:
(1)尿素(化学式CO(NH2)2的化学式量为=12+16+(14+1×2)×2=60
(2)根据尿素(化学式CO(NH2)2,则一个尿素分子中所含原子数为8;
(3)根据尿素(化学式CO(NH2)2,则尿素中碳元素:氧元素:氮元素:氢元素质量比为3:4:7:1
(4)尿素中氮元素的质量分数=
×100%=
×100%=46.7%
(5)因为纯尿素中氮元素的质量分数为46.7%,而化肥尿素包装袋上部分信息见图:44.8%.则判断该化肥属于混合物;
(6)设:需要硝酸铵的质量为x.
100kg×44.8%=
×x
44.8kg=35%×x,解得x=128kg
答:要保证含氮量相当,所需硝酸铵128kg.
故答案为:
(1)60;(2)8;(3)3:4:7:1(4)46.7%(5)混合物;(6)128kg.
(1)尿素(化学式CO(NH2)2的化学式量为=12+16+(14+1×2)×2=60
(2)根据尿素(化学式CO(NH2)2,则一个尿素分子中所含原子数为8;
(3)根据尿素(化学式CO(NH2)2,则尿素中碳元素:氧元素:氮元素:氢元素质量比为3:4:7:1
(4)尿素中氮元素的质量分数=
| 氮元素的相对原子质量×2 |
| 尿素的化学式量 |
| 14×2 |
| 60 |
(5)因为纯尿素中氮元素的质量分数为46.7%,而化肥尿素包装袋上部分信息见图:44.8%.则判断该化肥属于混合物;
(6)设:需要硝酸铵的质量为x.
100kg×44.8%=
| 氮元素的相对原子质量×2 |
| 硝酸铵的相对分子质量 |
44.8kg=35%×x,解得x=128kg
答:要保证含氮量相当,所需硝酸铵128kg.
故答案为:
(1)60;(2)8;(3)3:4:7:1(4)46.7%(5)混合物;(6)128kg.
点评:本题主要考查学生运用化学式进行计算的能力.

练习册系列答案
 数学奥赛暑假天天练南京大学出版社系列答案
数学奥赛暑假天天练南京大学出版社系列答案
相关题目
根据下表判断,肉类变质过程中酸碱性的变化趋势是( )
| 名称 | 新鲜肉 | 次鲜肉 | 变质肉 |
| pH | 5.8~6.2 | 6.3~6.6 | >6.7 |
| A、酸性不变 | B、酸性变强 |
| C、酸性变弱 | D、碱性变弱 |
 小琴同学设计如图所示的A、B 两个实验.
小琴同学设计如图所示的A、B 两个实验.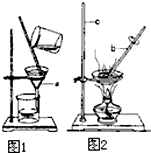 如图是粗盐提纯实验的两个主要操作示意图
如图是粗盐提纯实验的两个主要操作示意图