题目内容
有一包白色粉末可能由NaCl、NaNO3、MgCl2、CuSO4、中的一种或多种物质组成.小明为了探究其成分,设计并完成了如下图所示的实验.
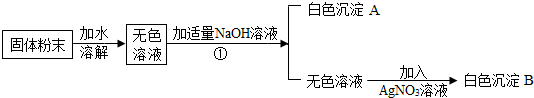
根据以上实验,回答:
(1)操作①是 ;
(2)原固体粉末中一定没有的成分是 ;
(3)生成沉淀A的化学方程式是 ;
(4)根据上述实验 (填‘能’或‘不能’)确定原固体粉末中含有NaCl、NaNO3.

根据以上实验,回答:
(1)操作①是
(2)原固体粉末中一定没有的成分是
(3)生成沉淀A的化学方程式是
(4)根据上述实验
考点:物质的鉴别、推断,盐的化学性质,书写化学方程式、文字表达式、电离方程式
专题:混合物组成的推断题
分析:(1)据图可知操作是过滤;
(2)根据硫酸铜溶于水得到蓝色溶液分析.
(3)根据氯化镁和氢氧化钠反应生成氢氧化镁白色沉淀和氯化钠书写;
(4)据于MgCl2存在,已提供了氯离子,硝酸钠不发生任何反应分析;
(2)根据硫酸铜溶于水得到蓝色溶液分析.
(3)根据氯化镁和氢氧化钠反应生成氢氧化镁白色沉淀和氯化钠书写;
(4)据于MgCl2存在,已提供了氯离子,硝酸钠不发生任何反应分析;
解答:解:(1)具体可知操作①是过滤;
(2)固体粉末加水溶解得到无色溶液,硫酸铜溶于水得到蓝色溶液,说明固体粉末中没有硫酸铜;
(3)无色溶液和氢氧化钠反应得到白色沉淀,因为氯化镁和氢氧化钠反应生成氢氧化镁白色沉淀和氯化钠,生成沉淀A的化学方程式是 MgCl2+2NaOH=Mg(OH)2↓+2NaCl;
(4)虽然加入AgNO3产生了白色沉淀B,但由于MgCl2存在,已提供了氯离子,因此不能判断氯化钠是否存在,硝酸钠不发生任何反应,所以也不能确定固体中是否含有硝酸钠;
故答案:(1)过滤(2)硫酸铜(3)MgCl2+2NaOH=Mg(OH)2↓+2NaCl(4)不能
(2)固体粉末加水溶解得到无色溶液,硫酸铜溶于水得到蓝色溶液,说明固体粉末中没有硫酸铜;
(3)无色溶液和氢氧化钠反应得到白色沉淀,因为氯化镁和氢氧化钠反应生成氢氧化镁白色沉淀和氯化钠,生成沉淀A的化学方程式是 MgCl2+2NaOH=Mg(OH)2↓+2NaCl;
(4)虽然加入AgNO3产生了白色沉淀B,但由于MgCl2存在,已提供了氯离子,因此不能判断氯化钠是否存在,硝酸钠不发生任何反应,所以也不能确定固体中是否含有硝酸钠;
故答案:(1)过滤(2)硫酸铜(3)MgCl2+2NaOH=Mg(OH)2↓+2NaCl(4)不能
点评:本题考查了酸碱盐的知识.硫酸铜溶于水形成硫酸溶液和氢氧化镁是不溶于水的白色沉淀,熟练掌握这些知识和复分解反应发生的条件就可较快解答该题.

练习册系列答案
相关题目
化学用语是学习化学的重要工具,下列与含义相符的是( )
| A、4Fe2+:4个铁离子 |
| B、N2O3:1个三氧化二氮分子 |
| C、Ca+2:显+2价的钙元素 |
| D、2H:1个氢分子由2个氢原子构成 |
下列化肥中,不能跟碱性物质混用的是( )
| A、氯化钾 | B、尿素 |
| C、磷矿粉 | D、硝酸铵 |
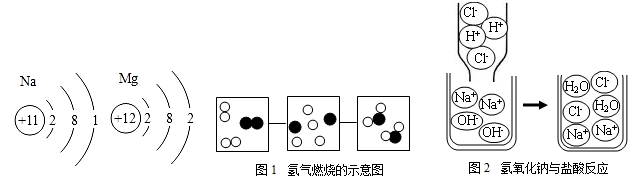
 某兴趣小组根据实验室提供的仪器和药品进行了氧气的制备实验.
某兴趣小组根据实验室提供的仪器和药品进行了氧气的制备实验.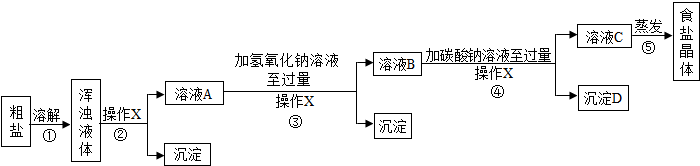
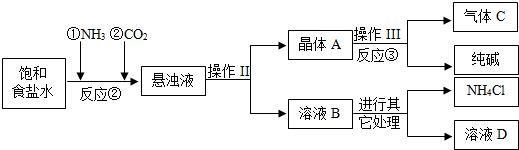
 把某稀硫酸分为等体积的两份,放入两个烧杯中,分别加入等质量的甲、乙两种金属,反应后金属都没有剩余,产生H2的质量随时间变化的趋势如图.下列说法正确的是
把某稀硫酸分为等体积的两份,放入两个烧杯中,分别加入等质量的甲、乙两种金属,反应后金属都没有剩余,产生H2的质量随时间变化的趋势如图.下列说法正确的是