题目内容
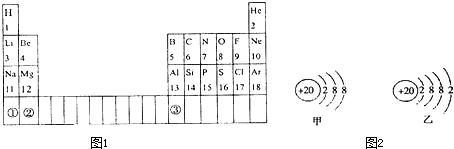
图1为元素周期表的部分示意图,请利用下表回答相关问题.
(1)一个水分子共有
(2)我发现如下规律:①在化学反应中,第1纵行的元素比较容易
②从原子结构方面看:同一横行的元素具有相同的
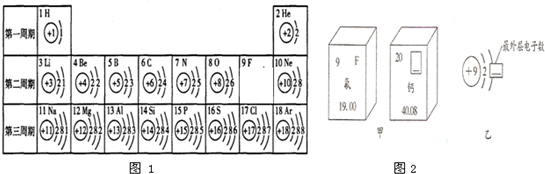
(3)图2甲是两种元素在周期表中的信息,图2乙是氟原子的原子结构示意图.请完成下列问题:
图甲方框的横线上填的是

(1)一个水分子共有
3
3
个原子核、10
10
个质子.一个Mg2+核外共有10
10
个电子;Cl-的最外层电子数和氩
氩
原子的最外层电子数相同.(2)我发现如下规律:①在化学反应中,第1纵行的元素比较容易
失
失
电子(除H外);第6纵行的元素比较容易得
得
电子;都通常达到8个电子的稳定结构.可见元素的化学性质主要决定于原子的最外层电子
最外层电子
数.②从原子结构方面看:同一横行的元素具有相同的
电子层
电子层
数;同一纵行的元素具有相同的最外层电子
最外层电子
数.(3)图2甲是两种元素在周期表中的信息,图2乙是氟原子的原子结构示意图.请完成下列问题:
图甲方框的横线上填的是
Ca
Ca
,图乙方框横线上的数字是7
7
.分析:(1)根据水的化学式分析分子构成,质子数,根据粒子结构示意图分析
(2)根据元素周期表及原子结构示意图的特点分析
(3)根据元素周期表中一个小方格中的信息及原子结构特点分析
(2)根据元素周期表及原子结构示意图的特点分析
(3)根据元素周期表中一个小方格中的信息及原子结构特点分析
解答:解:(1)水分子化学式为H2O,一个水分子中含有两个氢原子和一个氧原子,共有三个原子核,氢原子质子数为1,氧原子质子数为8,故共有 10个质子.一个Mg2+核外共有 10个电子;Cl-的最外层电子数是8,和 氖原子和原子的最外层电子数相同.
(2)①在化学反应中,第1纵行的元素最外层电子数为1,容易 失电子(除H外);第6纵行的元素最外层上的电子数为6,比较容易 得电子;达到8个电子的稳定结构.元素的化学性质主要决定于原子的最外层电子数.
②同一横行的元素电子层数相同;同一纵行的元素最外层电子数相同.
(3)元素周期表中每小方格右上角符号表示元素符号,故图甲方框的横线上填的是 Ca,原子中,质子数等于核外电子数,故方框横线上的数字是 7.
故答案为:(1)3、10 10 氩(2)失 得 最外层电子.
②电子层 最外层电子.(3)Ca,7.
(2)①在化学反应中,第1纵行的元素最外层电子数为1,容易 失电子(除H外);第6纵行的元素最外层上的电子数为6,比较容易 得电子;达到8个电子的稳定结构.元素的化学性质主要决定于原子的最外层电子数.
②同一横行的元素电子层数相同;同一纵行的元素最外层电子数相同.
(3)元素周期表中每小方格右上角符号表示元素符号,故图甲方框的横线上填的是 Ca,原子中,质子数等于核外电子数,故方框横线上的数字是 7.
故答案为:(1)3、10 10 氩(2)失 得 最外层电子.
②电子层 最外层电子.(3)Ca,7.
点评:本题考查学生对元素周期表的认识和应用,注重了对基础知识的考查,明确周期表中的一个小格中的信息,并利用周期和族来寻找规律,较好的训练了学生分析解决问题的能力.

练习册系列答案
相关题目
如图1为元素周期表的部分内容,结合表中内容回答问题.
| 族 周期 | ⅠA | 0 | ||||||
| 1 | 1 H 氢 | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 2 He 氦 |
| 2 | 3 Li 锂 | 4 Be 铍 | 5 B 硼 | 6 C 碳 | 7 N 氮 | 8 O 氧 | 9 F 氟 | 10 Ne 氖 |
| 3 | 11 Na 钠 | 12 Mg 镁 | 13 Al 铝 | 14 Si 硅 | 15 P 磷 | 16 S 硫 | 17 Cl 氯 | 18 Ar 氩 |
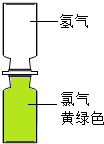
图2
(1)12号元素镁的元素符号为______.
(2)氟元素的原子结构示意图为
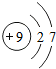 ,从原子结构分析,下列元素化学性质与氟相似的是______(填序号).
,从原子结构分析,下列元素化学性质与氟相似的是______(填序号).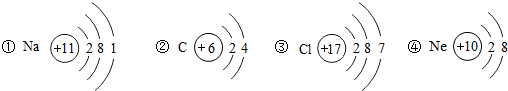
(3)某种钠原子的相对原子质量为23,该钠原子核内的中子数为______.
(4)小红取一瓶氢气和一瓶氯气进行实验.首先将氢气和氯气按图2所示装置放置,抽掉玻璃片,过一会观察到______,产生这一现象的原因是______.然后点燃一段镁条,靠近集气瓶,氢气和氯气在光照条件下发生爆炸,生成稳定的化合物氯化氢,该反应的化学方程式为______.
如图1为元素周期表的部分内容,结合表中内容回答问题.
图1
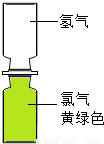
图2
(1)12号元素镁的元素符号为 .
(2)氟元素的原子结构示意图为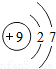 ,从原子结构分析,下列元素化学性质与氟相似的是 (填序号).
,从原子结构分析,下列元素化学性质与氟相似的是 (填序号).
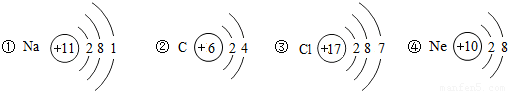
(3)某种钠原子的相对原子质量为23,该钠原子核内的中子数为 .
(4)小红取一瓶氢气和一瓶氯气进行实验.首先将氢气和氯气按图2所示装置放置,抽掉玻璃片,过一会观察到 ,产生这一现象的原因是 .然后点燃一段镁条,靠近集气瓶,氢气和氯气在光照条件下发生爆炸,生成稳定的化合物氯化氢,该反应的化学方程式为 .
| 族 周期 | ⅠA | |||||||
| 1 | 1 H 氢 | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 2 He 氦 |
| 2 | 3 Li 锂 | 4 Be 铍 | 5 B 硼 | 6 C 碳 | 7 N 氮 | 8 O 氧 | 9 F 氟 | 10 Ne 氖 |
| 3 | 11 Na 钠 | 12 Mg 镁 | 13 Al 铝 | 14 Si 硅 | 15 P 磷 | 16 S 硫 | 17 Cl 氯 | 18 Ar 氩 |

图2
(1)12号元素镁的元素符号为 .
(2)氟元素的原子结构示意图为
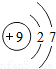 ,从原子结构分析,下列元素化学性质与氟相似的是 (填序号).
,从原子结构分析,下列元素化学性质与氟相似的是 (填序号).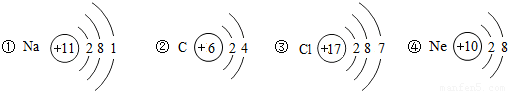
(3)某种钠原子的相对原子质量为23,该钠原子核内的中子数为 .
(4)小红取一瓶氢气和一瓶氯气进行实验.首先将氢气和氯气按图2所示装置放置,抽掉玻璃片,过一会观察到 ,产生这一现象的原因是 .然后点燃一段镁条,靠近集气瓶,氢气和氯气在光照条件下发生爆炸,生成稳定的化合物氯化氢,该反应的化学方程式为 .

 ,从原子结构分析,下列元素化学性质与氟相似的是
,从原子结构分析,下列元素化学性质与氟相似的是