题目内容
(2012?金山区一模)如图1为元素周期表的部分内容,结合表中内容回答问题.
图1

图2
(1)12号元素镁的元素符号为
(2)氟元素的原子结构示意图为 ,从原子结构分析,下列元素化学性质与氟相似的是
,从原子结构分析,下列元素化学性质与氟相似的是

(3)某种钠原子的相对原子质量为23,该钠原子核内的中子数为
(4)小红取一瓶氢气和一瓶氯气进行实验.首先将氢气和氯气按图2所示装置放置,抽掉玻璃片,过一会观察到
| 族 周期 |
ⅠA | 0 | ||||||
| 1 | 1 H 氢 |
ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 2 He 氦 |
| 2 | 3 Li 锂 |
4 Be 铍 |
5 B 硼 |
6 C 碳 |
7 N 氮 |
8 O 氧 |
9 F 氟 |
10 Ne 氖 |
| 3 | 11 Na 钠 |
12 Mg 镁 |
13 Al 铝 |
14 Si 硅 |
15 P 磷 |
16 S 硫 |
17 Cl 氯 |
18 Ar 氩 |

图2
(1)12号元素镁的元素符号为
Mg
Mg
.(2)氟元素的原子结构示意图为
 ,从原子结构分析,下列元素化学性质与氟相似的是
,从原子结构分析,下列元素化学性质与氟相似的是③
③
(填序号).
(3)某种钠原子的相对原子质量为23,该钠原子核内的中子数为
12
12
.(4)小红取一瓶氢气和一瓶氯气进行实验.首先将氢气和氯气按图2所示装置放置,抽掉玻璃片,过一会观察到
上下都变为黄绿色,但颜色较原Cl2的颜色浅
上下都变为黄绿色,但颜色较原Cl2的颜色浅
,产生这一现象的原因是分子在不断运动
分子在不断运动
.然后点燃一段镁条,靠近集气瓶,氢气和氯气在光照条件下发生爆炸,生成稳定的化合物氯化氢,该反应的化学方程式为H2+Cl2
2HCl
| ||
H2+Cl2
2HCl
.
| ||
分析:(1)根据质子数决定元素种类解答.
(2)最外层相似的原子化学性质相似.
(3)根据相对原子质量=质子数+中子数.
(4)根据分子不断运动解答.
(2)最外层相似的原子化学性质相似.
(3)根据相对原子质量=质子数+中子数.
(4)根据分子不断运动解答.
解答:解:(1)12号元素镁的元素符号为镁元素,符号为Mg.
(2)氟元素的原子最外层有7个电子,最外层电子数相同的原子化学性质相似,故选③
(3)某种钠原子的相对原子质量为23,钠原子的质子数为11,相对原子质量等于质子数+中子数,所以钠原子核内的中子数为12.
(4)由于分子不断运动,所以当抽掉玻璃片时,氯气分子和氢气分子不断运动,上下都变为黄绿色,但颜色较原Cl2的颜色浅,氢气和氯气在光照条件下发生爆炸,生成稳定的化合物氯化氢,反应的化学方程式为:H2+Cl2
2HCl
故答案为:(1)Mg.
(2)③
(3)12.
(4)上下都变为黄绿色,但颜色较原Cl2的颜色浅,分子在不断运动. H2+Cl2
2HCl
(2)氟元素的原子最外层有7个电子,最外层电子数相同的原子化学性质相似,故选③
(3)某种钠原子的相对原子质量为23,钠原子的质子数为11,相对原子质量等于质子数+中子数,所以钠原子核内的中子数为12.
(4)由于分子不断运动,所以当抽掉玻璃片时,氯气分子和氢气分子不断运动,上下都变为黄绿色,但颜色较原Cl2的颜色浅,氢气和氯气在光照条件下发生爆炸,生成稳定的化合物氯化氢,反应的化学方程式为:H2+Cl2
| ||
故答案为:(1)Mg.
(2)③
(3)12.
(4)上下都变为黄绿色,但颜色较原Cl2的颜色浅,分子在不断运动. H2+Cl2
| ||
点评:明确质子数决定元素种类,相对原子质量等于质子数+中子数,分子不断运动的知识是解答本题关健.

练习册系列答案
相关题目
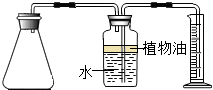 (2012?金山区一模)小明买了一种“汽泡爽”的冲调饮料.小明观察了饮料说明后,他借助化学实验的方法,探究“汽泡爽”产生气体的成分,以及加水温度对产生气体量的影响.
(2012?金山区一模)小明买了一种“汽泡爽”的冲调饮料.小明观察了饮料说明后,他借助化学实验的方法,探究“汽泡爽”产生气体的成分,以及加水温度对产生气体量的影响.