题目内容
8.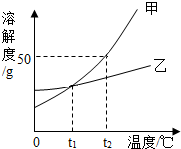 甲、乙两种物质的溶解度曲线如图所示,下列说法正确的是( )
甲、乙两种物质的溶解度曲线如图所示,下列说法正确的是( )| A. | 甲的溶解度大于乙的溶解度 | |
| B. | 当甲物质中混有少量杂质乙可用降温结晶法提纯 | |
| C. | t1℃时,甲、乙两种物质的溶液中,溶质质量分数相等 | |
| D. | t2℃时,甲饱和溶液溶质质量分数为50% |
分析 A、比较溶解度大小须确定温度;
B、据甲乙的溶解度受温度影响情况分析提纯物质的方法;
C、不知溶液中溶质、溶剂质量多少,无法判断溶质质量分数大小;
D、据饱和溶液中溶质的质量分数计算方法解答.
解答 解:A、比较溶解度大小须确定温度,温度低于t1℃时,甲的溶解度小于乙的溶解度,故错误;
B、甲的溶解度受温度影响 较大,乙的溶解度受温度较小,所以当甲物质中混有少量杂质乙可用降温结晶法提纯甲,正确;
C、不知溶液中溶质、溶剂质量多少,无法判断溶质质量分数大小,若饱和,则相等,故错误;
D、饱和溶液中溶质的质量分数=$\frac{溶解度}{溶解度+100g}$×100%,t2℃时甲的溶解度是50g,则甲饱和溶液溶质质量分数为$\frac{50g}{150g}$×100%<50%,故错误;
故选:B.
点评 本题主要考查了溶解度曲线及饱和溶液中溶质的质量分数的计算方法、物质的分离提纯等知识,据相关知识分析解答即可.

练习册系列答案
 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案
相关题目
5.推理是化学学习中常用的一种思维方法.下列推理正确的是( )
| A. | 铁和铜均是金属,铁嫩与稀硫酸反应生成氢气,则铜也能与稀硫酸反应生成氢气 | |
| B. | 离子是带电的粒子,则带电的粒子一定是离子 | |
| C. | 点燃H2和O2的混合气体可能发生爆炸,则点燃CH4与O2的混合气体也可能发生爆炸 | |
| D. | 酸溶液的pH<7,所以pH<7的溶液一定是酸溶液 |
16.某同学发现,上个月做实验用的氢氧化钠溶液忘记了盖瓶盖,对于该溶液是否变质,同学们提出了如下假设:
【猜想】猜想一:没有变质; 猜想二:部分变质; 猜想三:全部变质.
【查阅资料】Na2CO3溶液呈碱性.
【进行实验】对猜想二进行验证.
写出上述实验步骤(1)的化学方程式Na2CO3+BaCl2═2NaCl+BaCO3↓.
【反思】氢氧化钠溶液必须密封保存.
氢氧化钠溶液变质的原因(用化学方程表示)CO2+2NaOH═Na2CO3+H2O.
【猜想】猜想一:没有变质; 猜想二:部分变质; 猜想三:全部变质.
【查阅资料】Na2CO3溶液呈碱性.
【进行实验】对猜想二进行验证.
| 实验步骤 | 实验现象 | 结论 |
| (1)取少许该溶液于试管中,滴 入适量的BaCl2溶液. | 有白色沉淀 | 猜想二正确 |
| (2)静置上述溶液,取上层清液少许于另一支试管中,滴入几滴酚酞试液 | 溶液变红 |
【反思】氢氧化钠溶液必须密封保存.
氢氧化钠溶液变质的原因(用化学方程表示)CO2+2NaOH═Na2CO3+H2O.
3.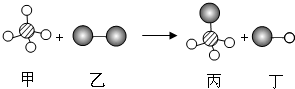 如图表示两种物质发生的化学反应,其中相同的球代表同种原子,小球间的短线代表原子间的结合(假定分别代表碳、氢、氧原子).下列说法中不正确的是( )
如图表示两种物质发生的化学反应,其中相同的球代表同种原子,小球间的短线代表原子间的结合(假定分别代表碳、氢、氧原子).下列说法中不正确的是( )
 如图表示两种物质发生的化学反应,其中相同的球代表同种原子,小球间的短线代表原子间的结合(假定分别代表碳、氢、氧原子).下列说法中不正确的是( )
如图表示两种物质发生的化学反应,其中相同的球代表同种原子,小球间的短线代表原子间的结合(假定分别代表碳、氢、氧原子).下列说法中不正确的是( )| A. | 图示丙分子由三种原子构成 | B. | 图示发生了复分解反应 | ||
| C. | 图示反应前后原子个数不变 | D. | 甲物质中碳、氢元素的质量比为3:1 |
20.下列说法错误的是( )
| A. | 分子、原子、离子都能构成物质 | |
| B. | 分子与原子的本质区别是化学变化中,分子可分而原子不可分 | |
| C. | 阳离子中核电荷数=核内质子数>核外电子数 | |
| D. | 温度升高,汞柱上升是因为原子体积变大 |
17.下列变化中,属于化学变化的是( )
| A. | 冰融化成水 | B. | 红磷燃烧 | C. | 矿石粉碎 | D. | 铜丝弯曲 |
18.炼铁厂以赤铁矿石、焦炭、石灰石、空气等为主要原料炼铁,主要反应过程如图所示:
请根据上图和所学知识判断下列说法错误的是( )

请根据上图和所学知识判断下列说法错误的是( )
| A. | 生铁属于混合物 | |
| B. | 反应过程①是置换反应,②③中属于化合反应 | |
| C. | 工业炼铁的设备是高炉 | |
| D. | 原料中焦炭的作用是提供能量和制取一氧化碳 |

