题目内容
3.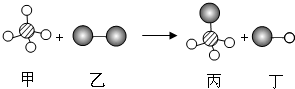 如图表示两种物质发生的化学反应,其中相同的球代表同种原子,小球间的短线代表原子间的结合(假定分别代表碳、氢、氧原子).下列说法中不正确的是( )
如图表示两种物质发生的化学反应,其中相同的球代表同种原子,小球间的短线代表原子间的结合(假定分别代表碳、氢、氧原子).下列说法中不正确的是( )| A. | 图示丙分子由三种原子构成 | B. | 图示发生了复分解反应 | ||
| C. | 图示反应前后原子个数不变 | D. | 甲物质中碳、氢元素的质量比为3:1 |
分析 A.根据分子结构来分析;
B.根据复分解反应的概念来分析;
C.根据质量守恒定律来分析;
D.根据化合物中元素质量比的计算方法来分析.
解答 解:A.由丙分子的结构示意图可知,丙分子是由三种原子构成的,故正确;
B.由该反应的生成物的微观模型示意图可知,反应物为一种化合物一种单质,生成物为两种化合物;复分解反应的反应物、生成物都是化合物.所以,该反应不属于复分解反应.故错误;
C.对比反应前后,原子的种类、数目不变.故正确;
D.甲物质的化学式为CH4,其中碳元素与氢元素的质量比为12:(1×4)=3:1,故正确.
故选B.
点评 分子由原子构成,构成不同的分子属于不同种物质的分子,由同种原子构成的分子属于单质分子,由不同种原子构成的分子属于化合物的分子.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
20.下列离子能在pH=2的水溶液中大量共存的是( )
| A. | Cl-、NO3-、K+、Na+ | B. | SO42-、NO3-、K+、OH- | ||
| C. | CO32-、SO42-、Mg2+ | D. | NH4+、Cl-、OH-、K+ |
14.下列实验不能达到目的是( )
| A. | 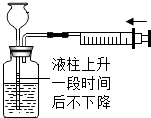 检查装置气密性 | B. | 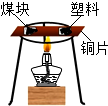 比较物质着火点 | ||
| C. | 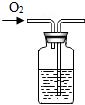 监控O2流速 | D. | 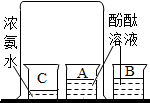 探究微粒运动 |
8.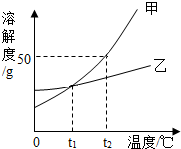 甲、乙两种物质的溶解度曲线如图所示,下列说法正确的是( )
甲、乙两种物质的溶解度曲线如图所示,下列说法正确的是( )
 甲、乙两种物质的溶解度曲线如图所示,下列说法正确的是( )
甲、乙两种物质的溶解度曲线如图所示,下列说法正确的是( )| A. | 甲的溶解度大于乙的溶解度 | |
| B. | 当甲物质中混有少量杂质乙可用降温结晶法提纯 | |
| C. | t1℃时,甲、乙两种物质的溶液中,溶质质量分数相等 | |
| D. | t2℃时,甲饱和溶液溶质质量分数为50% |
15.请用化学用语填空.
①1个一氧化二氮分子N2O;2个银原子2Ag;
②Na2SO4中含有的原子团名称为硫酸根;
③铝在空气中有良好的抗腐蚀性能的原因:4Al+3O2=2Al2O3(用反应方程式表示).
①1个一氧化二氮分子N2O;2个银原子2Ag;
②Na2SO4中含有的原子团名称为硫酸根;
③铝在空气中有良好的抗腐蚀性能的原因:4Al+3O2=2Al2O3(用反应方程式表示).
12.下列有关微粒的叙述中,错误的是( )
| A. | 温度越高分子运动越快 | |
| B. | 氯离子失去电子变成氯原子 | |
| C. | 分子可再分,原子不可再分 | |
| D. | 原子可以构成分子,也可以直接构成物质 |
 A、B、C、D是初中化学常见的物质,且为不同类别的化合物,A、B中都含有钙元素,它们之间的反应或转化关系如图所示(部分反应物、生成物及反应条件已略去)
A、B、C、D是初中化学常见的物质,且为不同类别的化合物,A、B中都含有钙元素,它们之间的反应或转化关系如图所示(部分反应物、生成物及反应条件已略去)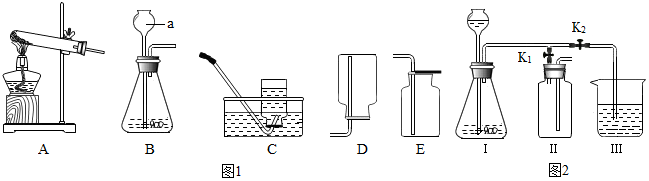
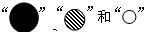 分别表示三种原子.
分别表示三种原子.