题目内容
6.实验是进行科学探究的重要途径.(1)下列实验室仪器不能用作反应容器的是c(填字母代号).
a.烧杯 b.试管 c.量筒 d.锥形瓶
(2)根据下面2个实验装置示意图回答相关问题.
①实验Ⅰ两支试管中出现现象的不同之处是A试管中无明显现象,B试管中产生白色沉淀,通过实验可认识到:虽然酸类物质具有相似的化学性质,但由于不同的酸溶于水时电离出的阴离子或酸根离子不同,其性质也存在差异.
②变量控制是科学研究常用的方法,例如我们在实验室做检验CO2的溶解性实验时需控制两个因素:一是两个塑料容器的容积相同,二是容器中加入的水量相同,则实验Ⅱ中控制的两个因素分别是温度、可燃物.
(3)某同学将一枚洁净的铁钉放入硫酸铜溶液中,观察到铁钉表面有红色的物质析出,且产生少量的气体,于是,他重新配制硫酸铜溶液,再次实验,又观察到相同的现象,请回答下列问题:
①产生的气体可能是H2;②由实验可以得出两种金属的活动性顺序是Fe>Cu.
(4)钢铁是使用最多的金属材料,如图3是实验室制备金属铁的装置图,要制得5.6g铁,最少需要多少克一氧化碳?

分析 (1)运用常见仪器的用途和使用方法解答;
(2)①酸类因为溶于水时电离出的阳离子相同,有形同的化学性质,又因为溶于水时电离出的阴离子或酸根离子不同,其性质也存在差异.
②根据燃烧的条件和实验中的现象分析;
(3)铁钉放入硫酸铜溶液中,观察到铁钉表面有红色的物质析出,且产生少量的气体,说明除了铁和硫酸铜反应生成铜和硫酸亚铁外还有其他的反应.
(4)根据化学方程式计算出所需一氧化碳的质量.
解答 解:(1)a、烧杯可用于做反应器,故错误;b、试管可用于加热也可用作反应器,故错误;c、量筒只能用于量取液体的体积不能用作反应器,故正确;d、锥形瓶可用作较大量液体的反应容器,故错误.
(2)①酸类因为溶于水时电离出的阳离子相同,有形同的化学性质,又因为溶于水时电离出的阴离子或酸根离子不同,其性质也存在差异.
②可燃物燃烧的条件是与氧气接触、达到着火点,图示中的白磷能够燃烧,是因为达到着火点,并且与空气接触;红磷不能燃烧是因为没有达到着火点.可燃物是否与氧气(或空气)接触,可燃物是否达到燃烧所需的温度.
(3)由质量守恒定律可知,溶液可能显酸性,生成的可能是氢气;铁和硫酸铜反应生成铜和硫酸亚铁的反应,说明金属活动性顺序:Fe>Cu
(4)设生成5.6g铁需要一氧化碳的质量为x.
3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2
84 112
x 5.6g
$\frac{84}{112}$=$\frac{x}{5.6g}$,x=4.2g.
故填:(1)c;(2)①A试管中无明显现象,B试管中产生白色沉淀; 阴离子或酸根离子;②温度;可燃物;(3)①H2;②Fe>Cu;(4)最少需要4.2克一氧化碳.
点评 用于量筒、试管、烧杯、集气瓶的用途和使用方法解答,平时复习时注意同类知识的积累和比较就能较快解答,正确完成化学实验的基础是要具备完备的化学知识,并且要了解各种实验的特点.

 字词句段篇系列答案
字词句段篇系列答案| A. | 有机物:CH4、H2CO3 | B. | 复合肥料:硝酸钾、磷酸氢二铵 | ||
| C. | 化合物:合金、胆矾 | D. | 合成材料:淀粉、塑料 |
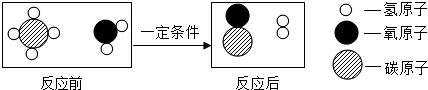 甲烷和水反应可以制水煤气(混合气体),其反应的微观示意图如图所示:根据以上微观 示意图得出的结论中.正确的是( )
甲烷和水反应可以制水煤气(混合气体),其反应的微观示意图如图所示:根据以上微观 示意图得出的结论中.正确的是( )| A. | 该反应属于置换反应 | |
| B. | 水煤气的成分是一氧化碳和氧气 | |
| C. | 该反应中含氢元素的化合物有3种 | |
| D. | 该反应的化学方程式中甲烷和水的计量数之比为1:1 |
| 第1次 | 第2次 | 第3次 | |
| 所取样品的质量 | 20g | 20g | 20g |
| 所取稀盐酸的质量 | 80g | 100g | 120g |
| 生成CO2的质量 | 3.58g | 4.4g | 4.4g |
(2)求原样品中Ca(OH)2的质量分数?
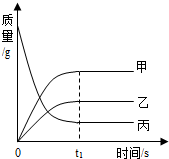 如图反映了某个化学反应各物质质量与时间的关系.
如图反映了某个化学反应各物质质量与时间的关系.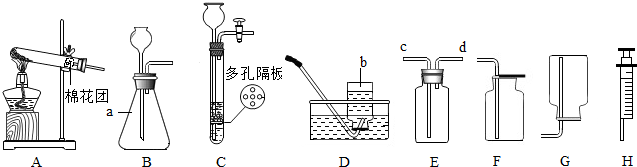
 如图是探究酒精灯灯焰结构及性质的实验示意图:请写出图中所示灯焰各部分的名称:
如图是探究酒精灯灯焰结构及性质的实验示意图:请写出图中所示灯焰各部分的名称: 知某混合物中只含Na2CO3和NaOH.现取该样品26.2g,逐滴加入稀盐酸,生成的二氧化碳与滴加的稀盐酸的质量关系如图所示:
知某混合物中只含Na2CO3和NaOH.现取该样品26.2g,逐滴加入稀盐酸,生成的二氧化碳与滴加的稀盐酸的质量关系如图所示: