题目内容
16. 针对市场上一些不法商贩使用有毒的SO2气体对某些食品进行漂白,某科技兴趣小组以小麦幼叶为实验对象,研究SO2对植物的危害.他们通过查阅资料,得知硫酸溶液与固态的亚硫酸钠(Na2SO3)反应可产生SO2气体,设计实验如图所示.
针对市场上一些不法商贩使用有毒的SO2气体对某些食品进行漂白,某科技兴趣小组以小麦幼叶为实验对象,研究SO2对植物的危害.他们通过查阅资料,得知硫酸溶液与固态的亚硫酸钠(Na2SO3)反应可产生SO2气体,设计实验如图所示.(1)该小组从实验室取得溶质质量分数为75%硫酸溶 液100克,含溶质硫酸75克;
(2)该小组若想制取0.64克二氧化硫,至少需要亚 硫酸钠多少克?(化学方程式为Na2SO3+H2SO4=Na2SO4+SO2↑+H2O)
分析 (1)由溶液质量和溶质质量分数根据溶质质量分数的计算公式可以计算出溶质质量.
(2)由生成二氧化硫的质量根据化学方程式可以计算出参加反应的亚硫酸钠溶液的质量.
解答 解:(1)含硫酸的质量为100g×75%=75g;故填:75;
(2)设需要亚硫酸钠的质量为x.
Na2SO3+H2SO4=Na2SO4+SO2↑+H2O
126 64
x 0.64g
$\frac{126}{x}=\frac{64}{0.64g}$
解得x=1.26g
答:需要亚硫酸钠的质量为1.26g.
点评 本题考查溶质质量分数的计算、有关化学方程式的计算、碱的化学性质、实验探究二氧化硫的危害等知识,难度稍大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
8.通过下列图示实验得出的结论中正确的是( )
| A. |  实验既说明甲烷具有可燃性,又说明甲烷中含有碳、氢两种元素 实验既说明甲烷具有可燃性,又说明甲烷中含有碳、氢两种元素 | |
| B. |  实验既说明二氧化碳密度比空气大,又说明二氧化碳不能燃烧也不支持燃烧 实验既说明二氧化碳密度比空气大,又说明二氧化碳不能燃烧也不支持燃烧 | |
| C. |  实验既说明氧气约占空气质量的$\frac{1}{5}$,又说明氮气不溶于水也不支持燃烧 实验既说明氧气约占空气质量的$\frac{1}{5}$,又说明氮气不溶于水也不支持燃烧 | |
| D. |  实验既可探究可燃物的燃烧条件,又说明红磷不是可燃物 实验既可探究可燃物的燃烧条件,又说明红磷不是可燃物 |
 2012年6月16日第三届亚沙会将在烟台海阳举行.它是亚洲最大的沙滩体育盛会.
2012年6月16日第三届亚沙会将在烟台海阳举行.它是亚洲最大的沙滩体育盛会.



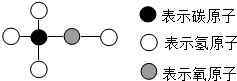 长江商报消息3月23日起,宜昌市五峰土家族自治县相继发生散装白酒致人死亡事件,至25日晚10时,已有4人因疑似甲醇中毒死亡,甲醇有剧毒,不能食用,其分子结构可如图所示的模型表示.从模型可看出甲醇由三种元素组成,其的化学式为CH4O.
长江商报消息3月23日起,宜昌市五峰土家族自治县相继发生散装白酒致人死亡事件,至25日晚10时,已有4人因疑似甲醇中毒死亡,甲醇有剧毒,不能食用,其分子结构可如图所示的模型表示.从模型可看出甲醇由三种元素组成,其的化学式为CH4O.