题目内容
11.下列仪器不能加热的容器的是( )| A. | 试管 | B. | 蒸发皿 | C. | 量筒 | D. | 烧杯 |
分析 根据常见的不能用于加热的仪器进行分析解答,不能加热的仪器有:漏斗、量筒、集气瓶等.
解答 解:通过我们学过的知识可知,能够直接加热的仪器有:试管、燃烧匙、蒸发皿和坩埚等;需要垫石棉网的是:烧杯、烧瓶、锥形瓶等;不能加热的仪器有:漏斗、量筒、集气瓶等.
A、试管可以用于直接加热,故选项错误.
B、蒸发皿可以用于直接加热,故选项错误.
C、量筒不能进行加热,故选项正确.
D、烧杯能进行加热,但必需垫上石棉网,故选项错误.
故选:C.
点评 本题难度不大,考查不能用于加热的仪器,了解常见仪器的名称、用途、注意事项等是解答本题的关键.

练习册系列答案
 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案
相关题目
2.安徽省凤形耐磨材料股份有限公司是一家高新技术企业,重点生产耐磨球段,耐磨球段是工业生产中关键设备的消耗品,可降低材料的损耗、提高研磨效率、实现节能减排的目标,下列选项中,你认为不属于化学研究范畴的是( )
| A. | 耐磨球段的组成与结构 | B. | 耐磨球段的变化与性质 | ||
| C. | 耐磨球段的运动状态 | D. | 耐磨球段的用途与制取 |
3.下列有关实验操作及分析均合理的是( )
| A. | 排水法收集O2:导气管口刚有气泡冒出立即收集,收集到的O2更纯净 | |
| B. | 测量液体体积:俯视导致测量出的液体体积偏小 | |
| C. | 测定空气里O2含量:点燃红磷慢慢伸入集气瓶并塞紧瓶塞,导致测定结果偏低 | |
| D. | 探究CO2性质:将CO2快速倒入盛有燃着蜡烛的烧杯中,便于观察低处蜡烛先熄灭 |
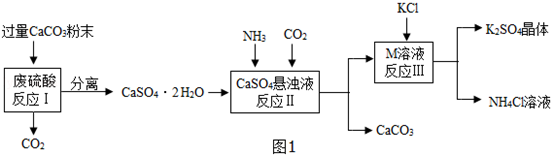
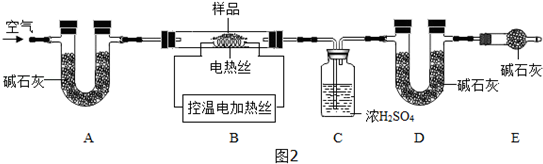
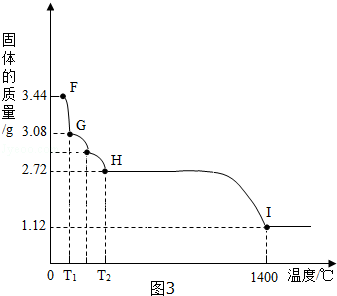
 大气是大自然对人类的恩赐,与人类的生存息息相关.
大气是大自然对人类的恩赐,与人类的生存息息相关.

