题目内容
4.硝酸铵(NH4NO3)是农村最常用的一种化肥,因其含氮量高而深受农民的喜爱,其市场价为860元/t,请计算:(1)硝酸铵(NH4NO3)中各元素的质量比.
(2)现用1000元买硝酸铵,请问所购买到的化肥中含氮元素的质量是多少吨?
分析 (1)根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解答.
(2)先根据市场价计算出所能购买硝酸铵的质量,再根据“物质质量×元素质量分数=元素质量”计算化肥中所含氮元素的质量.
解答 解:(1)硝酸铵中氮、氢、氧三种元素之间的质量之比是:MN:MH:MO=(14×2):(1×4):(16×3)=7:1:12.
(2)1000元所购买硝酸铵的质量为:1000元÷860元/t=1.163t;
所购买到的化肥中含氮元素的质量为:1.163t×$\frac{14×2}{14+1×4+14+16×3}×100%$=0.41t.
故答案为答:(1)MN:MH:MO=7:1:12;(2)0.41t
点评 本题难度不大,考查同学们灵活运用化学式的有关计算进行分析问题、解决问题的能力.

练习册系列答案
 小题狂做系列答案
小题狂做系列答案
相关题目
14.在相同分子个数的H2O2和H2O中,下列叙述不正确的是( )
| A. | 氢分子个数一样多 | B. | 氢原子个数一样多 | ||
| C. | H2O2和H2O的质量比为17:9 | D. | 氢元素质量一样多 |
19.下列变化属于化学变化的是( )
| A. | 燃放烟花 | B. | 电灯发光 | ||
| C. | 蜡烛熔化 | D. | 分离液态空气制氧气 |
16.下列物质属于碱的是( )
| A. | BaCl2 | B. | H2SO4 | C. | NH3.H2O | D. | CaO |
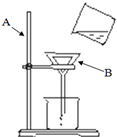 如图是实验室中进行过滤操作的示意图.请回答下列问题:
如图是实验室中进行过滤操作的示意图.请回答下列问题: