题目内容
8. 图甲是某元素在元素周期表中的部分信息,图乙是该元素的一种粒子结构示意图.
图甲是某元素在元素周期表中的部分信息,图乙是该元素的一种粒子结构示意图.①该元素的原子的核电荷数为16,该原子的最外层电子数为6.
②图乙所示粒子的符号为S2-.
分析 ①由题目中的图可知原子序数,再根据“原子序数=核内质子数=核外电子数=核电荷数”,可知该元素的原子的核电荷数以及最外层电子数;
②图乙所示粒子的符号符合“阴离子中,核电荷数(等于)质子数(小于)核外电子数”,故为阴离子,得2个电子,带2个负电荷,故可书写其化学符号
解答 解:①由题目中的图可知原子序数为16;再根据“原子序数=核内质子数=核外电子数=核电荷数”,可知该元素的原子的核电荷数16;最外层电子数为6;
②由分析可知,图乙所示粒子的符号为阴离子,得2个电子,带2个负电荷,故可书写其化学符号S2-.
故答为:(1)16;6;(2)S2-.
点评 了解元素周期表的特点及其应用;掌握相对原子质量的概念及其计算;掌握原子结构示意图与离子结构示意图的区别、特点;了解化学符号及其周围数字的意义.

练习册系列答案
 小学课时特训系列答案
小学课时特训系列答案
相关题目
18.新买的铝锅、铝壶烧开水时,凡是水浸到的地方都会变黑,说明水中溶有( )
| A. | 钾的化合物溶液 | B. | 钠的化合物溶液 | C. | 钙的化合物溶液 | D. | 铁的化合物溶液 |
16.下列属于分解反应的是( )
| A. | 磷+氧气$\stackrel{点燃}{→}$五氧化二磷 | |
| B. | 氧化铜+一氧化碳$\stackrel{点燃}{→}$铜+二氧化碳 | |
| C. | 碳酸氢钙$\stackrel{点燃}{→}$碳酸钙+水+二氧化碳 | |
| D. | 甲烷+氧气$\stackrel{点燃}{→}$二氧化碳+水 |
13.下列哪种试剂能鉴别出硫酸、氢氧化钠和氯化钠三种无色稀溶液( )
| A. | 石蕊溶液 | B. | 稀盐酸 | C. | 碳酸钠溶液 | D. | 氯化钾溶液 |
20.在一定质量NaOH溶液中逐滴加入稀盐酸,如图中能正确表示溶液的pH变化的是(横坐标表示加入稀盐酸的质量,纵坐标表示溶液的pH)( )
| A. | 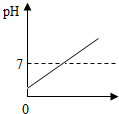 稀盐酸的体积 | B. | 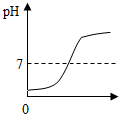 稀盐酸的体积 | C. | 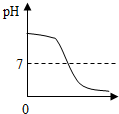 稀盐酸的体积 | D. | 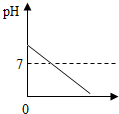 稀盐酸的体积 |
17.下列物质属于纯净物的是( )
| A. | 石灰石 | B. | 干冰 | C. | 澄清石灰水 | D. | 家用煤气 |
18.食品包装中经常用到铝箔.铝能制成铝箔是因为铝具有良好的( )
| A. | 延展性 | B. | 导电性 | C. | 抗腐蚀性 | D. | 传热性 |
