题目内容
19.下列实验方案设计正确的是( )| 选项 | 实验目的 | 实验方案 |
| A | 检验氧气是否收集满 | 将带火星的木条伸入集气瓶内 |
| B | 除去一氧化碳气体中昏有点二氧化碳 | 将混合气体通过灼热的氧化铜粉末 |
| C | 鉴别硬水和软水 | 加肥皂水,振荡后观察现象 |
| D | 获取纯净水 | 将河水过滤 |
| A. | A、 | B. | B、 | C. | C、 | D. | D、 |
分析 A、氧气能使带火星的木条复燃,将带火星的木条放在集气瓶口,如果带火星的木条复燃,说明已经集满,反之则没有集满;
B、一氧化碳能和灼热的氧化铜反应生成铜和二氧化碳;
C、鉴别硬水和软水,可加肥皂水,振荡后观察现象,若有大量气泡产生,则是软水,否则是硬水;
D、过滤不能除去水中可溶性矿物质.
解答 解:A、氧气能使带火星的木条复燃,将带火星的木条放在集气瓶口,如果带火星的木条复燃,说明已经集满,反之则没有集满,不能将木条伸入集气瓶内,该选项不能够达到实验目的;
B、一氧化碳能和灼热的氧化铜反应生成铜和二氧化碳,将混合气体通过灼热的氧化铜时,一氧化碳转化成二氧化碳,该选项不能达到实验目的;
C、鉴别硬水和软水,可加肥皂水,振荡后观察现象,若有大量气泡产生,则是软水,否则是硬水,该选项能够达到实验目的;
D、过滤不能除去水中可溶性矿物质,不能获取纯净水,该选项不能够达到实验目的.
故选:C.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

练习册系列答案
相关题目
7.在反应2A+B=3C+D中,A和B的相对分子量之比为5:1,已知20gA与一定量B恰好完全反应,生成5gD,则在此反应中,B和C的质量之比为( )
| A. | 2:17 | B. | 1:3 | C. | 3:5 | D. | 4:9 |
14.下列物质属于氧化物的是( )
| A. | 氯酸钾 | B. | 水 | C. | 氧气 | D. | 空气 |
4.如图为实验室常用的制取气体装置:
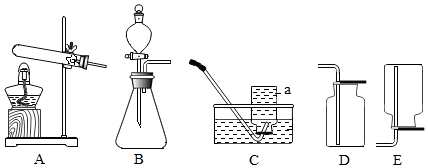
(1)仪器a的名称是集气瓶;组装A装置时,酒精灯应在固定试管之前(填“前”或“后”)放置.
(2)实验室用高锰酸钾制取氧气,反应的化学方程式:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑,宜选用的发生装置是A(填装置标号,下同),不宜选用的收集装置是E.
(3)实验室制取二氧化碳的研究中,在其他条件相同的情况下,进行如下实验:
①实验室制取二氧化碳的化学方程式:CaCO3+2HCl=CaCl2+H2O+CO2↑.
②若要研究盐酸浓度大小对反应快慢的影响,可选择实验甲与乙(填实验编号)对照.
③除盐酸的浓度外,上述实验研究的另一个影响反应快慢的因素是固体反应物的颗粒大小(或反应物的接触面积).
④研究发现盐酸的浓度越大,产生气体越快.与甲比较,下列对丁分析正确的是A(填标号)
A.反应更剧烈 B.产生的二氧化碳的质量更大 C.参加反应的大理石更多
(4)请从实验原理、原料、发生装置、操作等方面,阐述下列实验中可以产生较平稳气体的主要原因.

(1)仪器a的名称是集气瓶;组装A装置时,酒精灯应在固定试管之前(填“前”或“后”)放置.
(2)实验室用高锰酸钾制取氧气,反应的化学方程式:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑,宜选用的发生装置是A(填装置标号,下同),不宜选用的收集装置是E.
(3)实验室制取二氧化碳的研究中,在其他条件相同的情况下,进行如下实验:
| 实验标号 药品 | 甲 | 乙 | 丙 | 丁 |
| 大理石(m0g) | 块状 | 块状 | 粉末状 | 粉末状 |
| 盐酸(过量) | 稀盐酸 | 浓盐酸 | 稀盐酸 | 浓盐酸 |
②若要研究盐酸浓度大小对反应快慢的影响,可选择实验甲与乙(填实验编号)对照.
③除盐酸的浓度外,上述实验研究的另一个影响反应快慢的因素是固体反应物的颗粒大小(或反应物的接触面积).
④研究发现盐酸的浓度越大,产生气体越快.与甲比较,下列对丁分析正确的是A(填标号)
A.反应更剧烈 B.产生的二氧化碳的质量更大 C.参加反应的大理石更多
(4)请从实验原理、原料、发生装置、操作等方面,阐述下列实验中可以产生较平稳气体的主要原因.
| 实验目的 | 原料 | 发生装置 | 主要原因 |
| 制取氧气 | 粉末状二氧化锰和稀过氧化氢溶液 | B |
11.下列情况:①植物光合作用;②汽车尾气;③燃放烟花爆竹;④氢气燃烧;⑤煤的燃烧;⑥工业污水的任意排放.其中能引起大气污染的是( )
| A. | ①②③④⑤⑥ | B. | ②③⑤⑥ | C. | ②③④⑤ | D. | ②③⑤ |
8.学习化学的重要目的是要善于用化学知识去解决生产、生活中的问题.从化学角度看,下列做法中错误的是( )
| A. | 发生森林火灾时,消防人员开辟防火带防止火势蔓延 | |
| B. | 炒菜时油锅着火,用锅盖盖灭火焰 | |
| C. | 发现燃气(天然气、煤气等)泄漏,点火检查泄漏处 | |
| D. | 面粉加工厂、加油站严禁烟火 |
9.为了探究金属与酸反应的速率与哪些因素有关,小谷进行了以下实验探究:
【实验方案】
【发现问题】在同一反应中其速率也不一样.
【继续探究】小谷对锌粉与稀硫酸反应过程中速率的变化情况进行探究
在100mL稀硫酸中加入足量的锌粉,用图中的一种装置收集并测量氢气的体积,记录的实验数据如下表:
【讨论】(1)实验中测定反应产生氢气的体积可选用的装置是C(填序号)
(2)实验数据反映,锌与稀硫酸反应的速率是先逐渐加快,一段时间后反应速率逐渐变慢,其原因是锌与稀硫酸反应放热,反应速率加快,随着反应的进行,硫酸的浓度变小,反应速率变慢.
【实验方案】
| 实验步骤 | 现象 | 结论 |
| ①将足量铁粉与锌粉分别放入10%100mL稀硫酸中,观察现象 | 产生气泡速率 Fe<Zn | 反应速率与反应物的金属种类有关 |
| ②将等质量的锌粉与锌片分别放入10%100mL稀硫酸中,观察现象 | 产生气泡速率 锌粉>锌片 | 反应速率与反应物的接触面积大小有关 |
【继续探究】小谷对锌粉与稀硫酸反应过程中速率的变化情况进行探究
在100mL稀硫酸中加入足量的锌粉,用图中的一种装置收集并测量氢气的体积,记录的实验数据如下表:

| 时间(min) | 1 | 2 | 3 | 4 | 5 |
| 氢气体积(mL) | 50 | 120 | 232 | 290 | 310 |
(2)实验数据反映,锌与稀硫酸反应的速率是先逐渐加快,一段时间后反应速率逐渐变慢,其原因是锌与稀硫酸反应放热,反应速率加快,随着反应的进行,硫酸的浓度变小,反应速率变慢.
