题目内容
2.下列化学用语的书写及解释均正确的是( )| A. | H2-2个氢原子 | B. | 铁元素的化合价为+3-$\stackrel{+3}{Fe}$ | ||
| C. | 1个镁离子一Mg+2 | D. | 2N一2个氮元素 |
分析 A、原子的表示方法,用元素符号来表示一个原子,表示多个该原子,就在其元素符号前加上相应的数字.
B、化合价的表示方法,在该元素的上方用正负号和数字表示,正负号在前,数字在后.
C、离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略.若表示多个该离子,就在其离子符号前加上相应的数字.
D、原子的表示方法,用元素符号来表示一个原子,表示多个该原子,就在其元素符号前加上相应的数字.
解答 解:A、由原子的表示方法,用元素符号来表示一个原子,表示多个该原子,就在其元素符号前加上相应的数字,故2个氢原子表示为:2H,故选项说法错误.
B、由化合价的表示方法,在该元素的上方用正负号和数字表示,正负号在前,数字在后,故铁元素的化合价为+3可表示为:$\stackrel{+3}{Fe}$,故选项说法正确.
C、由离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略.1个镁离子可表示为:Mg2+,故选项化学用语书写错误.
D、由原子的表示方法,用元素符号来表示一个原子,表示多个该原子,就在其元素符号前加上相应的数字,故2N可表示2个氮原子,元素只讲种类、不讲个数,故选项说法错误.
故选:B.
点评 本题难度不大,掌握常见化学用语(原子符号、化合价、离子符号等)的书写方法、离子符号与化合价表示方法的区别等是正确解答此类题的关键.

练习册系列答案
 小题狂做系列答案
小题狂做系列答案
相关题目
17.下列实验现象描述错误的是( )
| A. | 将锌片放入少量稀硫酸中:银白色固体减少,固体表面产生气泡,放热 | |
| B. | 铝丝插入硫酸铜溶液中:银白色固体表面有紫红色固体析出,溶液由蓝色变为浅绿色 | |
| C. | 红磷在空气中燃烧:产生大量白色烟及黄色火焰,放热 | |
| D. | 氯化铵与熟石灰混合研磨:白色固体中产生刺激性气味的气体 |
7.氢化钙(CaH2)是一种常用的储氢材料,也是登山运动员常用的能源提供剂,某研究性学习小组模拟生产企业制取氢化钙.
【查阅资料】
Ⅰ白色的无水硫酸铜粉末吸水后会变蓝;
Ⅱ碱石灰是氧化钙和氢氧化钠的混合物;
Ⅲ钙、氢化钙遇水立即发生剧烈反应:Ca+2H2O=Ca(OH)2+H2↑;CaH2+2H2O=Ca(OH)2+2H2↑;
Ⅳ钙能燃烧生成氧化钙;氢化钙能燃烧生成氧化钙和水.
【实验原理】
用锌粒和稀硫酸反应制得干燥、纯净的氢气,再与金属钙在加热的条件下直接化合,即可制得CaH2.
(1)同学们设计了以下实验装置:
请回答:
①装置A中发生反应的化学方程式为Zn+H2SO4═ZnSO4+H2↑;为了实验安全,点燃C装置酒精灯前应先在E导管口收集氢气进行验纯或先通一会儿氢气;
②上图1装置B中装有无水氯化钙,其作用是干燥H2,若要证明进入C装置中的氢气已经干燥,在B、C之间应连接图2中的②(选填:①或②)装置;
③图1装置D中浓硫酸的作用是防止空气中的水蒸汽进入C中;
【进行实验)过程略
【验证产物】略
【实验拓展】(2)定性实验用化学方法鉴别Ca与CaH2,完成下表中内容.
(3)定量实验:测定Ca和CaH2混合物中CaH2的质量分数.

①取m1g样品与水完全反应,利用如图3装置测定生成的气体体积时,在a时进行收集(选填字母);
a.刚开始有气泡时 b.气泡连续均匀冒出时 C.气体经过验纯
②按图3实验装置进行测定时,甲同学发现,即使气密性良好,操作正确,测得的气体体积还是偏大,可能原因是因液体加入引起气体排出(或反应放热气体温度升高,体积膨胀引起气体排出),导致气体体积测定变大;(写出任一点即可)
③乙同学将实验装置改进为如图4(固定装置省略)所示,调整水准管高度,使量气装置两边的液面保持在同一水平面上,读取量气管中液面所示刻度为10.0mL.将Y形管慢慢倾斜,直至A中的水全部倒入B中,与样品混合反应,待反应结束后,冷却至室温,再次调节量气管与水准管液面相平,读取量气管中液面所示刻度为98.9mL.已知该实验条件下,氢气的密度为0.09mg/mL.样品中氢化钙的质量分数为66.3%;(结果精确到0.1%)
【反思与交流】
(4)登山运动员常用氢化钙作为能源提供剂,与氢气相比,其优点是氢化钙是固体,携带方便.既然金属钙与水反应也能生成氢气,为什么还要将金属钙制备成氢化钙呢?你的观点是等质量的钙和CaH2与水完全反应,CaH2产生的氢气多.
【查阅资料】
Ⅰ白色的无水硫酸铜粉末吸水后会变蓝;
Ⅱ碱石灰是氧化钙和氢氧化钠的混合物;
Ⅲ钙、氢化钙遇水立即发生剧烈反应:Ca+2H2O=Ca(OH)2+H2↑;CaH2+2H2O=Ca(OH)2+2H2↑;
Ⅳ钙能燃烧生成氧化钙;氢化钙能燃烧生成氧化钙和水.
【实验原理】
用锌粒和稀硫酸反应制得干燥、纯净的氢气,再与金属钙在加热的条件下直接化合,即可制得CaH2.
(1)同学们设计了以下实验装置:

请回答:
①装置A中发生反应的化学方程式为Zn+H2SO4═ZnSO4+H2↑;为了实验安全,点燃C装置酒精灯前应先在E导管口收集氢气进行验纯或先通一会儿氢气;
②上图1装置B中装有无水氯化钙,其作用是干燥H2,若要证明进入C装置中的氢气已经干燥,在B、C之间应连接图2中的②(选填:①或②)装置;
③图1装置D中浓硫酸的作用是防止空气中的水蒸汽进入C中;
【进行实验)过程略
【验证产物】略
【实验拓展】(2)定性实验用化学方法鉴别Ca与CaH2,完成下表中内容.
| 实验步骤 | 预期现象和结论 |
| 取少量固体样品,在干燥条件下与氧气反应,将 其产物通入装有无水硫酸铜的干燥管; | 若观察到无水硫酸铜变蓝色,证明是氢化钙,反之是钙 |

①取m1g样品与水完全反应,利用如图3装置测定生成的气体体积时,在a时进行收集(选填字母);
a.刚开始有气泡时 b.气泡连续均匀冒出时 C.气体经过验纯
②按图3实验装置进行测定时,甲同学发现,即使气密性良好,操作正确,测得的气体体积还是偏大,可能原因是因液体加入引起气体排出(或反应放热气体温度升高,体积膨胀引起气体排出),导致气体体积测定变大;(写出任一点即可)
③乙同学将实验装置改进为如图4(固定装置省略)所示,调整水准管高度,使量气装置两边的液面保持在同一水平面上,读取量气管中液面所示刻度为10.0mL.将Y形管慢慢倾斜,直至A中的水全部倒入B中,与样品混合反应,待反应结束后,冷却至室温,再次调节量气管与水准管液面相平,读取量气管中液面所示刻度为98.9mL.已知该实验条件下,氢气的密度为0.09mg/mL.样品中氢化钙的质量分数为66.3%;(结果精确到0.1%)
【反思与交流】
(4)登山运动员常用氢化钙作为能源提供剂,与氢气相比,其优点是氢化钙是固体,携带方便.既然金属钙与水反应也能生成氢气,为什么还要将金属钙制备成氢化钙呢?你的观点是等质量的钙和CaH2与水完全反应,CaH2产生的氢气多.
11.在科学研究中,常常通过实验的方法将不易观察的现象直观地反映出来.下列实验与这一思想方法不符合的是( )
| A. |  用红墨水和水扩散研究分子的运动 | B. |  以木块移动距离表示钢球动能大小 | ||
| C. |  用铁屑显示磁体周围磁场分布 | D. |  研究铁生锈 |
 某化学兴趣小组的同学取来50g某建筑废料于烧杯中,然后向烧杯中加入足量的8%稀盐酸进行反应,烧杯中剩余固体的质量与加入盐酸质量的关系如图所示.求:(假设该建筑废料中只有CaCO3与酸反应)
某化学兴趣小组的同学取来50g某建筑废料于烧杯中,然后向烧杯中加入足量的8%稀盐酸进行反应,烧杯中剩余固体的质量与加入盐酸质量的关系如图所示.求:(假设该建筑废料中只有CaCO3与酸反应)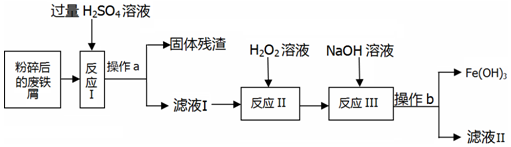


 钢铁是人类广泛使用的金属材料,请完成下列填空.
钢铁是人类广泛使用的金属材料,请完成下列填空.