题目内容
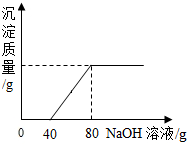
在一烧杯中盛有Na2CO3和NaOH的混合物10g,向其中加入100g水,固体全部溶解.向所得溶液中滴加澄清石灰水,产生沉淀的质量与滴入石灰水的质量关系曲线如图所示.请根据题意回答下列问题:(1)在滴入石灰水时,产生沉淀的颜色是______.
(2)当滴入石灰水至图中A点时,烧杯中溶液里含有的溶质是(写化学式)______.
(3)计算当滴入石灰水至图中B点时,溶液中溶质的质量为多少?(计算结果精确至0.1g)

【答案】分析:(1)Na2CO3和NaOH的混合溶液中滴加澄清石灰水,碳酸钠与氢氧化钙发生反应生成碳酸钙沉淀和氢氧化钠.
(2)当滴入石灰水至图中A点时,碳酸钠没有和氢氧化钙完全反应,碳酸钠有剩余,据此进行分析解答.
(3)当滴入石灰水至图中B点时,碳酸钠和氢氧化钙恰好完全反应,溶液中的溶质为氢氧化钠,根据生成的沉淀由反应的化学方程式进行分析计算即可.
解答:解:(1)Na2CO3和NaOH的混合溶液中滴加澄清石灰水,碳酸钠与氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,碳酸钙的颜色为白色.故答案为:白色;
(2)当滴入石灰水至图中A点时,碳酸钠没有和氢氧化钙完全反应,碳酸钠有剩余,故烧杯中溶液是氢氧化钠和碳酸钠的混合溶液,溶质是Na2CO3、NaOH.故答案为:Na2CO3、NaOH.
(3)解:设混合物中Na2CO3的质量为x,反应生成的NaOH的质量为y
Na2CO3+Ca(OH)2═CaCO3↓+2NaOH
106 100 80
x 5g y
 x=5.3g
x=5.3g
 y=4g
y=4g
溶液中溶质的质量为 10g-5.3g+4g=8.7g.
答:当滴入石灰水至图中B点时,溶液中溶质的质量为8.7g.
点评:本题难度不大,理解图形分析反应的进程、抓住“三点一趋势”(起点、拐点、终点和图象的变化趋势)、分析图象中所给数据的含义、正确的运用有关数据解决问题是解答此类题目的关键所在.
(2)当滴入石灰水至图中A点时,碳酸钠没有和氢氧化钙完全反应,碳酸钠有剩余,据此进行分析解答.
(3)当滴入石灰水至图中B点时,碳酸钠和氢氧化钙恰好完全反应,溶液中的溶质为氢氧化钠,根据生成的沉淀由反应的化学方程式进行分析计算即可.
解答:解:(1)Na2CO3和NaOH的混合溶液中滴加澄清石灰水,碳酸钠与氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,碳酸钙的颜色为白色.故答案为:白色;
(2)当滴入石灰水至图中A点时,碳酸钠没有和氢氧化钙完全反应,碳酸钠有剩余,故烧杯中溶液是氢氧化钠和碳酸钠的混合溶液,溶质是Na2CO3、NaOH.故答案为:Na2CO3、NaOH.
(3)解:设混合物中Na2CO3的质量为x,反应生成的NaOH的质量为y
Na2CO3+Ca(OH)2═CaCO3↓+2NaOH
106 100 80
x 5g y
 x=5.3g
x=5.3g  y=4g
y=4g 溶液中溶质的质量为 10g-5.3g+4g=8.7g.
答:当滴入石灰水至图中B点时,溶液中溶质的质量为8.7g.
点评:本题难度不大,理解图形分析反应的进程、抓住“三点一趋势”(起点、拐点、终点和图象的变化趋势)、分析图象中所给数据的含义、正确的运用有关数据解决问题是解答此类题目的关键所在.

练习册系列答案
相关题目
 已知Na2CO3的水溶液呈碱性,在一烧杯中盛有20.4g Na2CO3和NaCl组成的固体混合物.向其中逐渐滴加溶质质量分数为10%的稀盐酸.放出气体的总质量与所滴入稀盐酸的质量关系曲线如下图所示,请根据题意回答问题:
已知Na2CO3的水溶液呈碱性,在一烧杯中盛有20.4g Na2CO3和NaCl组成的固体混合物.向其中逐渐滴加溶质质量分数为10%的稀盐酸.放出气体的总质量与所滴入稀盐酸的质量关系曲线如下图所示,请根据题意回答问题: 在一烧杯中盛有42.2g CaCO3和CaCl2的粉末状混合物,向其中加入188.8g水,使混合物中的可溶物完全溶解.然后再向其中逐滴加入溶质的质量分数为10%的稀盐酸,烧杯中难溶固体物质的质量与所滴入稀盐酸的质量关系曲线如图X所示:
在一烧杯中盛有42.2g CaCO3和CaCl2的粉末状混合物,向其中加入188.8g水,使混合物中的可溶物完全溶解.然后再向其中逐滴加入溶质的质量分数为10%的稀盐酸,烧杯中难溶固体物质的质量与所滴入稀盐酸的质量关系曲线如图X所示: (2010?济南)在一烧杯中盛有一定质量的氧化铜,向其中加入足量的稀硫酸,至恰好完全反应,在一定温度下得到40gCuSO4的不饱和溶液.向所得溶液中逐滴滴入溶质质量分数为10%的NaOH溶液,溶液的总质量与滴入NaOH溶液的质量的质量关系曲线如图所示.请根据题意回答下列问题:
(2010?济南)在一烧杯中盛有一定质量的氧化铜,向其中加入足量的稀硫酸,至恰好完全反应,在一定温度下得到40gCuSO4的不饱和溶液.向所得溶液中逐滴滴入溶质质量分数为10%的NaOH溶液,溶液的总质量与滴入NaOH溶液的质量的质量关系曲线如图所示.请根据题意回答下列问题: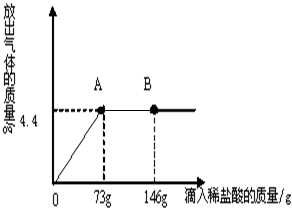 小刚在化学实验室发现,盛放NaOH溶液的试剂瓶瓶口和橡皮塞上出现了白色粉末.小刚叫来小军和小红,共同探究这种白色粉末的成分.
小刚在化学实验室发现,盛放NaOH溶液的试剂瓶瓶口和橡皮塞上出现了白色粉末.小刚叫来小军和小红,共同探究这种白色粉末的成分.