题目内容
8.某兴趣小组取一块6克生铁样品置于烧杯中(烧杯质量为50g),将100g稀硫酸均分为5次加入烧杯中(杂质不与稀硫酸反应且不溶于水),称得烧杯的质量见下表,请回答下列问题:| 序号 | 第1次 | 第2次 | 第3次 | 第4次 | 第5次 |
| 加入稀硫酸的质量/g | 20 | 20 | 20 | 20 | 20 |
| 剩余烧杯的总质量/g | 75.95 | m | 115.85 | 135.8 | 155.8 |
(2)计算生铁样品中铁的质量(写出计算过程).
分析 根据表中的数据对比分析可知,每20g的硫酸完全反应,生成氢气的质量为50g+6g+20g-75.95g=0.05g,由于在第三次时剩余烧杯的总质量总共有115.85g,由第四次剩余烧杯的总质量总共有135.8g,还有氢气生成,说明第二次反应后铁有剩余;由此可以求出m的值,根据生成氢气的质量求解生铁样品中铁的质量.
解答 解:(1)根据表中的数据对比分析可知,每20g的硫酸完全反应,生成氢气的质量为0.5g,由于在第三次时剩余烧杯的总质量总共有115.85g,由第四次剩余烧杯的总质量总共有135.8g,还有氢气生成,说明第二次反应后铁有剩余;由此为75.95g+20g-0.05g=95.9g;
(2)生成氧气的质量为:m(H2)=100+50+6-155.8=0.2g
设生铁样品中铁的质量为x
Fe+H2SO4=FeSO4+H2↑
56 2
x 0.2g
$\frac{56}{x}$=$\frac{2}{0.2g}$
x=5.6g
故答案为:(1)95.9;
(2)5.6g.
点评 本题主要考查了化学方程式的计算,难度不大,注意解题的规范性和准确性.

练习册系列答案
相关题目
18.下列实验操作中,正确的是( )
| A. | 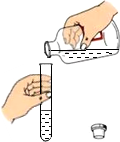 倾倒液体 倾倒液体 | B. |  铁在氧气中燃烧 | C. | 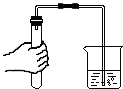 检查气密性 | D. |  熄灭酒精灯 |
3.下列说法错误的是( )
| A. | 密闭容器内的水中加入硝酸铵并搅拌后温度下降,是因为硝酸铵溶于水时吸热 | |
| B. | 汽油能洗去油污,是因为汽油能溶解油污 | |
| C. | 液氧可用于火箭发射,是因为氧气具有可燃性 | |
| D. | 用水可以灭火,是因为降低了可燃物的温度至着火点以下 |
13.水是生命之源,下面有关水的叙述正确的是( )
| A. | 水汽化时分子间空隙发生了变化 | |
| B. | 用明矾可以鉴别软水和硬水 | |
| C. | 水和过氧化氢的组成元素一样,所以化学性质也一样 | |
| D. | 硬水过滤后可软化为软水 |
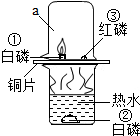 某老师在《燃烧的条件》教学中,改进了教材中的实验如图所示,在铜片上罩了仪器a,请回答:
某老师在《燃烧的条件》教学中,改进了教材中的实验如图所示,在铜片上罩了仪器a,请回答: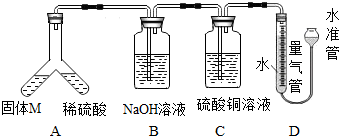 某课外兴趣小组为了探究铁与硫在隔绝空气的条件下反应所得固体M的成分,设计了如图所示装置.倾斜A使稀硫酸(足量)与固体M充分反应,待反应停止后,B装置增重,C装置中溶液无变化,反应后进入了量气管气体的体积为VmL.有上述实验事实可知:(提示:铁和硫生成硫化亚铁,硫化铜是一种不溶于酸也不溶于水的黑色固体)
某课外兴趣小组为了探究铁与硫在隔绝空气的条件下反应所得固体M的成分,设计了如图所示装置.倾斜A使稀硫酸(足量)与固体M充分反应,待反应停止后,B装置增重,C装置中溶液无变化,反应后进入了量气管气体的体积为VmL.有上述实验事实可知:(提示:铁和硫生成硫化亚铁,硫化铜是一种不溶于酸也不溶于水的黑色固体)