题目内容
8. 全球近140个国家将根据签署的《国际防治汞污染公约》,在2020年前禁止生产和出口含汞产品,如电池、荧光灯、化妆品、温度计、血压计等,关于汞元素的相关信息正确的是( )
全球近140个国家将根据签署的《国际防治汞污染公约》,在2020年前禁止生产和出口含汞产品,如电池、荧光灯、化妆品、温度计、血压计等,关于汞元素的相关信息正确的是( )| A. | 汞原子的中子数是80 | B. | 汞原子的质量为200.8g | ||
| C. | 汞的化学式为Hg | D. | 汞为非金属元素 |
分析 根据图中元素周期表可以获得的信息:左上角的数字表示原子序数;字母表示该元素的元素符号;中间的汉字表示元素名称;汉字下面的数字表示相对原子质量,进行分析判断即可.
解答 解:A.根据元素周期表中的一格可知,左上角的数字为80,表示原子序数为80;根据原子序数=核电荷数=质子数,则该元素的原子质子数为80,而不是中子数为80,故选项说法错误.
B.根据元素周期表中的一格可知,汉字下面的数字表示相对原子质量,元素的相对原子质量为200.6,相对原子质量单位是“1”,不是“克”,故选项说法错误.
C.根据元素周期表中的一格可知,字母表示该元素的元素符号,该元素的元素符号为Hg;汞属于金属单质,直接用元素符号表示其化学式,汞的化学式为Hg,故选项说法正确.
D.根据元素周期表中的一格可知,中间的汉字表示元素名称,该元素的名称是汞,属于金属元素,故选项说法错误.
故选:C.
点评 本题难度不大,考查学生灵活运用元素周期表中元素的信息(原子序数、元素符号、元素名称、相对原子质量)进行分析解题的能力.

练习册系列答案
相关题目
19.下列各组物质的名称、俗称、化学式完全对应的是( )
| A. | 汞、水银、Ag | B. | 氢氧化钠、纯碱、NaOH | ||
| C. | 酒精、甲醇、C2H5OH | D. | 碳酸氢钠、小苏打、NaHCO3 |
16.某化工厂排出澄清的废水,其中可能含有的离子是Ba2+、Fe3+、Fe2+、Ag+、Cu2+、SO42-、Cl-、NO3-.[已知:白色的Fe(OH)2沉淀在空气中会迅速转化为红褐色的Fe(OH)3.]
①取少量废水,加入过量稀盐酸,产生白色沉淀,过滤,将滤液分成两份,一份加入稀硫酸,产生白色沉淀;另一份加入过量NaOH溶液,产生蓝色沉淀.
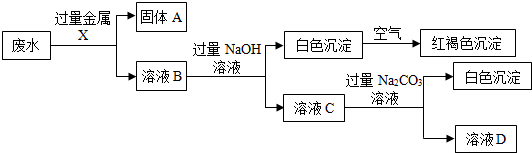
②某化学兴趣小组设计了一个处理该废水的实验方案,部分流程如图:
下列说法正确的是 (填字母).( )

①取少量废水,加入过量稀盐酸,产生白色沉淀,过滤,将滤液分成两份,一份加入稀硫酸,产生白色沉淀;另一份加入过量NaOH溶液,产生蓝色沉淀.
②某化学兴趣小组设计了一个处理该废水的实验方案,部分流程如图:
下列说法正确的是 (填字母).( )
| A. | 在①中,向一份滤液中加入过量NaOH溶液,其中与OH-反应的离子是H+、Cu2+ | |
| B. | 在②中,固体A中一定含有Ag和Cu,可能含有Fe | |
| C. | 在②中,溶液B的溶质有Ba(NO3)2、Fe(NO3)3 | |
| D. | 废水中含有Ba2+、Ag+、Cu2+、Fe2+、NO3- |
3.午饭的食谱中有①炒油菜 ②苹果 ③米饭 ④红烧肉 ⑤糖醋鱼,你认为比较合理的搭配是( )
| A. | ①②③ | B. | ①③⑤ | C. | ①④⑤ | D. | ③④⑤ |
13.根据你的化学知识和生活经验,判断下列说法正确的是( )
| A. | 分离液态空气制取氧气是因为分子可以再分 | |
| B. | 水烧开后易把壶盖冲起是因为温度升高分子会变大 | |
| C. | 用洗洁精洗涤餐具上的油污是因为洗洁精是高效的溶剂 | |
| D. | 铝制品有抗腐蚀性能是因为表面生成了致密氧化膜起保护作用 |
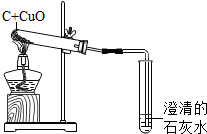 如图是碳和氧化铜在-定条件下进行反应的实验装置,该反应需几分钟时间.
如图是碳和氧化铜在-定条件下进行反应的实验装置,该反应需几分钟时间.
