23.(15分)A、B、C、D、E、F、G全为短周期元素,它们在中学常见化合物中显示的部分化合价及原子、离子半径从大到小的序号如下:(注:半径按①、②、③……的顺序依次减小)
|
元素 性质 |
A |
B |
C |
D |
E |
F |
G |
|
化合价 |
+1、+5、+7 |
只有+2 |
+4 |
-3、+2、+4、+5 |
只有-1 |
只有+3 |
只有+1 |
|
原子半径 |
⑤ |
② |
④ |
⑥ |
⑦ |
③ |
① |
|
离子半径 |
① |
⑤ |
无离子 |
② |
③ |
⑥ |
④ |
(1)用电子式表示BA2的形成过程 。
(2)写出F的最高价氧化物对应的水化物和G的最高价氧化物对应的水化物反应的离子方程式
。
(3)请设计实验比较B、F的活动性强弱。
|
元素 |
实验设计 |
现象 |
结论 |
|
B |
|
|
活动性:B F (填“>”、“<”或“=”) |
|
F |
23.(15分)下表是元素周期表的一部分(注意:以下各空所涉及的元素填元素符号,不能用字母代替)
|
族 周期 |
ⅠA |
ⅡA |
ⅢA |
IVA |
VA |
VIA |
VIIA |
0族 |
|
1 |
|
|
|
|
|
|
|
|
|
2 |
|
|
|
G |
H |
|
D |
|
|
3 |
B |
|
C |
|
|
|
E |
|
|
4 |
F |
A |
|
|
|
|
|
|
(1)用电子式表示AD2的形成过程 。
(2)写出C的最高价氧化物对应的水化物和E的最高价氧化物对应的水化物反应的离子方程式
。
(3)请设计实验比较B、F的金属性强弱顺序。
|
元素 |
实验设计 |
现象
|
结论 |
|
B |
|
|
金属性:B F (填“>”、“<”或“=”) |
|
F |
21.(6分)在一次学生实验中,学生用铝片分别和稀盐酸、稀硫酸反应,发现:铝片与稀盐酸反应现象非常明显,而和稀硫酸几乎不反应。这和教材中“铝能跟稀盐酸或稀硫酸反应生成氢气“的说法不一致。为排除因试剂变质等因素造成的影响,该学生在教师的指导下重新进行下列实验,验证是否存在上述现象。
实验用品:仪器(略,凡是实验需要的都有)
药品:3.0 mol·L-1盐酸、1.5 mol·L-1硫酸、3.0 mol·L-1硫酸,相同大小的铝片(纯度>99.5%)
实验过程:往三根相同的试管中分别加入相同的铝片各一片,再往试管中分别加入等体积的3.0 mol·L-1盐酸、1.5 mol·L-1硫酸、3.0 mol·L-1硫酸,观察反应进行到1、2、5、15、20分钟时的铝与酸反应的情况。结果如下:
|
反应进程(分钟) |
1 |
2 |
5 |
15 |
20 |
|
3.0mol/L盐酸 |
少量气泡 |
较多气泡 |
大量气泡 |
反应剧烈 |
铝片耗尽 |
|
1.5mol/L硫酸 |
均无明显现象(无气泡产生) |
||||
|
3.0mol/L硫酸 |
均无明显现象(无气泡产生) |
通过上述实验可知,无论是用1.5 mol·L-1硫酸还是3.0 mol·L-1硫酸,均无明显的现象,而
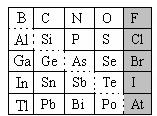 (12分)元素在周期表中的位置,反映了元素的原子结构和元素的性质。下图是元素周期表的一部分。
(12分)元素在周期表中的位置,反映了元素的原子结构和元素的性质。下图是元素周期表的一部分。 CaO (s) + CO2 (g) Δ H = +178.2
kJ·mol-1
CaO (s) + CO2 (g) Δ H = +178.2
kJ·mol-1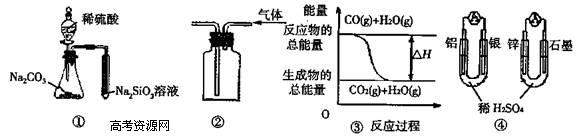
 C.图 ③ 表示可逆反应“CO(g)+H2O(g) CO2(g)+H2(g)”中的△H>0
C.图 ③ 表示可逆反应“CO(g)+H2O(g) CO2(g)+H2(g)”中的△H>0