网址:http://m.1010jiajiao.com/timu_id_922326[举报]
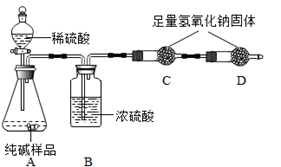
某品牌纯碱中含有少量氯化钠。某化学探究小组欲测定该品牌纯碱的纯度(即碳酸钠的质量分数)。(一)甲组同学设计如图所示实验:
【实验步骤】
①组装好如图仪器,并检查 ;
②称取13.0g样品放入锥形瓶中,加入少量蒸馏水溶解,并在其他装置中加入相应的药品;
③称量装置C的质量;
④打开分液漏斗旋塞滴入稀硫酸,直到不再产生气泡为止;
⑤再次称量装置C 的总质量;
⑥计算出样品中碳酸钠的质量分数。
【实验分析】
(1)A装置中反应的化学方程式为 。
(2)B装置的作用是 。
(3)如果没有B装置则所测样品中碳酸钠的质量分数 。(填偏大、偏小、不变)
(4)小明提出能否用盐酸代替硫酸?同学们经过讨论认为不能,理由是 。
(5)称得纯碱样品的质量为13.0g,实验前、后C装置(包含药品)的质量分别为61.2g和65.6g,则该纯碱样品的纯度为 %(精确到0.1%)。
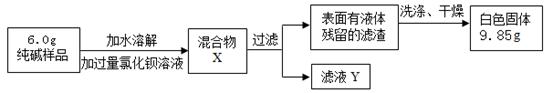
(二)乙组同学采用生成沉淀的方法来测定样品中纯碱的质量分数,设计了如下实验:
(1)判断加入氯化钡溶液是否过量的合适方法是 ,然后观察现象判断。
A.静置混合物X,向上层清液中继续滴加氯化钡溶液,若无白色沉淀生成,则氯化钡已经过量;
B.向混合物X中滴加稀硫酸,若有白色沉淀生成则说明氯化钡已经过量。
(2)判断滤渣是否洗涤干净,可以采取向最后的洗出液中滴加 ,然后观
察现象判断。
A.氯化钡溶液 B.稀硫酸 C.硝酸银溶液 D.稀盐酸
(3)根据实验数据,乙组测得样品中碳酸钠的质量分数为 %(精确到0.1%)。
【实验反思】
甲乙两组同学所测该品牌中碳酸钠的质量分数,你认为 组(填“甲”或“乙”)更准确,另一组存在较大偏差的原因可能是 。
【实验步骤】
①组装好如图仪器,并检查 ;
②称取13.0g样品放入锥形瓶中,加入少量蒸馏水溶解,并在其他装置中加入相应的药品;
③称量装置C的质量;
④打开分液漏斗旋塞滴入稀硫酸,直到不再产生气泡为止;
⑤再次称量装置C 的总质量;
⑥计算出样品中碳酸钠的质量分数。
【实验分析】
(1)A装置中反应的化学方程式为 。
(2)B装置的作用是 。
(3)如果没有B装置则所测样品中碳酸钠的质量分数 。(填偏大、偏小、不变)
(4)小明提出能否用盐酸代替硫酸?同学们经过讨论认为不能,理由是 。
(5)称得纯碱样品的质量为13.0g,实验前、后C装置(包含药品)的质量分别为61.2g和65.6g,则该纯碱样品的纯度为 %(精确到0.1%)。
(二)乙组同学采用生成沉淀的方法来测定样品中纯碱的质量分数,设计了如下实验:
(1)判断加入氯化钡溶液是否过量的合适方法是 ,然后观察现象判断。
A.静置混合物X,向上层清液中继续滴加氯化钡溶液,若无白色沉淀生成,则氯化钡已经过量;
B.向混合物X中滴加稀硫酸,若有白色沉淀生成则说明氯化钡已经过量。
(2)判断滤渣是否洗涤干净,可以采取向最后的洗出液中滴加 ,然后观
察现象判断。
A.氯化钡溶液 B.稀硫酸 C.硝酸银溶液 D.稀盐酸
(3)根据实验数据,乙组测得样品中碳酸钠的质量分数为 %(精确到0.1%)。
【实验反思】
甲乙两组同学所测该品牌中碳酸钠的质量分数,你认为 组(填“甲”或“乙”)更准确,另一组存在较大偏差的原因可能是 。
Ⅰ、甲组用下图装置通过测定气体质量再计算出纯碱的质量分数.
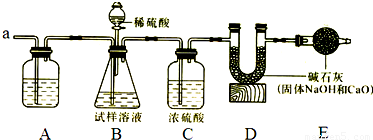
其主要步骤如下:
①按图组装仪器并检查气密性;
②称取m克试样放入锥形瓶中加适量蒸馏水使之完全溶解;
③称量装置D中装有碱石灰的U形管质量是a1克;
④从分液漏斗中慢慢滴加20%的稀硫酸
⑤从导管a中缓缓鼓入空气;
⑥再次称量装置D中装有碱石灰的U形管质量;
⑦重复⑤和⑥的操作,直到装置D中U形管质量基本不变,测得质量为a2克.
试回答相关问题:
(1)A装置中最好装______溶液,作用是______;
(2)装置C中浓硫酸的作用是______;
(3)步骤④中,从分液漏斗中慢慢滴加20%的稀硫酸直至观察到______为止,写出该反应的化学方程式______;
(4)若没有步骤⑤会使测定结果______(偏大或偏小);
(5)E装置中碱石灰的作用是______;
(6)装置B中分液漏斗内的稀硫酸不能换成浓盐酸的理由是______.
Ⅱ、乙组用生成沉淀的方法来测定纯碱(Na2CO3)的质量分数,称取12.5克样品加入107.2克的氯化钡溶液恰好完全反应过滤得到的沉淀干燥后为19.7克和一定量滤液(设没有损失),试计算①样品中纯碱的质量分数;②滤液中溶质的质量分数.
查看习题详情和答案>>