摘要:(1)40℃时.甲的溶解度 乙的溶解度.(2)80℃时.甲的饱和溶液的溶质质量分数为 .(3)当温度为 ℃时.甲.乙两种物质能形成溶质质量分数相同的饱和溶液.
网址:http://m.1010jiajiao.com/timu_id_919985[举报]
溶解度的相对大小是判断物质溶解性的依据,请回答:
(1)氯化铵在不同温度时的溶解度数据如表:
①氯化铵在0℃时的溶解度是
②50℃时氯化铵饱和溶液中溶质的质量分数约为
(2)在10℃时把等质量的固体甲和乙分别放入100g水中,溶解现象如图1,要使剩余的固体继续溶解可采用的方法是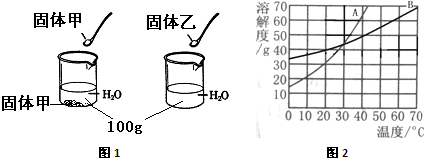
查看习题详情和答案>>
| 温度/℃ | 溶解度/g |
| 0 | 29.4 |
| 10 | 33.3 |
| 30 | 41.4 |
| 40 | 45.8 |
| 50 | 50.0 |
| 60 | 55.2 |
| 70 | 60.2 |
| 80 | 65.6 |
| 100 | 77.3 |
①氯化铵在0℃时的溶解度是
29.4g
29.4g
g.②50℃时氯化铵饱和溶液中溶质的质量分数约为
33.3%
33.3%
.(计算精确到0.1%)(2)在10℃时把等质量的固体甲和乙分别放入100g水中,溶解现象如图1,要使剩余的固体继续溶解可采用的方法是
升温
升温
(只需写出一种).图1中A、B表示上述两种物质的溶解度曲线.观察可知,在30
30
℃时,这两种物质的溶解度相等,且A表示的是甲
甲
物质(填“甲”或“乙”)的溶解度曲线.
 溶解度可表示物质溶解性的大小.
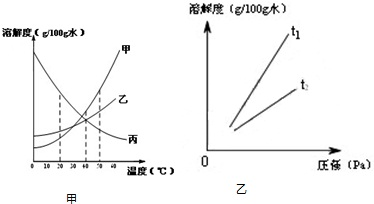
溶解度可表示物质溶解性的大小.①如图甲是甲、乙、丙三种固体物质(均不含结晶水)的溶解度曲线.
Ⅰ.20℃时,甲的溶解度
<
<
(填“>”、“<”或“=”)乙的溶解度.Ⅱ.20℃时,烧杯中分别盛有相同质量甲、乙、丙的饱和溶液,各加入等质量的对应固体,并升温至50℃.请填写下表.
| 烧杯中的溶质 | 烧杯中固体的变化 |
| 甲 | 固体逐渐减少,至全部溶解 固体逐渐减少,至全部溶解 |
| 乙 | 固体逐渐减少至全部溶解 |
| 丙 | 固体逐渐增加 固体逐渐增加 |
Ⅰ.打开可乐瓶,逸出大量气泡.由此可见,压强越小,CO2的溶解度越
小
小
.为增大CO2的溶解度,可采用的一种方法是加大压强
加大压强
.Ⅱ.不同温度下,氧气的溶解度随压强的变化如图乙所示,图中t1对应的温度为40℃,则t2对应的温度
a
a
(填编号).a.大于40℃b.小于40℃c.无法确定.
 40℃时,分别向盛有10g水的两支试管中,加入等质量的甲、乙两种固体物质充分溶解,刚好得到甲物质的饱和溶液.
40℃时,分别向盛有10g水的两支试管中,加入等质量的甲、乙两种固体物质充分溶解,刚好得到甲物质的饱和溶液.
(1)图B中可表示甲物质溶解度曲线的是________(填“a”或“b”).
(2)向烧杯中加入固体硝酸铵后,甲试管内的现象是________.
(3)向烧杯中加入固体烧碱后,乙试管内溶液的溶质质量分数________(填“增大”、“减小”或“不变”).
查看习题详情和答案>>
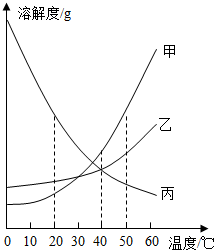 溶解度可表示物质溶解性的大小.如图是甲、乙、丙三种固体物质(均不含结晶水)的溶解度曲线.
溶解度可表示物质溶解性的大小.如图是甲、乙、丙三种固体物质(均不含结晶水)的溶解度曲线.
(1)50℃时,甲的溶解度______乙的溶解度(填“>”、“<”或“=”).
(2)40℃时,乙和丙______形成溶质质量分数相同的饱和溶液(填“能”或“不能”).
(3)20℃时,烧杯中分别盛有相同质量甲、乙、丙的饱和溶液,各加入等质量的对应固体,并升温至50℃.请填写下表
| 烧杯中的溶质 | 烧杯中固体的变化 |
| 甲 | ______ |
| 乙 | 固体逐渐减少至全部溶解 |
| 丙 | ______ |
A.溶剂的质量一定变小 B.溶质的质量可能不变
C.溶质的质量分数一定变大 D.溶液的质量一定变大
E.该饱和溶液还可以溶解其它物质
(5)通常情况下,在实验室用固体甲配制一定溶质质量分数的甲溶液,需用到的仪器有:托盘天平(带砝码盒)、烧杯和______.
A.酒精灯 B.药匙 C.玻璃棒 D.漏斗 E.铁架台 F.量筒 G.胶头滴管. 查看习题详情和答案>>
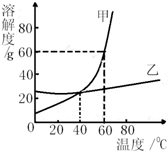 溶解度曲线为我们定量描述物质的溶解性强弱提供了便利.请你根据右图的溶解度曲线回答下列问题:
溶解度曲线为我们定量描述物质的溶解性强弱提供了便利.请你根据右图的溶解度曲线回答下列问题: