摘要:24.实验室里有一袋粗盐.含有较多的氯化钙和其它不可溶杂质.小华想知道其中氯化钠的质量分数是多少.于是按下面的步骤进行实验.请你帮他补充完全.①称量.②溶解.③向溶液中加入过量 试剂.过滤.④沉淀洗涤后小心烘干.得到固体A.⑤向滤液中滴加适量的稀盐酸后.进行 操作.即可得到纯净的固体B.⑥称量实验中得到的某种固体质量.回答问题:(1)在②③⑤步骤中.都使用到一种仪器是 它在步骤②和⑤中操作方法相同.但目的不同.其目的分别是② ⑤ (2)步骤⑤中加入稀盐酸的目的 (3)步骤⑥中.你认为需要称量固体A还是固体B的质量 你不选择称量另一种固体的理由
网址:http://m.1010jiajiao.com/timu_id_918644[举报]
氯化钠既是重要的调味品,又是重要的工业原料.
①实验室里有一小袋粗盐,其中含有较多的可溶性杂质(MgCl2、CaCl2等)和泥沙等不溶性杂质,要初步提纯这袋粗盐需要经过的步骤是溶解、过滤和 .若要计算提纯后所得精盐的产率.必须用的仪器是 .
②工业上用给饱和食盐水通电的方法可制得一种碱R和氢气、氯气,化学方程式为:
2NaCl+2H2O
2R+H2↑+Cl2↑,其中R的化学式为 ,若反应中消耗了58.5g氯化钠,则理论上可得到R的质量为 g.
查看习题详情和答案>>
①实验室里有一小袋粗盐,其中含有较多的可溶性杂质(MgCl2、CaCl2等)和泥沙等不溶性杂质,要初步提纯这袋粗盐需要经过的步骤是溶解、过滤和
②工业上用给饱和食盐水通电的方法可制得一种碱R和氢气、氯气,化学方程式为:
2NaCl+2H2O
| ||
氯化钠既是重要的调味品,又是重要的工业原料.
①实验室里有一小袋粗盐,其中含有较多的可溶性杂质(MgCl2、CaCl2等)和泥沙等不溶性杂质,要初步提纯这袋粗盐需要经过的步骤是溶解、过滤和______.若要计算提纯后所得精盐的产率.必须用的仪器是______.
②工业上用给饱和食盐水通电的方法可制得一种碱R和氢气、氯气,化学方程式为:
2NaCl+2H2O
2R+H2↑+Cl2↑,其中R的化学式为______,若反应中消耗了58.5g氯化钠,则理论上可得到R的质量为______g.
查看习题详情和答案>>
①实验室里有一小袋粗盐,其中含有较多的可溶性杂质(MgCl2、CaCl2等)和泥沙等不溶性杂质,要初步提纯这袋粗盐需要经过的步骤是溶解、过滤和______.若要计算提纯后所得精盐的产率.必须用的仪器是______.
②工业上用给饱和食盐水通电的方法可制得一种碱R和氢气、氯气,化学方程式为:
2NaCl+2H2O
| ||
氯化钠既是重要的调味品,又是重要的工业原料.
①实验室里有一小袋粗盐,其中含有较多的可溶性杂质(MgCl2、CaCl2等)和泥沙等不溶性杂质,要初步提纯这袋粗盐需要经过的步骤是溶解、过滤和______.若要计算提纯后所得精盐的产率.必须用的仪器是______.
②工业上用给饱和食盐水通电的方法可制得一种碱R和氢气、氯气,化学方程式为:
2NaCl+2H2O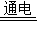 2R+H2↑+Cl2↑,其中R的化学式为______,若反应中消耗了58.5g氯化钠,则理论上可得到R的质量为______g.
2R+H2↑+Cl2↑,其中R的化学式为______,若反应中消耗了58.5g氯化钠,则理论上可得到R的质量为______g.
查看习题详情和答案>>
①实验室里有一小袋粗盐,其中含有较多的可溶性杂质(MgCl2、CaCl2等)和泥沙等不溶性杂质,要初步提纯这袋粗盐需要经过的步骤是溶解、过滤和______.若要计算提纯后所得精盐的产率.必须用的仪器是______.
②工业上用给饱和食盐水通电的方法可制得一种碱R和氢气、氯气,化学方程式为:
2NaCl+2H2O
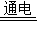 2R+H2↑+Cl2↑,其中R的化学式为______,若反应中消耗了58.5g氯化钠,则理论上可得到R的质量为______g.
2R+H2↑+Cl2↑,其中R的化学式为______,若反应中消耗了58.5g氯化钠,则理论上可得到R的质量为______g.查看习题详情和答案>>
 2R+H2↑+Cl2↑,其中R的化学式为________,若反应中消耗了58.5g氯化钠,则理论上可得到R的质量为________g.
2R+H2↑+Cl2↑,其中R的化学式为________,若反应中消耗了58.5g氯化钠,则理论上可得到R的质量为________g. 2R+H2↑+Cl2↑,其中R的化学式为__________,若反应中消耗了58.5g氯化钠,则理论上可得到R的质量为___g。
2R+H2↑+Cl2↑,其中R的化学式为__________,若反应中消耗了58.5g氯化钠,则理论上可得到R的质量为___g。