摘要:18.利用下图1装置能制取氧气并测定所收集气体的体积.
网址:http://m.1010jiajiao.com/timu_id_911680[举报]
 某化工厂为综合利用生产过程中的副产品CaSO4,与相邻的化肥厂联合设计了制备(NH4)2SO4的工艺流程.
某化工厂为综合利用生产过程中的副产品CaSO4,与相邻的化肥厂联合设计了制备(NH4)2SO4的工艺流程.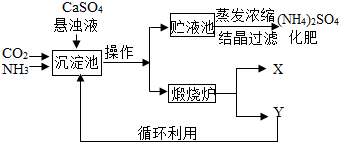
(1)操作a的名称是
(2)经操作a后得到的白色固体M在高温中分解生成X和Y两种物质,X常常被用做食品干燥剂.该工艺中,Y被作为原料之一循环利用.Y的化学式为
(3)沉淀池中发生的主要化学反应为:
(4)沉淀池中也可能生成少量NH4HCO3.为了判断(NH4)2SO4化肥中有无NH4HCO3:取少量试样溶于水,滴加足量的
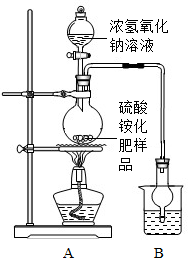
(5)为测定硫酸铵化肥的纯度(已确定该化肥中不存在NH4HCO3杂质),工厂的技术人员设计了右图所示装置进行实验.已知氨气极易溶于水,其水溶液为氨水.氨水呈碱性,不稳定,易挥发.实验过程中,技术人员往烧瓶中加入足量浓氢氧化钠溶液,并加热使硫酸铵充分反应完全转化为NH3.通过测出氨气的质量,然后算出化肥中硫酸铵的纯度.烧杯中的试剂是为了吸收产生的氨气,下列最适宜的试剂是
烧杯中干燥管的作用是
 某化工厂为综合利用生产过程中的副产品CaSO4,与相邻的化肥厂联合设计了制备(NH4)2SO4的工艺流程.
某化工厂为综合利用生产过程中的副产品CaSO4,与相邻的化肥厂联合设计了制备(NH4)2SO4的工艺流程.

(1)操作a的名称是______,若在实验室进行此操作,用到的玻璃仪器除玻璃棒、烧杯外,还需要______.
(2)经操作a后得到的白色固体M在高温中分解生成X和Y两种物质,X常常被用做食品干燥剂.该工艺中,Y被作为原料之一循环利用.Y的化学式为______.
(3)沉淀池中发生的主要化学反应为:______.
(4)沉淀池中也可能生成少量NH4HCO3.为了判断(NH4)2SO4化肥中有无NH4HCO3:取少量试样溶于水,滴加足量的______,无气泡产生,则可判断该化肥中不存在NH4HCO3.
(5)为测定硫酸铵化肥的纯度(已确定该化肥中不存在NH4HCO3杂质),工厂的技术人员设计了右图所示装置进行实验.已知氨气极易溶于水,其水溶液为氨水.氨水呈碱性,不稳定,易挥发.实验过程中,技术人员往烧瓶中加入足量浓氢氧化钠溶液,并加热使硫酸铵充分反应完全转化为NH3.通过测出氨气的质量,然后算出化肥中硫酸铵的纯度.烧杯中的试剂是为了吸收产生的氨气,下列最适宜的试剂是______(填序号):①水 ②浓HCl ③稀H2SO4 ④NaOH溶液
烧杯中干燥管的作用是______.
查看习题详情和答案>>
某化工厂为综合利用生产过程中的副产品CaSO4,与相邻的化肥厂联合设计了制备(NH4)2SO4的工艺流程.

(1)操作a的名称是______,若在实验室进行此操作,用到的玻璃仪器除玻璃棒、烧杯外,还需要______.
(2)经操作a后得到的白色固体M在高温中分解生成X和Y两种物质,X常常被用做食品干燥剂.该工艺中,Y被作为原料之一循环利用.Y的化学式为______.
(3)沉淀池中发生的主要化学反应为:______.
(4)沉淀池中也可能生成少量NH4HCO3.为了判断(NH4)2SO4化肥中有无NH4HCO3:取少量试样溶于水,滴加足量的______,无气泡产生,则可判断该化肥中不存在NH4HCO3.
(5)为测定硫酸铵化肥的纯度(已确定该化肥中不存在NH4HCO3杂质),工厂的技术人员设计了右图所示装置进行实验.已知氨气极易溶于水,其水溶液为氨水.氨水呈碱性,不稳定,易挥发.实验过程中,技术人员往烧瓶中加入足量浓氢氧化钠溶液,并加热使硫酸铵充分反应完全转化为NH3.通过测出氨气的质量,然后算出化肥中硫酸铵的纯度.烧杯中的试剂是为了吸收产生的氨气,下列最适宜的试剂是______(填序号):①水 ②浓HCl ③稀H2SO4 ④NaOH溶液
烧杯中干燥管的作用是______.
 查看习题详情和答案>>
查看习题详情和答案>>

(1)操作a的名称是______,若在实验室进行此操作,用到的玻璃仪器除玻璃棒、烧杯外,还需要______.
(2)经操作a后得到的白色固体M在高温中分解生成X和Y两种物质,X常常被用做食品干燥剂.该工艺中,Y被作为原料之一循环利用.Y的化学式为______.
(3)沉淀池中发生的主要化学反应为:______.
(4)沉淀池中也可能生成少量NH4HCO3.为了判断(NH4)2SO4化肥中有无NH4HCO3:取少量试样溶于水,滴加足量的______,无气泡产生,则可判断该化肥中不存在NH4HCO3.
(5)为测定硫酸铵化肥的纯度(已确定该化肥中不存在NH4HCO3杂质),工厂的技术人员设计了右图所示装置进行实验.已知氨气极易溶于水,其水溶液为氨水.氨水呈碱性,不稳定,易挥发.实验过程中,技术人员往烧瓶中加入足量浓氢氧化钠溶液,并加热使硫酸铵充分反应完全转化为NH3.通过测出氨气的质量,然后算出化肥中硫酸铵的纯度.烧杯中的试剂是为了吸收产生的氨气,下列最适宜的试剂是______(填序号):①水 ②浓HCl ③稀H2SO4 ④NaOH溶液
烧杯中干燥管的作用是______.
 查看习题详情和答案>>
查看习题详情和答案>>
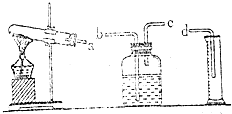 某校化学兴趣小组利用如图所示装置制取并收集一定体积的氧气.
某校化学兴趣小组利用如图所示装置制取并收集一定体积的氧气.(1)写出实验室用氯酸钾制备氧气的化学方程式
2KClO3
2KCl+3O2↑
| ||
| △ |
2KClO3
2KCl+3O2↑
;
| ||
| △ |
(2)利用上述装置收集的气体应具备的性质是
难溶于水
难溶于水
,根据量筒中液体的体积
量筒中液体的体积
可确定收集的气体的体积.(3)为达到实验目的,各装置的正确连接顺序是(填接口字母):a→
c
c
→b
b
→d(4)实验过程中发现B瓶中的水变红了的原因是
试管口没有放一团棉花,高锰酸钾粉末进入瓶中
试管口没有放一团棉花,高锰酸钾粉末进入瓶中
用收集的氧气做细铁丝燃烧的实验时,发现瓶底炸裂了,发生失误的原因可能是
瓶底未放少量水或沙子
瓶底未放少量水或沙子
(5)根据化学方程式理论上2克高锰酸钾完全分解可生成氧气0.203克.而实际测得氧气在标准状况下的体积为177毫升,换算成质量为0.253克超出理论值0.05克.从理论上推测,你认为超过理论量的氧气可能的来源物质是
K2MnO4、MnO2
K2MnO4、MnO2
(提示:空气、水因素不计).
某校化学兴趣小组利用如图所示装置制取并收集一定体积的氧气.
(1)写出实验室用氯酸钾制备氧气的化学方程式 ;
(2)利用上述装置收集的气体应具备的性质是 ,根据 可确定收集的气体的体积.
(3)为达到实验目的,各装置的正确连接顺序是(填接口字母):a→ → →d
(4)实验过程中发现B瓶中的水变红了的原因是
用收集的氧气做细铁丝燃烧的实验时,发现瓶底炸裂了,发生失误的原因可能是
(5)根据化学方程式理论上2克高锰酸钾完全分解可生成氧气0.203克.而实际测得氧气在标准状况下的体积为177毫升,换算成质量为0.253克超出理论值0.05克.从理论上推测,你认为超过理论量的氧气可能的来源物质是 (提示:空气、水因素不计).
 查看习题详情和答案>>
查看习题详情和答案>>
(1)写出实验室用氯酸钾制备氧气的化学方程式 ;
(2)利用上述装置收集的气体应具备的性质是 ,根据 可确定收集的气体的体积.
(3)为达到实验目的,各装置的正确连接顺序是(填接口字母):a→ → →d
(4)实验过程中发现B瓶中的水变红了的原因是
用收集的氧气做细铁丝燃烧的实验时,发现瓶底炸裂了,发生失误的原因可能是
(5)根据化学方程式理论上2克高锰酸钾完全分解可生成氧气0.203克.而实际测得氧气在标准状况下的体积为177毫升,换算成质量为0.253克超出理论值0.05克.从理论上推测,你认为超过理论量的氧气可能的来源物质是 (提示:空气、水因素不计).
 查看习题详情和答案>>
查看习题详情和答案>>