摘要:15.如图所示.将过氧化氢溶液滴到装有二氧化锰的广口瓶中.下列现象正确的是
网址:http://m.1010jiajiao.com/timu_id_906789[举报]
实验室用过氧化氢溶液(二氧化锰作催化剂)的反应来制取氧气,所用的装置如图所示:
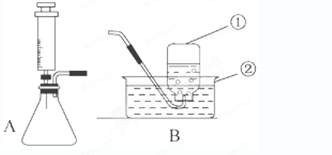
(1)带标号的仪器名称是①______,②______.
(2)注射器中应放入的物质是______,锥形瓶中应放入的物质是______.
(3)在制取氧气时,某同学观察到锥形瓶内开始产生大量气泡时,便立即用B装置收集氧气,收集满后,该同学用带火星的木条伸入该集气瓶的瓶口、瓶中、瓶底,均没有发现木条复燃,其原因是______,改进方法是______.
(4)实验中该同学发现装置A中反应太剧烈,他认为这是反应速度太快的原因,据此你认为在实验过程中的安全注意事项是(填序号)______.
①控制液体的滴加速度;②用体积较小的锥形瓶; ③加热反应物.
(5)反应后将锥形瓶内混合物分离的方法是______.
查看习题详情和答案>>

(1)带标号的仪器名称是①______,②______.
(2)注射器中应放入的物质是______,锥形瓶中应放入的物质是______.
(3)在制取氧气时,某同学观察到锥形瓶内开始产生大量气泡时,便立即用B装置收集氧气,收集满后,该同学用带火星的木条伸入该集气瓶的瓶口、瓶中、瓶底,均没有发现木条复燃,其原因是______,改进方法是______.
(4)实验中该同学发现装置A中反应太剧烈,他认为这是反应速度太快的原因,据此你认为在实验过程中的安全注意事项是(填序号)______.
①控制液体的滴加速度;②用体积较小的锥形瓶; ③加热反应物.
(5)反应后将锥形瓶内混合物分离的方法是______.
实验室用过氧化氢溶液(二氧化锰作催化剂)的反应来制取氧气,所用的装置如图所示: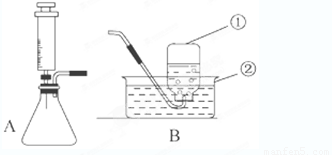
(1)带标号的仪器名称是①______,②______.
(2)注射器中应放入的物质是______,锥形瓶中应放入的物质是______.
(3)在制取氧气时,某同学观察到锥形瓶内开始产生大量气泡时,便立即用B装置收集氧气,收集满后,该同学用带火星的木条伸入该集气瓶的瓶口、瓶中、瓶底,均没有发现木条复燃,其原因是______,改进方法是______.
(4)实验中该同学发现装置A中反应太剧烈,他认为这是反应速度太快的原因,据此你认为在实验过程中的安全注意事项是(填序号)______.
①控制液体的滴加速度;②用体积较小的锥形瓶; ③加热反应物.
(5)反应后将锥形瓶内混合物分离的方法是______.
查看习题详情和答案>>

(1)带标号的仪器名称是①______,②______.
(2)注射器中应放入的物质是______,锥形瓶中应放入的物质是______.
(3)在制取氧气时,某同学观察到锥形瓶内开始产生大量气泡时,便立即用B装置收集氧气,收集满后,该同学用带火星的木条伸入该集气瓶的瓶口、瓶中、瓶底,均没有发现木条复燃,其原因是______,改进方法是______.
(4)实验中该同学发现装置A中反应太剧烈,他认为这是反应速度太快的原因,据此你认为在实验过程中的安全注意事项是(填序号)______.
①控制液体的滴加速度;②用体积较小的锥形瓶; ③加热反应物.
(5)反应后将锥形瓶内混合物分离的方法是______.
查看习题详情和答案>>
(2013?赤峰)二氧化碳与氢氧化钠溶液作用没有明显的现象,某同学设计了如右图所示的实验装置(A、B是气球).
(1)若该装置气密性良好,则将氢氧化钠溶液滴入锥形瓶中可观察到什么现象?试解释产生此现象的原因.
(2)氯气(C12)是一种有刺激性气味,有毒的气体,氯气可与水反应:C12+H2O=HCl+HClO(次氯酸).若将锥形瓶中的CO2气体换成氯气,也可产生上述现象.试写出氯气与氢氧化钠溶液发生反应的化学方程式
(3)若想使装置中产生的现象与(1)中的现象相反,则胶头滴管和锥形瓶中应分别装入什么药品(写出一组即可)
查看习题详情和答案>>

(1)若该装置气密性良好,则将氢氧化钠溶液滴入锥形瓶中可观察到什么现象?试解释产生此现象的原因.
(2)氯气(C12)是一种有刺激性气味,有毒的气体,氯气可与水反应:C12+H2O=HCl+HClO(次氯酸).若将锥形瓶中的CO2气体换成氯气,也可产生上述现象.试写出氯气与氢氧化钠溶液发生反应的化学方程式
C12+2NaOH=NaClO+NaCl+H2O
C12+2NaOH=NaClO+NaCl+H2O
.(3)若想使装置中产生的现象与(1)中的现象相反,则胶头滴管和锥形瓶中应分别装入什么药品(写出一组即可)
过氧化氢溶液和二氧化锰
过氧化氢溶液和二氧化锰
.为了研究外界条件对过氧化氢分解速率的影响,某同学做了以下实验,请回答
| 编号 | 操作 | 实验现象 |
| ① | 分别在试管A、B中加入5mL 5% H2O2溶液,各滴入2滴等浓度 FeCl3溶液.待试管中均有适量气泡出现时,将试管A放入盛有5℃左右冷水的烧杯中浸泡;将试管B放入盛有40℃左右热水的烧杯中浸泡. | 试管A中不再产生气泡;试管B中产生的气泡量增大. |
| ② | 另取两支试管分别加入5mL 5% H2O2溶液和5mL 10% H2O2溶液 | 试管A、B中均未明显见到有气泡产生. |
(2)实验①的目的是______.
实验中滴加FeCl3溶液的目的是______.
(3)实验②未观察到预期的实验现象,为了帮助该同学达到实验目的,你提出的对上述操作的改进意见是______(用实验中提供的试剂).
(4)某同学在50mL一定浓度的H2O2溶液中加入一定量的二氧化锰,放出气体的体积与反应时间的关系如图1所示,则A、B、C三点所表示的瞬时反应速率最慢的是______.
(5)催化剂是化学反应前后______ 均未改变的一类化学物质.
(6)对于H2O2分解反应,Cu2+也有一定的催化作用.为比较Fe3+和Cu2+对H2O2分解的催化效果,某化学研究小组的同学分别设计了如图甲、乙所示的实验.请回答相关问题:
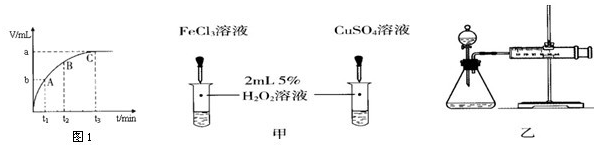
①定性分析:如图甲可通过观察______,定性比较得出结论.有同学提出将FeCl3改为______更为合理,其理由是______.
②定量分析:用图乙所示装置做对照实验,实验时均以生成40mL气体为准,其他可能影响实验的因素均已忽略.实验中需要测量的数据是______. 查看习题详情和答案>>
28、某实验小组欲用10克胆矾制取氧化铜并证明氧化铜能加快H2O2的分解.
Ⅰ.请你完成他们制取氧化铜的实验步骤.
(1)称取10克胆矾,将其放入小烧杯中,再
(2)向步骤(1)中的烧杯内滴加
(3)检验硫酸铜是否被作用完全,操作方法是
(4)将步骤(2)所得的混合物加热至沉淀全部变为黑色氧化铜.
(5)再将步骤(4)所得混合物过滤、洗涤、烘干后研细;验证是否洗净沉淀中硫酸根离子的方法是
Ⅱ.小明设计了如图实验装置来证明氧化铜能加快双氧水(浓度约7%)的分解并与二氧化锰的催化效果进行比较(即比较反应速率).用图示装置测量产生气体的体积,其它可能影响实验因素均已忽略,相关数据如下:
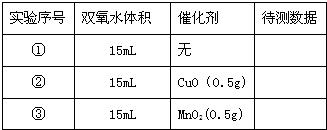
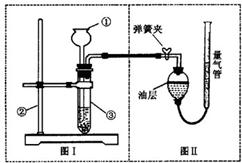
(1)从设计装置来看,有一个明显的缺陷,你认为如何纠正
(2)从设计原理看,实验中的“待测数据”可以是指
(3)实验时气体收集在图Ⅱ的球型漏斗中.若要保证读取的气体体积没有误差,在读数前应进行的操作是
(4)为探究CuO在实验②中是否起催化作用,除与①比较外,还需补做下列实验(不必写具体操作):a.证明CuO的化学性质没有改变;b.
Ⅲ.为证明氧化铜的化学性质在加入双氧水前后没有发生改变,你设计验证的实验是
查看习题详情和答案>>
Ⅰ.请你完成他们制取氧化铜的实验步骤.
(1)称取10克胆矾,将其放入小烧杯中,再
加适量的水使其全部溶解
.(2)向步骤(1)中的烧杯内滴加
氢氧化钠或氢氧化钾
溶液,直至产生大量的沉淀.(3)检验硫酸铜是否被作用完全,操作方法是
静置后,取上层清液少量于试管中,滴加氢氧化钠(或氢氧化钾)溶液,若没有蓝色沉淀生成,说明完全反应.
若有蓝色沉淀生成,说明没完全反应
.(4)将步骤(2)所得的混合物加热至沉淀全部变为黑色氧化铜.
(5)再将步骤(4)所得混合物过滤、洗涤、烘干后研细;验证是否洗净沉淀中硫酸根离子的方法是
取洗涤液少量于试管中,滴加氯化钡溶液,若有白色沉淀生成,说明洗涤液中含有硫酸根离子.若没有白色沉淀,说明没有硫酸根离
子
.Ⅱ.小明设计了如图实验装置来证明氧化铜能加快双氧水(浓度约7%)的分解并与二氧化锰的催化效果进行比较(即比较反应速率).用图示装置测量产生气体的体积,其它可能影响实验因素均已忽略,相关数据如下:


(1)从设计装置来看,有一个明显的缺陷,你认为如何纠正
把长颈漏斗改成分液漏斗
.(2)从设计原理看,实验中的“待测数据”可以是指
相同时间内收集到的氧气的体积数
.(3)实验时气体收集在图Ⅱ的球型漏斗中.若要保证读取的气体体积没有误差,在读数前应进行的操作是
上下移动量气管使球型漏斗液面与量气管液面相平
.若要检验产生的气体是氧气,应打开单孔橡皮塞,用带火星的木条放在球星漏斗口处,木条复燃,说明是氧气
.(4)为探究CuO在实验②中是否起催化作用,除与①比较外,还需补做下列实验(不必写具体操作):a.证明CuO的化学性质没有改变;b.
证明氧化铜的质量在反应前后没变
.Ⅲ.为证明氧化铜的化学性质在加入双氧水前后没有发生改变,你设计验证的实验是
取样品少量于试管中,滴加稀硫酸振荡,能完全溶解并且溶液变成蓝色,说明是氧化铜
.