摘要:18.下表是部分元素的原子结构示意图.主要化合价等信息第二周期
网址:http://m.1010jiajiao.com/timu_id_901016[举报]
下表是部分元素的原子结构示意图、主要化合价等信息:
(1)写出由铝元素与氯元素组成化合物的化学式 ;
(2)上表中各元素的最高正化合价与原子最外层电子数的关系是 (填“相等”或“不相等”).
(3)钠元素属于 (填“金属”或“非金属”),钠离子符号 ;氟原子在化学反应中易 电子(填“得”或“失”);原子的最外层电子数与元素的化学性质关系密切,在表中同一纵行的元素化学性质
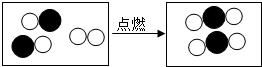
(4)如图形象地表示了某化学反应前后分子的变化.其中“ ”碳原子,“
”碳原子,“ ”表示氧原子,则该反应的化学方程式为: ;
”表示氧原子,则该反应的化学方程式为: ;
 查看习题详情和答案>>
查看习题详情和答案>>
| 第二周期 | 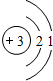 Li Li |
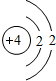 Be Be |
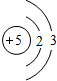 B B |
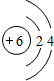 C C |
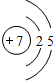 N N |
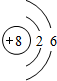 O O |
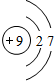 F F |
| 主要 化合价 |
+1 | +2 | +3 | +4,-4 | +5,-3 | -2 | -1 |
| 第三周期 |  Na Na |
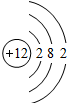 Mg Mg |
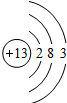 Al Al |
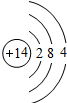 Si Si |
 P P |
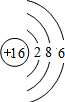 S S |
 Cl Cl |
| 主要 化合价 |
+1 | +2 | +3 | +4,-4 | +5,-3 | +6,-2 | +7,-1 |
(2)上表中各元素的最高正化合价与原子最外层电子数的关系是
(3)钠元素属于
(4)如图形象地表示了某化学反应前后分子的变化.其中“
 ”碳原子,“
”碳原子,“ ”表示氧原子,则该反应的化学方程式为:
”表示氧原子,则该反应的化学方程式为: 查看习题详情和答案>>
查看习题详情和答案>>
下表是部分元素的原子结构示意图、主要化合价等信息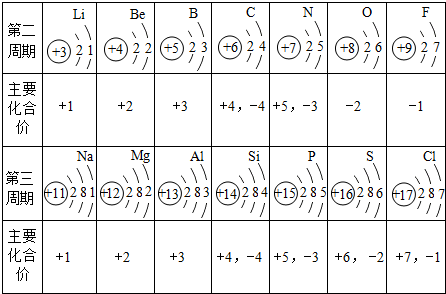
①表中不同种元素最本质的区别是 (填序号):
A.中子数不同;B.质子数不同;C.相对原子质量不同
②写出由原子序数为13和17的元素组成化合物的化学式 ;
③上表中各元素的最高正化合价与原子最外层电子数的关系是 (填“相等”或“不相等”).
④镁元素属于 (填“金属”或“非金属”),镁离子符号 ;氟原子在化学反应中易 电子(填“得”或“失”);原子的最外层电子数与元素的化学性质关系密切,在表中同一纵行的元素化学性质 ;
⑤右图形象地表示了某化学反应前后分子的变化.其中“ ”表示原子序数为8的原子,“
”表示原子序数为8的原子,“ ”表示原子序数为6的原子,则该反应的化学方程式为:
”表示原子序数为6的原子,则该反应的化学方程式为:
.
查看习题详情和答案>>

①表中不同种元素最本质的区别是
A.中子数不同;B.质子数不同;C.相对原子质量不同
②写出由原子序数为13和17的元素组成化合物的化学式
③上表中各元素的最高正化合价与原子最外层电子数的关系是
④镁元素属于

⑤右图形象地表示了某化学反应前后分子的变化.其中“
 ”表示原子序数为8的原子,“
”表示原子序数为8的原子,“ ”表示原子序数为6的原子,则该反应的化学方程式为:
”表示原子序数为6的原子,则该反应的化学方程式为:下表是部分元素的原子结构示意图、主要化合价等信息.

(1)硫元素原子的最外层电子数是
(2)核电荷数为14的元素名称是
(3)氟元素的原子在化学反应中一般较容易
(4)原子序数为11和17的元素组成化合物的化学式为
查看习题详情和答案>>

(1)硫元素原子的最外层电子数是
6
6
.(2)核电荷数为14的元素名称是
硅
硅
.(3)氟元素的原子在化学反应中一般较容易
得到
得到
电子(填“得到”或“失去”).(4)原子序数为11和17的元素组成化合物的化学式为
NaCl
NaCl
.下表是部分元素的原子结构示意图、主要化合价等信息.
请完成以下填空:
(1)地壳中含量最多的金属元素是
(2)硅原子的核外电子数为
(3)Na、Mg两种原子属于不同种元素的原子,其根本原因是
(4)若用M、R分别表示两种元素,根据上表写出微粒构型为MR3型的物质的化学式
(5)根据上表请你总结原子结构与元素化合价或周期数的关系
查看习题详情和答案>>
| 第三周期 | Na |
Mg |
Al |
Si |
P |
S |
Cl |
| 主要化合价 | +1 | +2 | +3 | +4,-4 | +5,-3 | +6,-2 | +7,-1 |
(1)地壳中含量最多的金属元素是
Al
Al
(写元素符号);(2)硅原子的核外电子数为
14
14
;(3)Na、Mg两种原子属于不同种元素的原子,其根本原因是
质子数不同
质子数不同
;(4)若用M、R分别表示两种元素,根据上表写出微粒构型为MR3型的物质的化学式
AlCl3
AlCl3
;(5)根据上表请你总结原子结构与元素化合价或周期数的关系
周期数=电子层数(合理均可)
周期数=电子层数(合理均可)
(任写一条).