摘要:17.下列说法中正确的是A.实验室收集密度比空气小的气体只能用向下排空气法B.向溶液中滴加BaCl2溶液有白色沉淀生成.但这不能确定该溶液中肯定含有SO42-C.硫酸铜可配制杀菌剂.所以可以用硫酸铜给饮用水杀菌消毒D.根据质量守恒定律.8 g氧气跟5 g碳起反应能生成13 g二氧化碳
网址:http://m.1010jiajiao.com/timu_id_900767[举报]
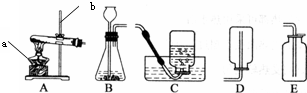 实验室常用下列装置来制取氧气:
实验室常用下列装置来制取氧气:(1)写出图中有标号仪器的名称:a
酒精灯
酒精灯
、b铁架台
铁架台
;(2)用高锰酸钾制取氧气时,可选用的发生装置是
A
A
(填序号),如何将高锰酸钾装入容器内:将试管平放,用纸槽将高锰酸钾粉末送入试管底部
将试管平放,用纸槽将高锰酸钾粉末送入试管底部
发生反应的文字表达式为高锰酸钾
锰酸钾+二氧化锰+氧气
| 加热 |
高锰酸钾
锰酸钾+二氧化锰+氧气
.| 加热 |
(3)若用E装置收集氧气则依据是
氧气的密度略大于空气
氧气的密度略大于空气
,检验氧气是否集满的方法是将带火星的木条伸入集气瓶口
将带火星的木条伸入集气瓶口
.
(4)若用排水法收集氧气,下面是制取氧气的实验步骤:①加热;②收集气体;③检查装置的气密性;④装入高锰酸钾;⑤将试管固定在铁架台上;⑥熄灭酒精灯; ⑦将导管移出水面.正确的顺序为
③④⑤①②⑦⑥
③④⑤①②⑦⑥
.(5)分析实验过程中出现以下情况的可能原因:
①水槽中的水呈紫色
试管口处未加一团棉花
试管口处未加一团棉花
.②加热的过程中,试管破裂
试管口未向下倾斜
试管口未向下倾斜
.③收集氧气结束时,水沿导管进入试管
先熄灭酒精灯,后撤导气管
先熄灭酒精灯,后撤导气管
.④用排水法收集到的氧气不纯
有气泡冒出就马上收集
有气泡冒出就马上收集
.(6)用双氧水和二氧化锰来制取氧气的文字表达式为
过氧化氢
水+氧气
| 二氧化锰 |
过氧化氢
水+氧气
| 二氧化锰 |
,可选用的发生装置是
B
B
(填序号),其中二氧化锰起催化
催化
作用;如何检查该装置的气密性:用弹簧夹夹住右边导管,向长颈漏斗中倒水,液面高度不变,说明装置气密性良好
用弹簧夹夹住右边导管,向长颈漏斗中倒水,液面高度不变,说明装置气密性良好
.(7)实验室用无水醋酸钠固体和固体碱石灰加热制取甲烷气体.甲烷的密度比空气小,不溶于水.选用
A
A
(填序号)发生装置制取甲烷,收集气体时可选用C
C
或D
D
(填序号).(8)实验室用FeS固体和稀硫酸在常温下可以制取H2S气体,该气体易溶于水,密度比空气大,应选用
B
B
(填序号)发生装置制取H2S,收集气体可以用E
E
(填序号)(8)研究性学习小组选择“双氧水生成氧气的快慢与什么因素有关”的课题进行探究,以下是他们探究的主要过程:
假 设:双氧水生成氧气的快慢与催化剂种类有关
实验方案:常温下,在两瓶同质量、同浓度的双氧水,分别加入相同质量的二氧化锰和红砖粉末,测量各生成一瓶(相同体积)氧气所需的时间.
此实验中宜采用的气体收集方法是
排水法
排水法
.实验记录:
| 实验编号 | 1 | 2 |
| 反应物 | 5%双氧水 | 5%双氧水 |
| 催化剂 | 1g红砖粉末 | 1g二氧化锰 |
| 时间 | 165秒 | 46秒 |
相同条件下H2O2生成O2的快慢与催化剂的种类有关.
相同条件下H2O2生成O2的快慢与催化剂的种类有关.
.反 思:双氧水在常温下分解缓慢,加入二氧化锰或红砖粉末后反应明显加快,若要证明二氧化锰和水泥块是该反应的催化剂,还需要增加实验来验证它们在化学反应前后的
质量
质量
、化学性质
化学性质
,是否改变.双氧水生成氧气的快慢还与什么因素有关?请你帮助他们继续探究.(只要求提出一种影响双氧水生成氧气的快慢的因素以及相关假设)
假 设:
H2O2生成O2的快慢与H2O2的质量分数有关.
H2O2生成O2的快慢与H2O2的质量分数有关.
.实验室制下列三种气体
A.O2:2KClO3
2KCl+3O2↑
B.CO2:
C.Cl2:MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O
说明:Cl2是一种黄绿色、有刺激性气味、密度比空气大、能溶于水的气体.
(1)写出制CO2的反应方程式.
(2)有下列三种制气装置(如图甲)和两种集气装置(如图乙)
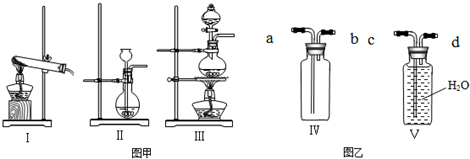
①制取CO2应选取的装置是 ,应选用Ⅲ装置制取的气体是 ;
②用Ⅳ装置收集Cl2应从 口进气,上述三种气体中,能用Ⅴ装置收集的气体有 ,应从 口进气.
(3)A中制O2后,从剩余固体中分离出MnO2的操作有 (不需烘干),所用到的玻璃仪器有 .
(4)用100g 36.5%的浓盐酸与足量MnO2混合加热,理论上能制得Cl2的质量为 g,而实际收集到的Cl2质量远远小于这个数值,若操作正确,装置不漏气,则可能的原因有(至少两点)
(5)将8g KClO3与1g MnO2混合加热制O2,充分反应后冷却,称得试管内剩余固体质量为4.2g,
①请用两种方法求生成KCl的质量
②计算结果表明,题目数据有问题,要使该题数据合理,可将KClO3质量由8g改为a g,则a的取值范围是 .
查看习题详情和答案>>
A.O2:2KClO3
| ||
B.CO2:
C.Cl2:MnO2+4HCl(浓)
| ||
说明:Cl2是一种黄绿色、有刺激性气味、密度比空气大、能溶于水的气体.
(1)写出制CO2的反应方程式.
(2)有下列三种制气装置(如图甲)和两种集气装置(如图乙)

①制取CO2应选取的装置是
②用Ⅳ装置收集Cl2应从
(3)A中制O2后,从剩余固体中分离出MnO2的操作有
(4)用100g 36.5%的浓盐酸与足量MnO2混合加热,理论上能制得Cl2的质量为
(5)将8g KClO3与1g MnO2混合加热制O2,充分反应后冷却,称得试管内剩余固体质量为4.2g,
①请用两种方法求生成KCl的质量
②计算结果表明,题目数据有问题,要使该题数据合理,可将KClO3质量由8g改为a g,则a的取值范围是