题目内容
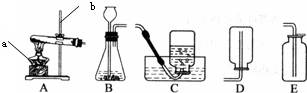 实验室常用下列装置来制取氧气:
实验室常用下列装置来制取氧气:(1)写出图中有标号仪器的名称:a
酒精灯
酒精灯
、b铁架台
铁架台
;(2)用高锰酸钾制取氧气时,可选用的发生装置是
A
A
(填序号),如何将高锰酸钾装入容器内:将试管平放,用纸槽将高锰酸钾粉末送入试管底部
将试管平放,用纸槽将高锰酸钾粉末送入试管底部
发生反应的文字表达式为高锰酸钾
锰酸钾+二氧化锰+氧气
| 加热 |
高锰酸钾
锰酸钾+二氧化锰+氧气
.| 加热 |
(3)若用E装置收集氧气则依据是
氧气的密度略大于空气
氧气的密度略大于空气
,检验氧气是否集满的方法是将带火星的木条伸入集气瓶口
将带火星的木条伸入集气瓶口
.
(4)若用排水法收集氧气,下面是制取氧气的实验步骤:①加热;②收集气体;③检查装置的气密性;④装入高锰酸钾;⑤将试管固定在铁架台上;⑥熄灭酒精灯; ⑦将导管移出水面.正确的顺序为
③④⑤①②⑦⑥
③④⑤①②⑦⑥
.(5)分析实验过程中出现以下情况的可能原因:
①水槽中的水呈紫色
试管口处未加一团棉花
试管口处未加一团棉花
.②加热的过程中,试管破裂
试管口未向下倾斜
试管口未向下倾斜
.③收集氧气结束时,水沿导管进入试管
先熄灭酒精灯,后撤导气管
先熄灭酒精灯,后撤导气管
.④用排水法收集到的氧气不纯
有气泡冒出就马上收集
有气泡冒出就马上收集
.(6)用双氧水和二氧化锰来制取氧气的文字表达式为
过氧化氢
水+氧气
| 二氧化锰 |
过氧化氢
水+氧气
| 二氧化锰 |
,可选用的发生装置是
B
B
(填序号),其中二氧化锰起催化
催化
作用;如何检查该装置的气密性:用弹簧夹夹住右边导管,向长颈漏斗中倒水,液面高度不变,说明装置气密性良好
用弹簧夹夹住右边导管,向长颈漏斗中倒水,液面高度不变,说明装置气密性良好
.(7)实验室用无水醋酸钠固体和固体碱石灰加热制取甲烷气体.甲烷的密度比空气小,不溶于水.选用
A
A
(填序号)发生装置制取甲烷,收集气体时可选用C
C
或D
D
(填序号).(8)实验室用FeS固体和稀硫酸在常温下可以制取H2S气体,该气体易溶于水,密度比空气大,应选用
B
B
(填序号)发生装置制取H2S,收集气体可以用E
E
(填序号)(8)研究性学习小组选择“双氧水生成氧气的快慢与什么因素有关”的课题进行探究,以下是他们探究的主要过程:
假 设:双氧水生成氧气的快慢与催化剂种类有关
实验方案:常温下,在两瓶同质量、同浓度的双氧水,分别加入相同质量的二氧化锰和红砖粉末,测量各生成一瓶(相同体积)氧气所需的时间.
此实验中宜采用的气体收集方法是
排水法
排水法
.实验记录:
| 实验编号 | 1 | 2 |
| 反应物 | 5%双氧水 | 5%双氧水 |
| 催化剂 | 1g红砖粉末 | 1g二氧化锰 |
| 时间 | 165秒 | 46秒 |
相同条件下H2O2生成O2的快慢与催化剂的种类有关.
相同条件下H2O2生成O2的快慢与催化剂的种类有关.
.反 思:双氧水在常温下分解缓慢,加入二氧化锰或红砖粉末后反应明显加快,若要证明二氧化锰和水泥块是该反应的催化剂,还需要增加实验来验证它们在化学反应前后的
质量
质量
、化学性质
化学性质
,是否改变.双氧水生成氧气的快慢还与什么因素有关?请你帮助他们继续探究.(只要求提出一种影响双氧水生成氧气的快慢的因素以及相关假设)
假 设:
H2O2生成O2的快慢与H2O2的质量分数有关.
H2O2生成O2的快慢与H2O2的质量分数有关.
.分析:(1)熟悉常见仪器的名称和用途.
(2)根据用高锰酸钾制取氧气的原理、装置及操作分析回答.
(3)根据E装置的特点分析氧气的性质,根据氧气的助燃性分析验满的方法.
(4)根据用高锰酸钾制取氧气的过程分析实验的步骤.
(5)根据实验制取氧气的注意事项分析.
(6)根据实验室用双氧水和二氧化锰来制取氧气的原理、装置、操作分析回答.
(7)根据实验室用无水醋酸钠固体和固体碱石灰加热制取甲烷气体的药品的状态及反应条件确定发生装置,根据甲烷的溶解性及密度确定收集装置.
(8)根据实验室用FeS固体和稀硫酸在常温下可以制取H2S气体的药品的状态及反应条件确定发生装置,根据H2S气体的溶解性及密度确定收集装置.
(9)可以根据制取气体的性质及实验的要求选择实验收集装置,根据催化剂的选择和作用可以设计合理的实验过程,根据表中提供的数据可以进行相关方面的判断.
(2)根据用高锰酸钾制取氧气的原理、装置及操作分析回答.
(3)根据E装置的特点分析氧气的性质,根据氧气的助燃性分析验满的方法.
(4)根据用高锰酸钾制取氧气的过程分析实验的步骤.
(5)根据实验制取氧气的注意事项分析.
(6)根据实验室用双氧水和二氧化锰来制取氧气的原理、装置、操作分析回答.
(7)根据实验室用无水醋酸钠固体和固体碱石灰加热制取甲烷气体的药品的状态及反应条件确定发生装置,根据甲烷的溶解性及密度确定收集装置.
(8)根据实验室用FeS固体和稀硫酸在常温下可以制取H2S气体的药品的状态及反应条件确定发生装置,根据H2S气体的溶解性及密度确定收集装置.
(9)可以根据制取气体的性质及实验的要求选择实验收集装置,根据催化剂的选择和作用可以设计合理的实验过程,根据表中提供的数据可以进行相关方面的判断.
解答:解:(1)图中有标号仪器的名称:a是酒精灯、b是 铁架台;
(2)用高锰酸钾制取氧气时,属于加热固体制取气体,可选用的发生装置是A,将高锰酸钾装入容器内的方法是:将试管平放,用纸槽将高锰酸钾粉末送入试管底部.发生反应的文字表达式为:高锰酸钾
锰酸钾+二氧化锰+氧气.
(3)若用E装置收集氧气,属于向上排空气集气法,则依据是:氧气的密度略大于空气.由于氧气有助燃性,所以检验氧气是否集满的方法是:将带火星的木条伸入集气瓶口.
(4)在实验室用用高锰酸钾制取氧气时,先要检查装置的气密性,装入高锰酸钾,在将试管固定在铁架台上,开始加热,收集气体实验完毕,先将导管移出水面后再熄灭酒精灯.所以正确的顺序为③④⑤①②⑦⑥.
(5)①水槽中的水呈紫色可能的原因是试管口处未加一团棉花,高锰酸钾粉末从导管进入水槽.
②加热的过程中,试管破裂的原因可能有:试管口未向上倾斜等.
③收集氧气结束时,水沿导管进入试管 的可能原因是:先熄灭酒精灯,后撤导气管.
④用排水法收集到的氧气不纯的原因可能是:有气泡冒出就马上收集等.
(6)用双氧水和二氧化锰来制取氧气的文字表达式为:过氧化氢
水+氧气,属于固液常温下反应制取气体,可选用的发生装置是B,其中二氧化锰起催化作用;检查该装置的气密性的方法是:用弹簧夹夹住右边导管,向长颈漏斗中倒水,液面高度不变,说明装置气密性良好.
(7)实验室用无水醋酸钠固体和固体碱石灰加热制取甲烷气体.属于加热固体制取气体.选用A发生装置制取甲烷,甲烷的密度比空气小,不溶于水收集气体时可选用C或D.
(8)实验室用FeS固体和稀硫酸在常温下可以制取H2S气体,属于固液常温下反应制取气体,应选用B发生装置制取H2S,该气体易溶于水,密度比空气大收集气体可以用E.
(9)实验方案:因为需要观察收集一瓶气体所用的时间,用排水法更好一些.
结论:由表中数据可知,相同条件下H2O2生成O2的快慢与催化剂的种类有关.故填:相同条件下H2O2生成O2的快慢与催化剂的种类有关.
反思:催化剂在化学反应前后质量和化学性质不变.
假设:H2O2生成O2的快慢与H2O2的质量分数有关.
故答为:(1)a 酒精灯、b 铁架台;(2)A; 将试管平放,用纸槽将高锰酸钾粉末送入试管底部;高锰酸钾
锰酸钾+二氧化锰+氧气.(3)氧气的密度略大于空气;将带火星的木条伸入集气瓶口.
(4)③④⑤①②⑦⑥;(5)①试管口处未加一团棉花.②试管口为向下倾斜.③先熄灭酒精灯,后撤导气管.④有气泡冒出就马上收集.(6)过氧化氢
水+氧气;B;催化; 用弹簧夹夹住右边导管,向长颈漏斗中倒水,液面高度不变,说明装置气密性良好.(7)A;C;D.(8)B;E.(9)实验方案:排水法;.结论:相同条件下H2O2生成O2的快慢与催化剂的种类有关.反思:质量、化学性质.假设:H2O2生成O2的快慢与H2O2的质量分数有关.
(2)用高锰酸钾制取氧气时,属于加热固体制取气体,可选用的发生装置是A,将高锰酸钾装入容器内的方法是:将试管平放,用纸槽将高锰酸钾粉末送入试管底部.发生反应的文字表达式为:高锰酸钾
| 加热 |
(3)若用E装置收集氧气,属于向上排空气集气法,则依据是:氧气的密度略大于空气.由于氧气有助燃性,所以检验氧气是否集满的方法是:将带火星的木条伸入集气瓶口.
(4)在实验室用用高锰酸钾制取氧气时,先要检查装置的气密性,装入高锰酸钾,在将试管固定在铁架台上,开始加热,收集气体实验完毕,先将导管移出水面后再熄灭酒精灯.所以正确的顺序为③④⑤①②⑦⑥.
(5)①水槽中的水呈紫色可能的原因是试管口处未加一团棉花,高锰酸钾粉末从导管进入水槽.
②加热的过程中,试管破裂的原因可能有:试管口未向上倾斜等.
③收集氧气结束时,水沿导管进入试管 的可能原因是:先熄灭酒精灯,后撤导气管.
④用排水法收集到的氧气不纯的原因可能是:有气泡冒出就马上收集等.
(6)用双氧水和二氧化锰来制取氧气的文字表达式为:过氧化氢
| 二氧化锰 |
(7)实验室用无水醋酸钠固体和固体碱石灰加热制取甲烷气体.属于加热固体制取气体.选用A发生装置制取甲烷,甲烷的密度比空气小,不溶于水收集气体时可选用C或D.
(8)实验室用FeS固体和稀硫酸在常温下可以制取H2S气体,属于固液常温下反应制取气体,应选用B发生装置制取H2S,该气体易溶于水,密度比空气大收集气体可以用E.
(9)实验方案:因为需要观察收集一瓶气体所用的时间,用排水法更好一些.
结论:由表中数据可知,相同条件下H2O2生成O2的快慢与催化剂的种类有关.故填:相同条件下H2O2生成O2的快慢与催化剂的种类有关.
反思:催化剂在化学反应前后质量和化学性质不变.
假设:H2O2生成O2的快慢与H2O2的质量分数有关.
故答为:(1)a 酒精灯、b 铁架台;(2)A; 将试管平放,用纸槽将高锰酸钾粉末送入试管底部;高锰酸钾
| 加热 |
(4)③④⑤①②⑦⑥;(5)①试管口处未加一团棉花.②试管口为向下倾斜.③先熄灭酒精灯,后撤导气管.④有气泡冒出就马上收集.(6)过氧化氢
| 二氧化锰 |
点评:本题的综合性非常强,题的容量非常大,涉及到常见的气体的制取.解题时只要把握住了制取气体的装置确定的因素就可分析解答.

练习册系列答案
相关题目

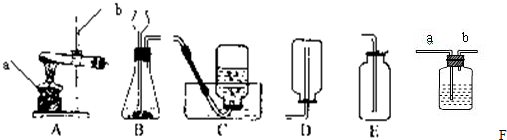

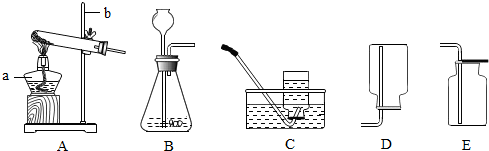
 实验室常用下列装置来制取氧气:
实验室常用下列装置来制取氧气: