摘要:①图l所示实验中数据记录纸上应该连续记录的实验数据是 和 .②由图2中曲线可以看出.固体物质与液体物质反应.当其他条件相同时.接触面积越 .其反应速率越 .③试求样品中碳酸钙的质量分数(假设样品中其他杂质不参加反应.不考虑水.氯化氢逸 出).
网址:http://m.1010jiajiao.com/timu_id_895762[举报]
某化学兴趣小组的同学对实验室制取氧气的实验展开了如下探究:

(1)小明同学选用如图1所示的装置制取氧气.制取过程中所发生反应的化学反应方程式为:
(2)小雨阅读课外资料得知:双氧水分解除了用二氧化锰还可用氧化铜等物质作催化剂,于是他对氧化铜产生了探究兴趣.
【提出问题】
氧化铜是否也能作氯酸钾分解的催化剂?它是否比二氧化锰催化效果更好?
【设计实验】
小雨以生成等体积的氧气为标准,设计了下列三组实验(其它可能影响实验的因素均忽略).
①上述实验应测量的“待测数据”是
②若实验②比实验①的“待测数据”更
③将实验②反应后的固体经提纯分离仍得到0.5克黑色粉末,再将黑色粉末放入试管中,
【评价设计】你认为小雨设计实验③和实验②对比的目的是
(3)小林同学对“过氧化氢溶液的浓度对反应速度有何影响”展开如下探究:取不同浓度的过氧化氢溶液,在其他条件相同的情况下进行实验,记录数据如下:
①根据以上数据分析过氧化氢溶液的浓度对反应速度有怎样的影响:
②小芳同学验证实验后二氧化锰的质量是否仍为0.5g,她取反应后的溶液进行如下操作:
查看习题详情和答案>>

(1)小明同学选用如图1所示的装置制取氧气.制取过程中所发生反应的化学反应方程式为:
2H2O2
2H2O+O2↑
| ||
2H2O2
2H2O+O2↑
.实验前小明同学先向仪器A中加入水,然后将导气管放入水槽中,并打开仪器A的活塞,观察导气管口是否有连续的气泡出现.该实验操作的目的是
| ||
检查装置的气密性
检查装置的气密性
.(2)小雨阅读课外资料得知:双氧水分解除了用二氧化锰还可用氧化铜等物质作催化剂,于是他对氧化铜产生了探究兴趣.
【提出问题】
氧化铜是否也能作氯酸钾分解的催化剂?它是否比二氧化锰催化效果更好?
【设计实验】
小雨以生成等体积的氧气为标准,设计了下列三组实验(其它可能影响实验的因素均忽略).
| 实验序号 | KClO3质量 | 其他物质质量 | 待测数据 |
| ① | 1.2g | l | |
| ② | 1.2g | CuO 0.5g | |
| ③ | 1.2g | MnO2 0.5g |
得到相同质量的氧气所需要的时间
得到相同质量的氧气所需要的时间
.②若实验②比实验①的“待测数据”更
小
小
(填“大”或“小”),说明氧化铜能加快氯酸钾的分解速率.③将实验②反应后的固体经提纯分离仍得到0.5克黑色粉末,再将黑色粉末放入试管中,
加入氯酸钾固体加热,一会儿就有气泡冒出
加入氯酸钾固体加热,一会儿就有气泡冒出
(简述操作和现象),说明氧化铜还能作氯酸钾的催化剂.【评价设计】你认为小雨设计实验③和实验②对比的目的是
比较氧化铜和二氧化锰哪个催化效果更好
比较氧化铜和二氧化锰哪个催化效果更好
.(3)小林同学对“过氧化氢溶液的浓度对反应速度有何影响”展开如下探究:取不同浓度的过氧化氢溶液,在其他条件相同的情况下进行实验,记录数据如下:
| 实验 | 1 | 2 | 3 | 4 | 5 |
| 过氧化氢溶液的浓度 | 1% | 3% | 5% | 10% | 15% |
| MnO2粉末用量/g | 0.5 | 0.5 | 0.5 | 0.5 | 0.5 |
| 收集到500mL气体时所用时间/秒 | 560 | 186 | 103 | 35 | 12 |
过氧化氢溶液的浓度越大,反应的速度越快
过氧化氢溶液的浓度越大,反应的速度越快
;②小芳同学验证实验后二氧化锰的质量是否仍为0.5g,她取反应后的溶液进行如下操作:
过滤
过滤
、洗涤、干燥、称量,她用如图2所示的装置进行实验,试指出图中的三处错误用烧杯直接向漏斗内倒液体
用烧杯直接向漏斗内倒液体
;液面高于滤纸边缘
液面高于滤纸边缘
;漏斗的下端在烧杯的中央
漏斗的下端在烧杯的中央
.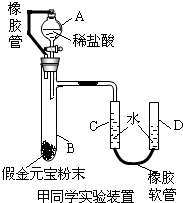 (2011?大庆)社会上曾经出现过有些不法分子用假金元宝骗取路人财物的案件.假设假金元宝为Cu和Zn的合金.甲、乙、丙三位同学为了测定假金元宝中锌的质量分数设计了如下实验步骤:
(2011?大庆)社会上曾经出现过有些不法分子用假金元宝骗取路人财物的案件.假设假金元宝为Cu和Zn的合金.甲、乙、丙三位同学为了测定假金元宝中锌的质量分数设计了如下实验步骤:①连接装置并检查装置的气密性;
②向试管B中加入假金元宝样品粉末;
③准确操作,记录C中液面刻度(C为带有刻度的量气管,D为可上下移动的水准管);
④由A向B中滴加稀盐酸至过量;
⑤B中不在有气体产生并恢复至室温后,准确操作,记录C中液面刻度,计算得到气体的体积为VmL(经查,该气体密度为ρ?g/L).
(1)B中发生的化学反应的化学方程式
Zn+2HCl═ZnCl2+H2↑
Zn+2HCl═ZnCl2+H2↑
.(2)如何向试管B中加粉末状药品
试管横放,用药匙(或纸槽)将药品送至试管底部,慢慢竖起试管
试管横放,用药匙(或纸槽)将药品送至试管底部,慢慢竖起试管
.(3)连接A、B的橡胶管的作用①
使分液漏斗内压强与试管内压强相同,有利于液体顺利流下
使分液漏斗内压强与试管内压强相同,有利于液体顺利流下
,②排除向加入盐酸体积对气体体积的影响,减小误差
排除向加入盐酸体积对气体体积的影响,减小误差
.(4)甲同学在不改变实验装置的情况下,如何在加入试剂前检查装置的气密性
从D管加入适量水,向上移动D管,若C、D两管内液面差保持稳定,则装置气密性良好
从D管加入适量水,向上移动D管,若C、D两管内液面差保持稳定,则装置气密性良好
.(5)甲同学发现试验中缺少某一步骤,导致缺少某一数据而无法计算,该步骤是:
称量所取样品的质量
称量所取样品的质量
,假设此步骤测得的数据用a表示,请结合以上数据计算锌的质量分数为| 13ρV |
| 4a |
| 13ρV |
| 4a |
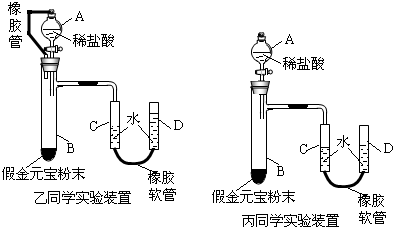
(6)以上是乙、丙两位同学做上述实验的装置,且在步骤⑤读数时装置所处的稳定状态图,则将会对实验结果产生的影响是(假设其余步骤完善且操作准确无误):乙
偏小
偏小
,丙偏大
偏大
(填“偏大”、“偏小”或“无影响”).下图是实验室所用盐酸试剂瓶上标签的部分内容,请仔细阅读后计算:
(1)欲配制14.6%的稀盐酸1000g,需用这种盐酸多少毫升?(计算结果精确到0.1)

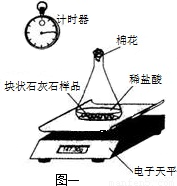
(2)取20.00g石灰石样品平均分成两份,分别与足量相同质量分数的稀盐酸反应进行下列测定(如图l),经数据处理得到释放出二氧化碳的质量与反应时间的关系图(如图2)。

①图1所示实验中数据记录纸上应该连续记录的实验数据是 和 。
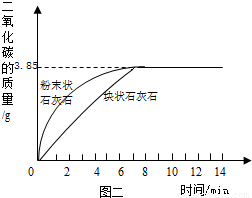
②由图2中曲线可以看出,固体物质与液体物质反应,当其他条件相同时,接触面积越
,其反应速率越 。
③试求样品中碳酸钙的质量分数(假设样品中其他杂质不参加反应,不考虑水、氯化氢逸出)。
查看习题详情和答案>>
如图是实验室所用盐酸试剂瓶上标签的部分内容,请仔细阅读后计算:
(1)欲配制14.6%的稀盐酸1000g,需用这种盐酸多少毫升?(计算结果精确到0.1)

(1)欲配制14.6%的稀盐酸1000g,需用这种盐酸多少毫升?(计算结果精确到0.1)
| 盐酸(分析纯) 化学式:HCI 相对分子质量:36.5 密度1.18g/cm 质量分数:36%(2)取20.00g石灰石样品平均分成两份,分别与足量相同质量分数的稀盐酸反应进行下列测定(如图l),经数据处理得到释放 出二氧化碳的质量与反应时间的关系图(如图2). 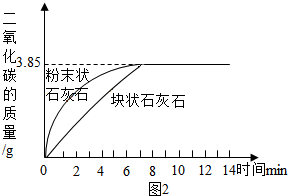 ①图1所示实验中数据记录纸上应该连续记录的实验数据是 ②由图2中曲线可以看出,固体物质与液体物质反应,当其他条件相同时,接触面积越 ③试求样品中碳酸钙的质量分数(假设样品中其他杂质不参加反应,不考虑水、氯化氢逸出).
如图是实验室所用盐酸试剂瓶上标签的部分内容,请仔细阅读后计算:
  (1)欲配制14.6%的稀盐酸1000g,需用这种盐酸多少毫升?(计算结果精确到0.1)
出二氧化碳的质量与反应时间的关系图(如图2). ①图1所示实验中数据记录纸上应该连续记录的实验数据是______和______. ②由图2中曲线可以看出,固体物质与液体物质反应,当其他条件相同时,接触面积越______,其反应速率越______. ③试求样品中碳酸钙的质量分数(假设样品中其他杂质不参加反应,不考虑水、氯化氢逸出).______. 查看习题详情和答案>> |