摘要:(2)反应生成的总质量为 g. (3)为了节约试剂.此实验加入适量盐酸即可恰好完全反应.求: ①此“适量盐酸 的质量.②加入适量盐酸恰好完全反应后所得溶液的溶质质量分数.
网址:http://m.1010jiajiao.com/timu_id_888540[举报]
某同学收集生活中的物质(见下表),建立了家庭小实验室.请你参与下面的探究.
(1)下表是该同学对这些物质分类存放的情况,请你在表中填写物质类别.(选填“金属”、“氧化物”、“酸”、“碱”、“盐”、“有机物”)
(2)食盐是由 构成的,铜是由 构成的,蔗糖是由 构成的.(选填“分子”、“原子”、或“离子”)
(3)请你仅利用表中的物质及水制取氢氧化钠溶液,写出反应的化学方程式: .请你仅利用表中的物质作反应物,另写一个反应的化学方程式: .
(4)请你自制指示剂并测定纯碱溶液的酸碱性,完成下面的实验报告:
(5)该同学粗略测定家里所用白醋中醋酸的质量分数(假设白醋中的酸都看作醋酸,醋酸的化学式为CH3COOH),在玻璃杯中加入10.0g碳酸钙粉末,再倒入200.0g白醋.反应停止后,碳酸钙有剩余,称得玻璃杯中的固体和液体总质量为207.8g.醋酸与碳酸钙反应的化学方程式为:2CH3COOH+CaCO3═(CH3COO)2Ca+CO2↑+H2O若不考虑醋酸与水的挥发及二氧化碳的溶解,求:
①反应生成的二氧化碳质量为 g.
②所测白醋中CH3COOH的质量分数.(写出计算过程)(相对分子质量:H-1,C-12,O-16,Ca-40) 查看习题详情和答案>>
(1)下表是该同学对这些物质分类存放的情况,请你在表中填写物质类别.(选填“金属”、“氧化物”、“酸”、“碱”、“盐”、“有机物”)
| 物质类别 | |||||
| 物质 | 蔗糖、酒精 | 铜丝、铁丝 | 盐酸 | 熟石灰 | 高锰酸钾、食盐、纯碱 |
(3)请你仅利用表中的物质及水制取氢氧化钠溶液,写出反应的化学方程式:
(4)请你自制指示剂并测定纯碱溶液的酸碱性,完成下面的实验报告:
| 实验步骤 | 实验现象 | 结论 |
| ①将切碎的紫包菜放入玻璃杯中,加入 |
自制指示剂呈紫色 | \ |
| ②分别向盛有少量澄清石灰水、盐酸的玻璃杯中加入几滴自制指示剂 | 自制指示剂遇石灰水变蓝色,遇盐酸变红色 | 能使自制指示剂变蓝色的溶液显 |
| ③取少量纯碱放入玻璃杯中,加水搅拌溶解.向其中加加几滴自制指示剂 | 自制指示剂变 |
纯碱溶液显碱性 |
①反应生成的二氧化碳质量为
②所测白醋中CH3COOH的质量分数.(写出计算过程)(相对分子质量:H-1,C-12,O-16,Ca-40) 查看习题详情和答案>>
某同学收集生活中的物质(见下表),建立了家庭小实验室.请你参与下面的探究.
(1)下表是该同学对这些物质分类存放的情况,请你在表中填写物质类别.(选填“金属”、“氧化物”、“酸”、“碱”、“盐”、“有机物”)
| 物质类别 | ________ | ________ | ________ | ________ | ________ |
| 物质 | 蔗糖、酒精 | 铜丝、铁丝 | 盐酸 | 熟石灰 | 高锰酸钾、食盐、纯碱 |
(3)请你仅利用表中的物质及水制取氢氧化钠溶液,写出反应的化学方程式:________.请你仅利用表中的物质作反应物,另写一个反应的化学方程式:________.
(4)请你自制指示剂并测定纯碱溶液的酸碱性,完成下面的实验报告:
| 实验步骤 | 实验现象 | 结论 |
| ①将切碎的紫包菜放入玻璃杯中,加入 ________浸泡,用纱布将浸泡出的紫包菜汁液过滤或挤出,得到自知指示剂 | 自制指示剂呈紫色 | \ |
| ②分别向盛有少量澄清石灰水、盐酸的玻璃杯中加入几滴自制指示剂 | 自制指示剂遇石灰水变蓝色,遇盐酸变红色 | 能使自制指示剂变蓝色的溶液显 ________性,能使自制指示剂变红色的溶液显 ________性. |
| ③取少量纯碱放入玻璃杯中,加水搅拌溶解.向其中加加几滴自制指示剂 | 自制指示剂变 ________色 | 纯碱溶液显碱性 |
①反应生成的二氧化碳质量为________g.
②所测白醋中CH3COOH的质量分数.(写出计算过程)(相对分子质量:H-1,C-12,O-16,Ca-40) 查看习题详情和答案>>
某同学收集生活中的物质(见下表),建立了家庭小实验室.请你参与下面的探究.
(1)下表是该同学对这些物质分类存放的情况,请你在表中填写物质类别.(选填“金属”、“氧化物”、“酸”、“碱”、“盐”、“有机物”)
(2)食盐是由______构成的,铜是由______构成的,蔗糖是由______构成的.(选填“分子”、“原子”、或“离子”)
(3)请你仅利用表中的物质及水制取氢氧化钠溶液,写出反应的化学方程式:______.请你仅利用表中的物质作反应物,另写一个反应的化学方程式:______.
(4)请你自制指示剂并测定纯碱溶液的酸碱性,完成下面的实验报告:
(5)该同学粗略测定家里所用白醋中醋酸的质量分数(假设白醋中的酸都看作醋酸,醋酸的化学式为CH3COOH),在玻璃杯中加入10.0g碳酸钙粉末,再倒入200.0g白醋.反应停止后,碳酸钙有剩余,称得玻璃杯中的固体和液体总质量为207.8g.醋酸与碳酸钙反应的化学方程式为:2CH3COOH+CaCO3═(CH3COO)2Ca+CO2↑+H2O若不考虑醋酸与水的挥发及二氧化碳的溶解,求:
①反应生成的二氧化碳质量为______g.
②所测白醋中CH3COOH的质量分数.(写出计算过程)(相对分子质量:H-1,C-12,O-16,Ca-40)
查看习题详情和答案>>
(1)下表是该同学对这些物质分类存放的情况,请你在表中填写物质类别.(选填“金属”、“氧化物”、“酸”、“碱”、“盐”、“有机物”)
| 物质类别 | ______ | ______ | ______ | ______ | ______ |
| 物质 | 蔗糖、酒精 | 铜丝、铁丝 | 盐酸 | 熟石灰 | 高锰酸钾、食盐、纯碱 |
(3)请你仅利用表中的物质及水制取氢氧化钠溶液,写出反应的化学方程式:______.请你仅利用表中的物质作反应物,另写一个反应的化学方程式:______.
(4)请你自制指示剂并测定纯碱溶液的酸碱性,完成下面的实验报告:
| 实验步骤 | 实验现象 | 结论 |
| ①将切碎的紫包菜放入玻璃杯中,加入 ______浸泡,用纱布将浸泡出的紫包菜汁液过滤或挤出,得到自知指示剂 |
自制指示剂呈紫色 | \ |
| ②分别向盛有少量澄清石灰水、盐酸的玻璃杯中加入几滴自制指示剂 | 自制指示剂遇石灰水变蓝色,遇盐酸变红色 | 能使自制指示剂变蓝色的溶液显 ______性,能使自制指示剂变红色的溶液显 ______性. |
| ③取少量纯碱放入玻璃杯中,加水搅拌溶解.向其中加加几滴自制指示剂 | 自制指示剂变 ______色 |
纯碱溶液显碱性 |
①反应生成的二氧化碳质量为______g.
②所测白醋中CH3COOH的质量分数.(写出计算过程)(相对分子质量:H-1,C-12,O-16,Ca-40)
(相对原子质量:H-1,C-12,Ca-40)某同学粗略测定家里所用白醋中醋酸的质量分数(假设白醋中的酸都看作醋酸,醋酸的化学式为CH3COOH),在玻璃杯中加入100g碳酸钙粉末,再倒入200.0g白醋.反应停止后,碳酸钙有剩余,称得玻璃杯中的固体和液体总质量为297.8g.醋酸与碳酸钙反应的化学方程式为:2CH3COOH+CaCO3═(CH3COO)2Ca+CO2↑+H2O.若不考虑醋酸与水的挥发及二氧化碳的溶解,求:
①反应生成的二氧化碳质量为
②写出求溶液中醋酸质量(X)的比例式
=
=
;
③所测白醋中CH3COOH的质量分数
查看习题详情和答案>>
①反应生成的二氧化碳质量为
2.2
2.2
g;②写出求溶液中醋酸质量(X)的比例式
| 120 |
| X |
| 44 |
| 2.2g |
| 120 |
| X |
| 44 |
| 2.2g |
③所测白醋中CH3COOH的质量分数
3%
3%
.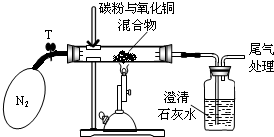 某学习小组对炭粉与氧化铜高温反应产物中气体的成分进行研究.
某学习小组对炭粉与氧化铜高温反应产物中气体的成分进行研究.【猜想】
①气体产物全部是CO2②气体产物是
若猜想①成立,则碳和氧化铜高温反应的化学方程式为:
【设计方案】将一定量氧化铜在隔绝氧气的条件下与过量的炭粉完全反应,测定参加反应的碳元素与氧元素的质量比.
【查阅资料】氮气不与碳、氧化铜产生反应,可用来隔绝氧气.
【实验】
| 操作步骤及实验现象 | 简答 |
| ①称取8g氧化铜与2g碳粉均匀混合,放入重48.4g的玻璃管中,按上图装置连接 | / |
| ②加热前,先通一段时间纯净、干燥的氮气 | 其目的是 |
| ③夹紧T处弹簧夹,加热一段时间,澄清石灰水变浑浊 | 澄清石灰水变浑浊的化学方程式为: |
| ④完全反应后,冷却至室温,称得玻璃管和固体的总质量为56.0g | / |
【结论】根据数据处理结果,得出猜想