题目内容
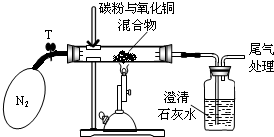 某学习小组对炭粉与氧化铜高温反应产物中气体的成分进行研究.
某学习小组对炭粉与氧化铜高温反应产物中气体的成分进行研究.【猜想】
①气体产物全部是CO2②气体产物是
若猜想①成立,则碳和氧化铜高温反应的化学方程式为:
【设计方案】将一定量氧化铜在隔绝氧气的条件下与过量的炭粉完全反应,测定参加反应的碳元素与氧元素的质量比.
【查阅资料】氮气不与碳、氧化铜产生反应,可用来隔绝氧气.
【实验】
| 操作步骤及实验现象 | 简答 |
| ①称取8g氧化铜与2g碳粉均匀混合,放入重48.4g的玻璃管中,按上图装置连接 | / |
| ②加热前,先通一段时间纯净、干燥的氮气 | 其目的是 |
| ③夹紧T处弹簧夹,加热一段时间,澄清石灰水变浑浊 | 澄清石灰水变浑浊的化学方程式为: |
| ④完全反应后,冷却至室温,称得玻璃管和固体的总质量为56.0g | / |
【结论】根据数据处理结果,得出猜想
分析:根据质量守恒定律可以书写化学方程式,根据相关数据可以进行相关方面的计算.
解答:解:【猜想】再一种情况是CO2和CO的混合物;故填:CO2和CO的混合物.
一氧化碳与氧化铜反应生成铜和二氧化碳,故填:2CuO+C
2Cu+CO2↑
【实验】先通入氮气能排出玻璃管内的空气,防止对实验造成干扰,目的是:排除玻璃管内空气对实验的干扰;
二氧化碳与氢氧化钙反应生成碳酸钙沉淀和水,故填:CO2+Ca(OH)2=CaCO3↓+H2O
【数据处理】根据质量守恒定律可得反应生成的气体质量为:48.4g+2g+8g-56.0g=2.4g.故填:2.4;
气体中碳元素的质量为:2.4g-1.6g=0.8g.故填:0.8.
一氧化碳中碳元素和氧元素的质量比为:12:16.二氧化碳中碳元素和氧元素的质量比为:12:44.都不是0.8g:1.6g=1:2.所以气体是一氧化碳和二氧化碳的混合物.
【结论】猜想②成立.
一氧化碳与氧化铜反应生成铜和二氧化碳,故填:2CuO+C
| ||
【实验】先通入氮气能排出玻璃管内的空气,防止对实验造成干扰,目的是:排除玻璃管内空气对实验的干扰;
二氧化碳与氢氧化钙反应生成碳酸钙沉淀和水,故填:CO2+Ca(OH)2=CaCO3↓+H2O
【数据处理】根据质量守恒定律可得反应生成的气体质量为:48.4g+2g+8g-56.0g=2.4g.故填:2.4;
气体中碳元素的质量为:2.4g-1.6g=0.8g.故填:0.8.
一氧化碳中碳元素和氧元素的质量比为:12:16.二氧化碳中碳元素和氧元素的质量比为:12:44.都不是0.8g:1.6g=1:2.所以气体是一氧化碳和二氧化碳的混合物.
【结论】猜想②成立.
点评:本题主要考查了化学方程式的书写及其质量守恒定律的应用等方面的内容.完成此题可以依据物质的性质及题干提供的数据进行.

练习册系列答案
相关题目
 某学习小组对炭粉与氧化铜高温反应产物中气体的成分进行研究.
某学习小组对炭粉与氧化铜高温反应产物中气体的成分进行研究.
【猜想】
①气体产物全部是CO2②气体产物是________③气体产物全部是CO
若猜想①成立,则碳和氧化铜高温反应的化学方程式为:________;
【设计方案】将一定量氧化铜在隔绝氧气的条件下与过量的炭粉完全反应,测定参加反应的碳元素与氧元素的质量比.
【查阅资料】氮气不与碳、氧化铜产生反应,可用来隔绝氧气.
【实验】
| 操作步骤及实验现象 | 简答 |
| ①称取8g氧化铜与2g碳粉均匀混合,放入重48.4g的玻璃管中,按上图装置连接 | / |
| ②加热前,先通一段时间纯净、干燥的氮气 | 其目的是________ |




