摘要:A.氧化钙+水氢氧化钙 B.水 + 二氧化碳碳酸
网址:http://m.1010jiajiao.com/timu_id_886489[举报]
氢氧化钙在生产和生活中有广泛的用途,请按要求回答问题:
(1)氢氧化钙的俗称
(2)氢氧化钙在部分温度下的溶解度如下表所示.
①20℃时,0.56g氧化钙放入到盛有100g水的烧杯中.恢复到20℃时,所得溶液中水的质量
②采用一种操作方法,将上述烧杯中剩余固体全部溶解,变为不饱和溶液.下列说法正确的是(填序号)
A.溶液的质量可能不变B.溶液中溶质的质量分数一定减小
C.溶液中溶质的质量一定增大D.可以升温使之变成不饱和溶液.
查看习题详情和答案>>
(1)氢氧化钙的俗称
熟石灰(或消石灰)
熟石灰(或消石灰)
,其水溶液的pH>
>
7(填“<”或“>”或“=”).农业上一般采用氢氧化钙改良酸
酸
性土壤(填“酸”或“碱”).氢氧化钙变质是由于与空气中的二氧化碳
二氧化碳
发生反应的缘故,反应的化学程式是:CO2+Ca(OH)2=CaCO3↓+H2O
CO2+Ca(OH)2=CaCO3↓+H2O
,因此氢氧化钙应密封
密封
保存.(2)氢氧化钙在部分温度下的溶解度如下表所示.
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
| 溶解度/g | 0.18 | 0.17 | 0.16 | 0.15 | 0.14 | 0.13 | 0.12 |
减小
减小
(填“增大”、“减小”或“不变”),溶液中溶质的质量分数是0.16%
0.16%
.②采用一种操作方法,将上述烧杯中剩余固体全部溶解,变为不饱和溶液.下列说法正确的是(填序号)
BC
BC
.A.溶液的质量可能不变B.溶液中溶质的质量分数一定减小
C.溶液中溶质的质量一定增大D.可以升温使之变成不饱和溶液.
氢氧化钙俗称熟石灰、消石灰等,微溶于水,其水溶液又称石灰水,它与二氧化碳能发生如下反应:CO2+Ca(OH)2=CaCO3↓+H2O,这一反应原理在生产生活和实验中有着广泛的应用.下列应用与该原理无关的是( )
查看习题详情和答案>>
氢氧化钙俗称熟石灰、消石灰等,微溶于水,其水溶液又称石灰水,它与二氧化碳能发生如下反应:CO2+Ca(OH)2=CaCO3↓+H2O,这一反应原理在生产生活和实验中有着广泛的应用.下列应用与该原理无关的是
- A.石灰水应密封保存,以防变质
- B.用石灰水保存鸡蛋
- C.用石灰浆砌砖抹墙
- D.施用熟石灰改良酸性土壤
氢氧化钠固体及溶液在空气中很容易发生变质生成碳酸钠.
(1)甲同学在实验室里发现一瓶敞口放置的氢氧化钠溶液,对其变质情况进行了如下探究.
【猜想与假设】该氢氧化钠溶液已部分变质.
【实验与结论】
【拓展探究】甲同学又尝试通过实验除去该氢氧化钠溶液中含有的碳酸钠,方案如下:
向该溶液中加入
(2)乙同学在实验室里发现少量部分变质的氢氧化钠固体,尝试通过实验测定其中碳酸钠的质量分数.
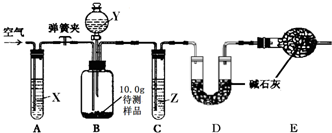
【设计和进行实验】乙同学设计了如图所示的实验装置(铁架台、铁夹等固定用装置已略去,碱石灰是固体氢氧化钠和生石灰的混合物).取10.0g待测样品,进行实验.实验步骤如下:
a.连接好装置,并检查气密性;
b.打开弹簧夹,缓缓通入一段时间空气;
c.称量装置D的质量为83.4g;
d.关闭弹簧夹,慢慢滴加Y溶液,至不再产生气泡为止;
e.打开弹簧夹,再次缓缓通入一段时间空气;
f.再次称量装置D的质量为84.5g.
【交流讨论】
①试剂X、Y、Z依次最适宜选用
A.氢氧化钠溶液 浓盐酸 浓硫酸 B.澄清石灰水 稀盐酸 稀硫酸
C.氢氧化钠溶液 稀硫酸 浓硫酸 D.浓硫酸 稀硫酸 氢氧化钠溶液
②步骤e中通入空气的作用是
③若没有装置C,则会导致测定结果
【交流讨论】根据实验中测得的有关数据,计算部分变质的氢氧化钠固体中碳酸钠的质量分数.
查看习题详情和答案>>

(1)甲同学在实验室里发现一瓶敞口放置的氢氧化钠溶液,对其变质情况进行了如下探究.
【猜想与假设】该氢氧化钠溶液已部分变质.
【实验与结论】
| 实验步骤 | 实验现象 | 实验结论 |
| a.取少量该溶液于一支试管中,加入 足量的氯化钙溶液 足量的氯化钙溶液 |
有白色沉淀生成 有白色沉淀生成 |
该氢氧化钠溶液已变质 |
| b.将步骤a所得的液体静置,取上层清液于另一支试管中,滴加 无色酚酞试液 无色酚酞试液 |
酚酞试液变红 酚酞试液变红 |
该氢氧化钠溶液已部分变质 |
向该溶液中加入
氢氧化钙
氢氧化钙
,充分反应后,经过滤
过滤
操作,即可除去该氢氧化钠溶液中含有的杂质.(2)乙同学在实验室里发现少量部分变质的氢氧化钠固体,尝试通过实验测定其中碳酸钠的质量分数.
【设计和进行实验】乙同学设计了如图所示的实验装置(铁架台、铁夹等固定用装置已略去,碱石灰是固体氢氧化钠和生石灰的混合物).取10.0g待测样品,进行实验.实验步骤如下:
a.连接好装置,并检查气密性;
b.打开弹簧夹,缓缓通入一段时间空气;
c.称量装置D的质量为83.4g;
d.关闭弹簧夹,慢慢滴加Y溶液,至不再产生气泡为止;
e.打开弹簧夹,再次缓缓通入一段时间空气;
f.再次称量装置D的质量为84.5g.
【交流讨论】
①试剂X、Y、Z依次最适宜选用
C
C
(选填字母).A.氢氧化钠溶液 浓盐酸 浓硫酸 B.澄清石灰水 稀盐酸 稀硫酸
C.氢氧化钠溶液 稀硫酸 浓硫酸 D.浓硫酸 稀硫酸 氢氧化钠溶液
②步骤e中通入空气的作用是
将B中产生的二氧化碳全部赶到D装置中
将B中产生的二氧化碳全部赶到D装置中
.③若没有装置C,则会导致测定结果
偏大
偏大
(选填“偏大”、“偏小”或“无影响”,下同);若没有装置E,则会导致测定结果偏大
偏大
.【交流讨论】根据实验中测得的有关数据,计算部分变质的氢氧化钠固体中碳酸钠的质量分数.
氢氧化钠、氢氧化钙等是初中化学中常用的碱,请结合信息回答问题:
Ⅰ.下表是NaOH和Ca(OH)2的溶解度数据:
(1)从表中数据可以获得的信息是______.(写一条)
(2)把80℃时NaOH的饱和溶液降温至20℃,可以看到的现象是______.
Ⅱ.查阅资料发现:氢氧化钾的性质与氢氧化钠的性质相似.A.纯净的氢氧化钾是白色固体;B.它极易溶解于水;C.氢氧化钾固体置于空气中易吸水而潮解;D.氢氧化钾能吸收空气中的二氧化碳;E.氢氧化钾和硫酸溶液可以发生中和反应.
(1)从上面的短文中得知,氢氧化钾的物理性质为______(填字母序号).
(2)写出资料中涉及到的与氢氧化钾的化学性质有关的化学方程式:______.
(3)根据氢氧化钾的性质,你认为保存其固体的方法是______.
查看习题详情和答案>>
Ⅰ.下表是NaOH和Ca(OH)2的溶解度数据:
溶解度/g 温度/℃ 物质 | 20 | 40 | 60 | 80 | 100 | |
| NaOH | 31 | 91 | 111 | 129 | 313 | 336 |
| Ca(OH)2 | 0.19 | 0.17 | 0.14 | 0.12 | 0.09 | 0.08 |
(2)把80℃时NaOH的饱和溶液降温至20℃,可以看到的现象是______.
Ⅱ.查阅资料发现:氢氧化钾的性质与氢氧化钠的性质相似.A.纯净的氢氧化钾是白色固体;B.它极易溶解于水;C.氢氧化钾固体置于空气中易吸水而潮解;D.氢氧化钾能吸收空气中的二氧化碳;E.氢氧化钾和硫酸溶液可以发生中和反应.
(1)从上面的短文中得知,氢氧化钾的物理性质为______(填字母序号).
(2)写出资料中涉及到的与氢氧化钾的化学性质有关的化学方程式:______.
(3)根据氢氧化钾的性质,你认为保存其固体的方法是______.
查看习题详情和答案>>