摘要:0产生气体质量(g)
网址:http://m.1010jiajiao.com/timu_id_881446[举报]
气体的实验室制法是一种重要的实验基本技能,请回顾二氧化碳的实验室制法,回答下列问题:
(1)化学反应能生成二氧化碳的反应很多,如见下面反应
①C+O2
CO2
②Na2CO3+2HCl=2NaCl+H20+CO2↑
③CaCO3+2HCl=2CaCl2+H20+CO2↑
④CaC2O4
CaO+CO↑+CO2↑
⑤CO+Fe2O3
2Fe+3CO2
…
请任意分析上面一个不适合于实验制取二氧化碳的反应的原因:
(2)盐酸密度(20℃时)和其溶质质量分数之间的关系
①分析上述数据可得到一个结论:
②现要配制200ml溶质质量分数为8.5%的稀盐酸用于制取二氧化碳,则需要溶质质量分数为37.2%的浓盐酸
(3)下面是二氧化碳的制取、净化、收集和量气的相关实验
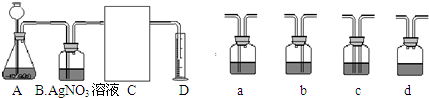
(温馨提示:C装置中装饱和碳酸氢钠溶液,二氧化碳不溶于饱和碳酸氢钠溶液)
①A中的长颈漏斗如果用分液漏斗代替的好处是
②实验过程B装置产生的主要实验现象是:
涉及化学反应是
③方线框中的C装置应该选择上面提供的a、b、c、d的
查看习题详情和答案>>
(1)化学反应能生成二氧化碳的反应很多,如见下面反应
①C+O2
| ||
②Na2CO3+2HCl=2NaCl+H20+CO2↑
③CaCO3+2HCl=2CaCl2+H20+CO2↑
④CaC2O4
| ||
⑤CO+Fe2O3
| ||
…
请任意分析上面一个不适合于实验制取二氧化碳的反应的原因:
反应②Na2CO3+2HCl═2NaCl+H20+CO2↑该反应速率太快,不利于收集
反应②Na2CO3+2HCl═2NaCl+H20+CO2↑该反应速率太快,不利于收集
.现提供有①纯净的CaCO3白色粉末,②大理石,③稀盐酸,③浓盐酸,④稀硫酸,⑤浓硫酸.其中最适合用于实验室制取二氧化碳的药品是②③
②③
(填代号)(2)盐酸密度(20℃时)和其溶质质量分数之间的关系
| 密度(ρ)/g?ml-1 | 1.00 | 1.02 | 1.04 | 1.06 | 1.08 | 1.10 | 1.12 | 1.14 | 1.16 | 1.185 |
| 溶质质量分数(w)/% | 0.4 | 4.4 | 8.5 | 12.5 | 16.5 | 20.4 | 24.2 | 28.2 | 32.2 | 37.2 |
溶液质量分数越大,其密度也越大
溶液质量分数越大,其密度也越大
;盐酸是氯化氢气体溶于水得到的溶液,升高盐酸溶液的温度,其密度将变减小
减小
.②现要配制200ml溶质质量分数为8.5%的稀盐酸用于制取二氧化碳,则需要溶质质量分数为37.2%的浓盐酸
40.1mL
40.1mL
ml.配制过程中要用到量筒、胶头滴管
胶头滴管
、烧杯、玻璃棒等仪器.(3)下面是二氧化碳的制取、净化、收集和量气的相关实验

(温馨提示:C装置中装饱和碳酸氢钠溶液,二氧化碳不溶于饱和碳酸氢钠溶液)
①A中的长颈漏斗如果用分液漏斗代替的好处是
分液漏斗比长颈漏斗能更方便的控制反应速率
分液漏斗比长颈漏斗能更方便的控制反应速率
②实验过程B装置产生的主要实验现象是:
产生白色沉淀
产生白色沉淀
;涉及化学反应是
AgNO3+HC═lAgCl↓+HNO3
AgNO3+HC═lAgCl↓+HNO3
.③方线框中的C装置应该选择上面提供的a、b、c、d的
a
a
.
气体的实验室制法是一种重要的实验基本技能,请回顾二氧化碳的实验室制法,回答下列问题:
(1)化学反应能生成二氧化碳的反应很多,如见下面反应
①C+O2 CO2
CO2
②Na2CO3+2HCl=2NaCl+H20+CO2↑
③CaCO3+2HCl=2CaCl2+H20+CO2↑
④CaC2O4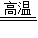 CaO+CO↑+CO2↑
CaO+CO↑+CO2↑
⑤CO+Fe2O3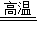 2Fe+3CO2
2Fe+3CO2
…
请任意分析上面一个不适合于实验制取二氧化碳的反应的原因:______.现提供有①纯净的CaCO3白色粉末,②大理石,③稀盐酸,③浓盐酸,④稀硫酸,⑤浓硫酸.其中最适合用于实验室制取二氧化碳的药品是______(填代号)
(2)盐酸密度(20℃时)和其溶质质量分数之间的关系
①分析上述数据可得到一个结论:______;盐酸是氯化氢气体溶于水得到的溶液,升高盐酸溶液的温度,其密度将变______.
②现要配制200ml溶质质量分数为8.5%的稀盐酸用于制取二氧化碳,则需要溶质质量分数为37.2%的浓盐酸______ml.配制过程中要用到量筒、______、烧杯、玻璃棒等仪器.
(3)下面是二氧化碳的制取、净化、收集和量气的相关实验
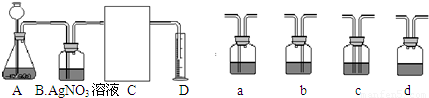
(温馨提示:C装置中装饱和碳酸氢钠溶液,二氧化碳不溶于饱和碳酸氢钠溶液)
①A中的长颈漏斗如果用分液漏斗代替的好处是______
②实验过程B装置产生的主要实验现象是:______;
涉及化学反应是______.
③方线框中的C装置应该选择上面提供的a、b、c、d的______.
查看习题详情和答案>>
(1)化学反应能生成二氧化碳的反应很多,如见下面反应
①C+O2
 CO2
CO2②Na2CO3+2HCl=2NaCl+H20+CO2↑
③CaCO3+2HCl=2CaCl2+H20+CO2↑
④CaC2O4
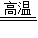 CaO+CO↑+CO2↑
CaO+CO↑+CO2↑⑤CO+Fe2O3
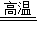 2Fe+3CO2
2Fe+3CO2…
请任意分析上面一个不适合于实验制取二氧化碳的反应的原因:______.现提供有①纯净的CaCO3白色粉末,②大理石,③稀盐酸,③浓盐酸,④稀硫酸,⑤浓硫酸.其中最适合用于实验室制取二氧化碳的药品是______(填代号)
(2)盐酸密度(20℃时)和其溶质质量分数之间的关系
| 密度(ρ)/g?ml-1 | 1.00 | 1.02 | 1.04 | 1.06 | 1.08 | 1.10 | 1.12 | 1.14 | 1.16 | 1.185 |
| 溶质质量分数(w)/% | 0.4 | 4.4 | 8.5 | 12.5 | 16.5 | 20.4 | 24.2 | 28.2 | 32.2 | 37.2 |
②现要配制200ml溶质质量分数为8.5%的稀盐酸用于制取二氧化碳,则需要溶质质量分数为37.2%的浓盐酸______ml.配制过程中要用到量筒、______、烧杯、玻璃棒等仪器.
(3)下面是二氧化碳的制取、净化、收集和量气的相关实验

(温馨提示:C装置中装饱和碳酸氢钠溶液,二氧化碳不溶于饱和碳酸氢钠溶液)
①A中的长颈漏斗如果用分液漏斗代替的好处是______
②实验过程B装置产生的主要实验现象是:______;
涉及化学反应是______.
③方线框中的C装置应该选择上面提供的a、b、c、d的______.
查看习题详情和答案>>
(1)某校研究性学习小组欲配制1000g溶质质量分数为15%的氢氧化钠溶液.需氢氧化钠固体 g,水 mL(水的密度是1g/cm3);称量氢氧化钠时 (填“能”或“不能”)放在纸上称量.
(2)甲乙丙丁四位同学在探究碱溶液与酚酞作用的实验时,发现了一个意外现象:氢氧化钠溶液滴入酚酞试液,溶液变成了红色,一会儿红色就消失了.
【猜想】:
甲:可能是酚酞变质的缘故;
乙:可能是氢氧化钠溶液与空气中二氧化碳反应的缘故;
丙:可能是酚酞与空气中氧气反应,使红色消失的缘故;
丁:可能与氢氧化钠溶液质量分数大小有关.
【理论分析】:
①甲同学刚提出自己的猜想,就遭到其余三位同学的否定,三位同学的理由是 .
②乙同学的猜想也不正确,理由是 .
【实验设计】:
③为证实丙同学的猜想,还需作如下实验,请完成下表.
④通过以上实验,四位同学看到:溶液先变成红色,一会儿红色又消失.因此酚酞红色褪去与氧气无关.若丁同学的猜想正确,设计如下实验证明并完成有关问题:
实验方法:观察到的现象和结论;
(3)质量分数小的溶液中红色不消失,质量分数大的溶液中红色会消失,则证明
.
方案二:将滴有酚酞试液的质量分数大的氢氧化钠溶液加水稀释观察到的现象和结论: .
(4)(8分)该校研究性学习小组向上述所配制的15%的氢氧化钠溶液中滴加稀盐酸,有气泡产生,由此可知所用的NaOH固体已变质.写出氢氧化钠在空气中变质的化学方程式 ;所以氢氧化钠应该 保存.(2分)
【提出问题】:所用的NaOH变质程度怎样?
【设计方案】:先称取21.2g 的NaOH样品(杂质为Na2CO3),配成溶液,然后向溶液中逐滴加入一定质量分数的稀硫酸直至过量,根据生成CO2的质量计算出Na2CO3的质量,从而进一步确定样品中NaOH的质量分数.
【进行实验】:实验测得加入稀硫酸的质量与产生CO2气体的质量关系如下图所示.
【数据处理】:写出以下计算过程:
(5)该样品中NaOH的质量分数为多少?
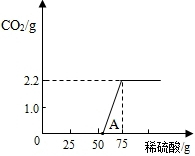
【反思与交流】:①从图中0~A点说明:在NaOH 与Na2CO3的混合溶液中,加入稀硫酸,首先反应的物质是 ;②根据反应方程式分析,NaOH部分变质或全部变质,与没有变质的NaOH相比,中和反应时消耗稀硫酸的量 (填“相等”或“大于”或“小于”.(2分)
查看习题详情和答案>>
(2)甲乙丙丁四位同学在探究碱溶液与酚酞作用的实验时,发现了一个意外现象:氢氧化钠溶液滴入酚酞试液,溶液变成了红色,一会儿红色就消失了.
【猜想】:
甲:可能是酚酞变质的缘故;
乙:可能是氢氧化钠溶液与空气中二氧化碳反应的缘故;
丙:可能是酚酞与空气中氧气反应,使红色消失的缘故;
丁:可能与氢氧化钠溶液质量分数大小有关.
【理论分析】:
①甲同学刚提出自己的猜想,就遭到其余三位同学的否定,三位同学的理由是
②乙同学的猜想也不正确,理由是
【实验设计】:
③为证实丙同学的猜想,还需作如下实验,请完成下表.
| 实验步骤 | 设计这一步骤的目的 |
| 1.用煮沸过的蒸馏水配制氢氧化钠溶液. | |
| 2.在氢氧化钠溶液中滴入酚酞,并在上方滴一些植物油. |
实验方法:观察到的现象和结论;
(3)质量分数小的溶液中红色不消失,质量分数大的溶液中红色会消失,则证明
方案二:将滴有酚酞试液的质量分数大的氢氧化钠溶液加水稀释观察到的现象和结论:
(4)(8分)该校研究性学习小组向上述所配制的15%的氢氧化钠溶液中滴加稀盐酸,有气泡产生,由此可知所用的NaOH固体已变质.写出氢氧化钠在空气中变质的化学方程式
【提出问题】:所用的NaOH变质程度怎样?
【设计方案】:先称取21.2g 的NaOH样品(杂质为Na2CO3),配成溶液,然后向溶液中逐滴加入一定质量分数的稀硫酸直至过量,根据生成CO2的质量计算出Na2CO3的质量,从而进一步确定样品中NaOH的质量分数.
【进行实验】:实验测得加入稀硫酸的质量与产生CO2气体的质量关系如下图所示.
【数据处理】:写出以下计算过程:
(5)该样品中NaOH的质量分数为多少?

【反思与交流】:①从图中0~A点说明:在NaOH 与Na2CO3的混合溶液中,加入稀硫酸,首先反应的物质是
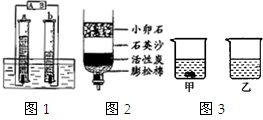 (1)按图1简易装置电解水,A、B是电源的两个电极.
(1)按图1简易装置电解水,A、B是电源的两个电极.①通电一段时间后,量筒a中收集到的气体是
氧气
氧气
,B是电源的负
负
极.②电解水的实验中,加入适量的NaOH可以增加水的导电性而使电解速率加快.在加了氢氧化钠的水中通电一段时间后,溶液中的变化是
BD
BD
.A.溶质质量减少 B.溶剂质量减少 C.溶液质量增加 D.溶质质量分数增大
(2)化学是研究物质的组成、结构、性质及其变化规律的基础自然科学.请回答下列问题:
①从组成角度看:水是由
氢元素和氧元素
氢元素和氧元素
组成的﹔②从微粒角度看:水是由
水分子
水分子
构成的﹔③从资源角度看:水是生命之源,图2是用来净化河水的简易装置,下列说法错误的是
BCD
BCD
.A.水是一种重要的溶剂 B.利用图2装置能把硬水变为软水 C.通过过滤可以除去水中所有的杂质 D.利用图2装置能对水杀菌消毒.
④从变化角度看:水通电分解生成最理想的能源-氢气,电解一定量的水,当其中一个电极产生5ml气体时,另一个电极产生的气体体积可能是
10ml或2.5
10ml或2.5
ml.(3)水是很好的溶剂.下表列出了氯化铵和氯化钠的溶解度,请回答问题:
①40℃时,向两个分别盛有45gNH4Cl和NaCl的烧杯中,各加入100g的水,充分溶解后,结果如图3所示,则乙烧杯中的溶质是
氯化铵
氯化铵
.②采用一种操作方法,将上述烧杯中的固体全部溶解,变为不饱和溶液.在这个过程中,下列说法正确的是
B
B
.(填字母)A.溶剂质量不变 B.溶液中溶质的质量分数一定减少 C.溶液质量一定增大 D.溶液中溶质的质量分数可能增大
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
| 溶解度 /g |
NaCl | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 | 39.8 |
| NH4Cl | 29.4 | 37.2 | 45.8 | 55.2 | 65.6 | 77.3 | |
 (1)汽车尾气处理相关反应为:2NO+2CO→N2+2CO2,
(1)汽车尾气处理相关反应为:2NO+2CO→N2+2CO2,①该反应涉及的物质中,
CO2
CO2
是光合作用的原料;②该反应涉及的一种有毒气体,高温下与赤铁矿石反应的化学方程式为为
3CO+Fe2O3
2Fe+3CO2
| ||
3CO+Fe2O3
2Fe+3CO2
.
| ||
(2)胞嘧啶(C4H5ON3)是DNA水解产物之一,由
4
4
种元素组成,胞嘧啶分子的相对分子质量为111
111
(3)
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 |
| KNO3溶解度g/100g水 | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | 138 |
硝酸钾的溶解度随着温度的升高而增大
硝酸钾的溶解度随着温度的升高而增大
.②60℃时,210g 饱和KNO3溶液,蒸发10g水后,再降温到60℃,可析出KNO3晶体的质量为
11.0g
11.0g
.③如图所示,20℃时,将盛有饱和KNO3溶液的小试管放入盛水的烧杯中,向水中加入某物质后,试管中有晶体析出.加入的物质可能是下列中的
C
C
(填字母序号).A.氢氧化钠固体 B.生石灰固体 C.冰块 D.浓硫酸.