题目内容
(1)某校研究性学习小组欲配制1000g溶质质量分数为15%的氢氧化钠溶液.需氢氧化钠固体(2)甲乙丙丁四位同学在探究碱溶液与酚酞作用的实验时,发现了一个意外现象:氢氧化钠溶液滴入酚酞试液,溶液变成了红色,一会儿红色就消失了.
【猜想】:
甲:可能是酚酞变质的缘故;
乙:可能是氢氧化钠溶液与空气中二氧化碳反应的缘故;
丙:可能是酚酞与空气中氧气反应,使红色消失的缘故;
丁:可能与氢氧化钠溶液质量分数大小有关.
【理论分析】:
①甲同学刚提出自己的猜想,就遭到其余三位同学的否定,三位同学的理由是
②乙同学的猜想也不正确,理由是
【实验设计】:
③为证实丙同学的猜想,还需作如下实验,请完成下表.
| 实验步骤 | 设计这一步骤的目的 |
| 1.用煮沸过的蒸馏水配制氢氧化钠溶液. | |
| 2.在氢氧化钠溶液中滴入酚酞,并在上方滴一些植物油. |
实验方法:观察到的现象和结论;
(3)质量分数小的溶液中红色不消失,质量分数大的溶液中红色会消失,则证明
方案二:将滴有酚酞试液的质量分数大的氢氧化钠溶液加水稀释观察到的现象和结论:
(4)(8分)该校研究性学习小组向上述所配制的15%的氢氧化钠溶液中滴加稀盐酸,有气泡产生,由此可知所用的NaOH固体已变质.写出氢氧化钠在空气中变质的化学方程式
【提出问题】:所用的NaOH变质程度怎样?
【设计方案】:先称取21.2g 的NaOH样品(杂质为Na2CO3),配成溶液,然后向溶液中逐滴加入一定质量分数的稀硫酸直至过量,根据生成CO2的质量计算出Na2CO3的质量,从而进一步确定样品中NaOH的质量分数.
【进行实验】:实验测得加入稀硫酸的质量与产生CO2气体的质量关系如下图所示.
【数据处理】:写出以下计算过程:
(5)该样品中NaOH的质量分数为多少?
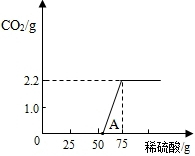
【反思与交流】:①从图中0~A点说明:在NaOH 与Na2CO3的混合溶液中,加入稀硫酸,首先反应的物质是
分析:配制溶液时首先要明确溶质和溶剂的质量,需要根据溶质的质量分数公式进行计算;氢氧化钠容易和二氧化碳发生化学反应而变质为碳酸钠,碳酸钠和氢氧化钠的水溶液都能使酚酞变红,酚酞在氢氧化钠溶液中变色有一定的PH范围.
解答:解:(1)根据溶质质量分数的计算公式可得,所需溶质的质量为1000g×15%=150g,水的质量为1000g-150g=850g,换算为体积就是850mL,由于氢氧化钠具有腐蚀性,称量时不能直接放在托盘的纸上,应放在玻璃器皿中称量,所以本题答案为:150,850,不能;
(2)氢氧化钠溶液滴入酚酞试液,溶液变成了红色,一会儿红色就消失了,说明仍保持了酚酞的特性,不可能变质,故:①答案为:若酚酞试剂变质,就不可能出现遇氢氧化钠溶液变红的现象;而氢氧化钠变质后生成的碳酸钠具有碱性,同样能使酚酞试液变红,故②答案为:碳酸钠溶液显碱性,也可使酚酞试剂变红;用煮沸后的水配制氢氧化钠溶液,是想清除溶解的氧气,在所配的溶液上方滴加植物油是想与空气隔绝,故③答案为:排除水中溶解的氧气,隔绝空气;
(3)质量分数小的溶液中红色不消失,质量分数大的溶液中红色会消失,说明溶液的浓稀影响酚酞的变色,
所以本题答案为:与氢氧化钠溶液质量分数大小有关;
溶液变红,说明与氢氧化钠溶液质量分数大小有关;
(4)氢氧化钠变质是因为与空气中的二氧化碳反应,因为易变质,所以要密封保存,故本题答案为:CO2+2NaOH=Na2CO3+H2O,密封;
(5)解:(1)设样品中碳酸钠的质量为x.
Na2CO3+H2SO4=Na2SO4+H2O+CO2↑
106 44
x 2.2g
=
x=5.3g
样品中含氢氧化钠的质量分数为:
×100%=75%
故本题答案为:75%;
(5)刚开始加入稀硫酸时,无气体产生,说明是氢氧化钠在发生反应,分析反应的化学方程式,①CO2+2NaOH=Na2CO3+H2O,②Na2CO3+H2SO4=Na2SO4+H2O+CO2↑,综合①②,可得:2NaOH++H2SO4=Na2SO4+2H2O,所以NaOH部分变质或全部变质,与没有变质的NaOH相比,中和反应时消耗稀硫酸的量相等,故本题答案为:NaOH,相等.
(2)氢氧化钠溶液滴入酚酞试液,溶液变成了红色,一会儿红色就消失了,说明仍保持了酚酞的特性,不可能变质,故:①答案为:若酚酞试剂变质,就不可能出现遇氢氧化钠溶液变红的现象;而氢氧化钠变质后生成的碳酸钠具有碱性,同样能使酚酞试液变红,故②答案为:碳酸钠溶液显碱性,也可使酚酞试剂变红;用煮沸后的水配制氢氧化钠溶液,是想清除溶解的氧气,在所配的溶液上方滴加植物油是想与空气隔绝,故③答案为:排除水中溶解的氧气,隔绝空气;
(3)质量分数小的溶液中红色不消失,质量分数大的溶液中红色会消失,说明溶液的浓稀影响酚酞的变色,
所以本题答案为:与氢氧化钠溶液质量分数大小有关;
溶液变红,说明与氢氧化钠溶液质量分数大小有关;
(4)氢氧化钠变质是因为与空气中的二氧化碳反应,因为易变质,所以要密封保存,故本题答案为:CO2+2NaOH=Na2CO3+H2O,密封;
(5)解:(1)设样品中碳酸钠的质量为x.
Na2CO3+H2SO4=Na2SO4+H2O+CO2↑
106 44
x 2.2g
| 106 |
| x |
| 44 |
| 2?2g |
x=5.3g
样品中含氢氧化钠的质量分数为:
| 21?2g-5?3g |
| 21?g |
故本题答案为:75%;
(5)刚开始加入稀硫酸时,无气体产生,说明是氢氧化钠在发生反应,分析反应的化学方程式,①CO2+2NaOH=Na2CO3+H2O,②Na2CO3+H2SO4=Na2SO4+H2O+CO2↑,综合①②,可得:2NaOH++H2SO4=Na2SO4+2H2O,所以NaOH部分变质或全部变质,与没有变质的NaOH相比,中和反应时消耗稀硫酸的量相等,故本题答案为:NaOH,相等.
点评:本题主要考查了氢氧化钠的性质,要结合氢氧化钠的主要化学性质进行回答,平时的学习中要注意掌握主要物质的性质,加强知识的储备.

练习册系列答案
相关题目
(1)某校研究性学习小组欲配制1000g溶质质量分数为15%的氢氧化钠溶液.需氢氧化钠固体________g,水________mL(水的密度是1g/cm3);称量氢氧化钠时________(填“能”或“不能”)放在纸上称量.
(2)甲乙丙丁四位同学在探究碱溶液与酚酞作用的实验时,发现了一个意外现象:氢氧化钠溶液滴入酚酞试液,溶液变成了红色,一会儿红色就消失了.
【猜想】:
甲:可能是酚酞变质的缘故;
乙:可能是氢氧化钠溶液与空气中二氧化碳反应的缘故;
丙:可能是酚酞与空气中氧气反应,使红色消失的缘故;
丁:可能与氢氧化钠溶液质量分数大小有关.
【理论分析】:
①甲同学刚提出自己的猜想,就遭到其余三位同学的否定,三位同学的理由是________.
②乙同学的猜想也不正确,理由是________.
【实验设计】:
③为证实丙同学的猜想,还需作如下实验,请完成下表.
| 实验步骤 | 设计这一步骤的目的 |
| 1.用煮沸过的蒸馏水配制氢氧化钠溶液. | |
| 2.在氢氧化钠溶液中滴入酚酞,并在上方滴一些植物油. |
实验方法:观察到的现象和结论;
(3)质量分数小的溶液中红色不消失,质量分数大的溶液中红色会消失,则证明
________.
方案二:将滴有酚酞试液的质量分数大的氢氧化钠溶液加水稀释观察到的现象和结论:________.
(4)(8分)该校研究性学习小组向上述所配制的15%的氢氧化钠溶液中滴加稀盐酸,有气泡产生,由此可知所用的NaOH固体已变质.写出氢氧化钠在空气中变质的化学方程式________;所以氢氧化钠应该________保存.(2分)
【提出问题】:所用的NaOH变质程度怎样?
【设计方案】:先称取21.2g 的NaOH样品(杂质为Na2CO3),配成溶液,然后向溶液中逐滴加入一定质量分数的稀硫酸直至过量,根据生成CO2的质量计算出Na2CO3的质量,从而进一步确定样品中NaOH的质量分数.
【进行实验】:实验测得加入稀硫酸的质量与产生CO2气体的质量关系如下图所示.
【数据处理】:写出以下计算过程:
(5)该样品中NaOH的质量分数为多少?

【反思与交流】:①从图中0~A点说明:在NaOH 与Na2CO3的混合溶液中,加入稀硫酸,首先反应的物质是________;②根据反应方程式分析,NaOH部分变质或全部变质,与没有变质的NaOH相比,中和反应时消耗稀硫酸的量________(填“相等”或“大于”或“小于”.(2分)