网址:http://m.1010jiajiao.com/timu_id_78996[举报]
第Ⅰ卷(66分)
一、选择题(本题共10分),每小题2分,只有一个正确选项
题 号
1
2
3
4
5
答 案
A
C
D
A
B
二、选择题(本题共36分),每小题3分,只有一个正确选项。
题号
6
7
8
9
10
11
12
13
14
15
16
17
答案
C
A
C
A
B
B
D
D
B
D
C
D
三、选择题(本题共20分),每小题4分,每小题有一个或两个正确选项。只有一个正确选项的,多选不给分;有两个正确选项的,选对一个给2分,选错一个该小题不给分。
题 号
18
19
20
21
22
答 案
BD
AD
BC
AC
CD
第二卷(共84分)
四、(本题共24分)
23.(共8分)
(1)三角锥形, (各1分,共2分)
(各1分,共2分)
(2)第三周期IIIA族,2Al + 2OH- + 2H2O → 2AlO2- + 3H2↑(各1分,共2分)
(3)N,HNO3 + NaHCO3 → NaNO3 + H2O +CO2↑(各1分,共2分)
(4)强(或弱),M是氟元素,非金属性比氯强(或M是硫元素,非金属性比氯弱)(各1分,共2分)
24.(共8分)
(1)CuI、I2(2分) (2)2Cu+I2 →2CuI↓(2分)
(3)>,高(2分) (4)a c(2分)(各1分,错选、多选不得分)
25.(共8分)
(1)0.075mol/L?min(1分)
(2)放热, CO(g)+2H2(g) → CH3OH(g) +91KJ, 不能(各1分,共3分)
(3)K = ,减小;(各1分,共2分) (4)c(2分)
26.(共12分)
(1)bc(2分) (2) 吸收多余的SO2,防止污染环境(1分)
(3)②(1分),将②加在A和B之间(1分)
(4)SO2+ Na2O2→ Na2SO4(2分)
(5)不合理(1分),如果固体中还有未反应的Na2O2,也能氧化亚硫酸钠为硫酸钠。(2分)
(6)acd(2分)
27.(共12分)
(1)Fe(OH)3 (1分) (2)3Cu + 2HNO3 + 3H2SO4 →3CuSO4 + 2NO↑+ 4H2O(2分)
(3)
(5)①方案二(1分) ②Cu2+的蓝色对检验有干扰(2分)
(6)4NO + 3O2 +H2O → 4HNO3(2分)。
28.(共8分)
(1) (2分)
(2分)
(2) (各1分,共3分)
(各1分,共3分)
(3) (各1分,共2分)
(各1分,共2分)
(4) (1分)
(1分)
29.(共12分)
(1) ,
, (各1分,共2分)
(各1分,共2分)
(2)取代,氧化,消除(或消去)(各1分,共3分)
(3) ,(2分)
,(2分)
 (2分)
(2分)
(4)C与G(1分)
(5) (2分)
(2分)
30.(共6分)
(1)0.01 mol(2分) (2)20%(2分) (3)0.1mol/L(2分)
31.(共10分)
(1)
(3)①3:10 (2分) ② y = (3分)
本资料由《七彩教育网》www.7caiedu.cn 提供!
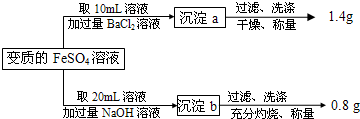
请计算(忽略Fe2+、Fe3+的水解):
(1)20mL变质的FeSO4溶液中,铁元素的总的物质的量为
(2)计算原溶液中Fe2+被氧化的百分率;
(3)原溶液中硫酸的物质的量浓度为

(1)为处理废铁屑表面的油污,用10%Na2CO3溶液清洗,请用离子方程式表示Na2CO3溶液呈碱性的原因:______.
(2)步骤1中采用倾析法分离出铁屑,下列适合用倾析法的有______:
A.沉淀的颗粒较大 B.沉淀容易沉降 C.沉淀呈胶状 D.沉淀呈絮状
(3)步骤2中铁屑过量的目的是(用离子方程式表示):______.步骤2中溶液趁热过滤的原因是______.
(4)步骤3中,加入(NH4)2SO4固体后,应加热到______时,停止加热.需经过的实验操作包括:______、______、减压过滤(或抽滤)等得到较为______的晶体.
(5)抽滤装置的仪器有:______、______、安全瓶、抽气泵组成.
(6)产品中Fe2+的定量分析:
制得的摩尔盐样品中往往含有极少量的Fe3+.为了测定摩尔盐产品中Fe2+的含量,一般采用在酸性下用KMnO4标准液滴定的方法.
称取4.0g的摩尔盐样品,溶于水,并加入适量稀硫酸.用0.2mo1/L KMnO4溶液滴定,当溶液中Fe2+ 全部被氧化时,消耗KMnO4溶液体积 10.00mL.
①请完成滴定过程中发生的离子方程式:
______Fe2++______MnO4-+______=______Mn2++______Fe3++______H2O
②本实验的指示剂______.
A.酚酞 B.甲基橙 C.石蕊 D.不需要
③KMnO4溶液置于______(酸式、碱式)滴定管中
④终点颜色的变化:______.
⑤产品中Fe2+的质量分数为______.
(7)在25℃时,相同物质的量浓度的(NH4)2 CO3、(NH4)2SO4、摩尔盐三种盐溶液a,b,c,其铵根离子浓度由小到大的排列顺序为:______.(用a,b,c回答)
查看习题详情和答案>>
绿矾(FeSO4·7H2O)、硫酸亚铁铵(FeSO4·(NH4 )2SO4·6H2O)是重要的化学化工试剂。工业上常利用机械加工行业产生的废铁屑为原料制备。
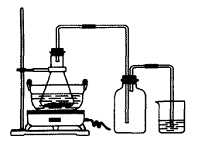
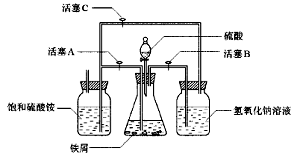
图Ⅰ 图Ⅱ
请回答下列问题:
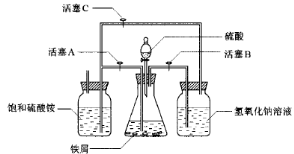
(1)图Ⅰ用于制备绿矾。其中锥形瓶中盛放的药品或原料是__________,集气瓶的作用是__________;烧杯中主要发生:①CuSO4+H2S=CuS↓+H2SO4 ②4CuSO4+PH3+4H2O=H3PO4+4H2SO4+4Cu↓,则烧杯中盛放的试剂是___ ___,其作用是_______________。
(2)图Ⅱ用于制备硫酸亚铁铵。在0~60℃的温度范围内,硫酸亚铁铵在水中的溶解度比硫酸铵、硫酸亚铁的溶解度小,冷却混合液至室温便析出硫酸亚铁铵。具体操作:①打开活塞____________,关闭活塞_________,从分液漏斗滴入6 mol·L-1 H2SO4到250 mL锥形瓶,充分反应。②待锥形瓶中的铁屑快反应完时,关闭活塞________,打开活塞________。③放置一段时间,试剂瓶底部将结晶出硫酸亚铁铵。
(3)在制备硫酸亚铁的过程中,理论上控制铁过量或酸过量均有利于防止Fe2+被氧化。设计两个实验:实验一,控制酸过量;实验二,控制铁过量;其余步骤同,制得硫酸亚铁铵,并对产品质量进行检测。检测结果如下:
| 序号 | 反应物用量 | 产品质量 |
| 1 | n(H2SO4):n(Fe)>1:1 | 介于Ⅰ级~Ⅱ级之间 |
| 2 | n(H2SO4):n(Fe)<1:1 | 优于Ⅰ级 |
已知产品质量标准:Fe3+的质量分数等于0.005%,产品质量定为Ⅰ级;Fe3+的质量分数等于0.01%,产品质量定为Ⅱ级,从实验结果中,可得出制备硫酸亚铁溶液时,反应控制___________过量为最佳。
查看习题详情和答案>>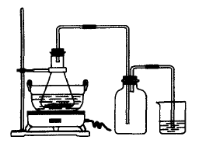
图Ⅰ 图Ⅱ
请回答下列问题:
(1)图Ⅰ用于制备绿矾。其中锥形瓶中盛放的药品或原料是__________,集气瓶的作用是__________;烧杯中主要发生:①CuSO4+H2S=CuS↓+H2SO4②4CuSO4+PH3+4H2O=H3PO4+4H2SO4+4Cu↓,则烧杯中盛放的试剂是___ ___,其作用是_______________。
(2)图Ⅱ用于制备硫酸亚铁铵。在0~60℃的温度范围内,硫酸亚铁铵在水中的溶解度比硫酸铵、硫酸亚铁的溶解度小,冷却混合液至室温便析出硫酸亚铁铵。具体操作:①打开活塞____________,关闭活塞_________,从分液漏斗滴入6 mol·L-1 H2SO4到250 mL锥形瓶,充分反应。②待锥形瓶中的铁屑快反应完时,关闭活塞________,打开活塞________。③放置一段时间,试剂瓶底部将结晶出硫酸亚铁铵。
(3)在制备硫酸亚铁的过程中,理论上控制铁过量或酸过量均有利于防止Fe2+被氧化。设计两个实验:实验一,控制酸过量;实验二,控制铁过量;其余步骤同,制得硫酸亚铁铵,并对产品质量进行检测。检测结果如下:
| 序号 | 反应物用量 | 产品质量 |
| 1 | n(H2SO4):n(Fe)>1:1 | 介于Ⅰ级~Ⅱ级之间 |
| 2 | n(H2SO4):n(Fe)<1:1 | 优于Ⅰ级 |
方法1、用下图所示的流程进行分离,同时获得硫酸亚铁晶体和铜粉.
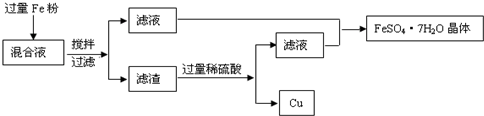
请回答:
(1)由滤液制取FeSO4?7H2O晶体要经过
(2)用100mL的混合液制取FeSO4?7H2O晶体,制得的晶体质量至少
方法2、用纸层析方法进行分离,实验步骤如下:

①点样:如右图所示,在滤纸条末端约2cm处用铅笔画一个小圆点作为原点.
在原点处滴一滴Fe2(SO4)3和CuSO4的混合溶液.晾干后再滴,重复3次,要求留下斑点的直径小于0.5cm.将滤纸条用大头针固定在橡胶塞下面.
②展开:在大试管中加入9mL丙酮和1mL 3mol?L-1硫酸,混合均匀.把滤纸末端浸入溶剂中约0.5cm,注意不要让试样点接触展开剂.塞紧橡胶塞,将大试管垂直静置.
③显色:待溶剂扩散到滤纸上端时,取下滤纸,放在盛有浓氨水的试剂瓶瓶口上方,用氨气熏.请回答:
(3)硫酸的作用是
(4)氨熏后红棕色出现在滤纸上端,其原因是