网址:http://m.1010jiajiao.com/timu_id_76188[举报]
一、选择题:1.B 2. B 3. C 4.C 5. A 6.A 7.D 8. C 9. B 10. A
11.B 12. D 13. C 14. C 15. B
二、选择题:16. C 17. C 18. B 19. AC 20. D 21. ABD 22. BD
23.(12分) (1)实物连结如右图(4分)
(2)9.0 10 (每空2分) (3) 9.0 11 (每空2分)
24.(15分)
-----理科综合.files/image205.jpg) 解:(1)从A到B的过程中,人与雪橇损失的机械能为:
解:(1)从A到B的过程中,人与雪橇损失的机械能为:
-----理科综合.files/image207.gif)
代入数据解得:-----理科综合.files/image209.gif)
(2)人与雪橇在BC段做减速运动的加速度大小:
-----理科综合.files/image211.gif)
根据牛顿第二定律:-----理科综合.files/image213.gif)
解得:-----理科综合.files/image215.gif)
由动能定理得:-----理科综合.files/image217.gif)
代入数据解得;-----理科综合.files/image219.gif)
25.(18分)解:(1)小球从M到N有-----理科综合.files/image221.gif)
解得-----理科综合.files/image223.gif)
(2)小球从M点到达N点所用时间-----理科综合.files/image225.gif)
小球从N点经过-----理科综合.files/image227.gif) 个圆周,到达P点,所以
个圆周,到达P点,所以-----理科综合.files/image229.gif)
小球从P点到D点的位移-----理科综合.files/image231.gif)
-----理科综合.files/image233.jpg) 小球从P点到D点的时间为
小球从P点到D点的时间为-----理科综合.files/image235.gif)
所以:时间-----理科综合.files/image237.gif)
(或-----理科综合.files/image239.gif) )
)
(3)小球运动一个周期的轨迹如图所示
小球的运动周期为-----理科综合.files/image241.gif) (或
(或-----理科综合.files/image243.gif) )
)
26.(14分)
(1)♂aaBb×♀Aabb (2分) (2)aaBB、AAbb(2分)
(3)①选取正常植株的花粉,进行花药离体培养,得到单倍幼苗;(2分)
②用适宜浓度的秋水仙素溶液处理单倍体玉米幼苗,得到纯合体二倍玉米植株,表现型为正常珠、雄珠、雌珠。(4分)
③选取多珠雌珠玉米和雄珠玉米分别杂交;若杂交后只有正常珠,则亲本为符合生产要求的纯合体雌珠和雄珠;若后代有雌珠和雄珠,则亲本为不符合要求的纯合体雌珠和雄珠。(4分)
27.(19分)
I.(1)胰岛A细胞(1分) [b]胰高血糖素(1分) [a]胰岛素(1分)
血糖的转化与利用(2分) 抑制非糖物质转化为血糖和肝糖原的分解(2分)
(2)反馈调节(2分)
(3)细胞膜上的受体蛋白不正常(a激素不能与受体结合或控制细胞膜上的受体蛋白的基因发生突变所致)(2分)
II.(1)(在光照强度为零时)小球藻呼吸作用吸收的氧气量(2分)
(2)呼吸作用吸收的氧气量等于光合作用产生的氧气量(2分)
(3)光照强度(2分)
(4)B试管中缺少镁元素,影响叶绿素的正常合成,其光合作用速率就比A试管低。(2分)
28.(14分)
(1)-----理科综合.files/image245.gif) (1分)
(1分)
-----理科综合.files/image247.gif) (1分)
(1分)
(2)①-----理科综合.files/image116.gif) (1分)
(1分)-----理科综合.files/image118.gif) (1分)(顺序可以颠倒)
(1分)(顺序可以颠倒)
②取适量滤液乙于蒸发皿中加热蒸发至干,将所得固体转移到试管中,塞上带导管的橡皮塞,并将导管插入澄清饱和石灰水,加热,一段时间后,若澄清饱和石灰水变混浊,则说明滤液乙中含有-----理科综合.files/image118.gif) ;另取适量滤液乙于试管中,加入足量的2mol?L-1
;另取适量滤液乙于试管中,加入足量的2mol?L-1-----理科综合.files/image251.gif) 溶液,将产生的沉淀过滤,洗涤后,再加入适量1 mol?L-盐酸,若有气泡产生,则滤液乙中含有
溶液,将产生的沉淀过滤,洗涤后,再加入适量1 mol?L-盐酸,若有气泡产生,则滤液乙中含有-----理科综合.files/image116.gif) 。(3分,其它合理答案也给分)
。(3分,其它合理答案也给分)
(3)-----理科综合.files/image253.gif) 或
或-----理科综合.files/image255.gif) (2分)
(2分)
(4)
-----理科综合.files/image257.gif)
(每个离子方程式1分,共3分)
②图像如下:(2分)
-----理科综合.files/image259.jpg)
29.(12分)(1)-----理科综合.files/image261.gif) ,
,-----理科综合.files/image263.gif) 1分) (2)硫酸,硫酸铵(亚硫酸钠)(1分,其它合理答案也给分)
1分) (2)硫酸,硫酸铵(亚硫酸钠)(1分,其它合理答案也给分)
(3)粗铜(1分) -----理科综合.files/image265.gif) (1分)
(1分)
(4)-----理科综合.files/image267.gif) (2分) 将
(2分) 将-----理科综合.files/image141.gif) 氧化成
氧化成-----理科综合.files/image165.gif) (2分)
(2分) -----理科综合.files/image141.gif) (1分) 否(1分) 根据溶度积,当溶液pH为7~8时,溶液A中
(1分) 否(1分) 根据溶度积,当溶液pH为7~8时,溶液A中-----理科综合.files/image272.gif) 同时生成沉淀而被除去(2分)
同时生成沉淀而被除去(2分)
-----理科综合.files/image274.jpg) 30.(16分)(1)
30.(16分)(1)-----理科综合.files/image276.gif) (2分); 取反应后的溶液少许于洁净的试管中,滴加氯化钡溶液,若有白色沉淀生成,证明有
(2分); 取反应后的溶液少许于洁净的试管中,滴加氯化钡溶液,若有白色沉淀生成,证明有-----理科综合.files/image278.gif) 存在。(或取反应后的溶液少许于洁净的试管中,滴加足量硝酸钡溶液,过滤,在滤液中滴加硝酸银溶液,若有白色沉淀生成证明有
存在。(或取反应后的溶液少许于洁净的试管中,滴加足量硝酸钡溶液,过滤,在滤液中滴加硝酸银溶液,若有白色沉淀生成证明有-----理科综合.files/image280.gif) 存在)(3分)
存在)(3分)
(2)防倒吸(2分) ①(2分)
(3) B、C(1分)
(4)⑤ (2分)品红褪色,加热不复原,说明氯气过量;品红褪色,加热又复原,说明二氧化硫过量。(2分)
31.(8分)【化学―化学与技术】
(1)2-----理科综合.files/image282.gif) (1分)
(1分)
-----理科综合.files/image284.gif) (1分)
(1分)
(反应不写水不扣分)
(2)常压、400―
(3)取少许滤液滴加到盐酸中产生气泡(2分)
(4)a d (2分)
32.(8分)【化学―物质结构与性质】
(1)⑨;分子晶体
(2)< 、>
(3)②>⑤>⑧
(4)-----理科综合.files/image286.gif)
-----理科综合.files/image288.gif) 与分子形成氢键且发生化学反应
与分子形成氢键且发生化学反应
(5)12; 1:2 (该题目每空1分)
33.(8分)【化学―有机化学基础】
(1)加成反应或还原反应(1分) 消去反应(1分)
-----理科综合.files/image290.jpg) (2)HOOCC
(2)HOOCC-----理科综合.files/image292.gif) CCOOH(1分)
CCOOH(1分)
-----理科综合.files/image294.jpg)
34.(8分)(1)蛋白酶 蛋白酶和脂肪酸 加酶和适当提高温度 因为高温使酶失活
(2)固定化酶 (3)平板划线法 (或稀释涂布平板法) 纤维素 (4)萃取法、蒸馏法、压榨法(任选两种)
35.(8分)
(1)目的基因 显微注射法
通过设备检测,发出明亮的绿色荧光细胞即为转基因体细胞 胚胎分割
(2)标记基因 为了鉴定受体细胞中是否含有目的基因
(3)GFD基因(绿色荧光蛋白基因)
预期蛋白质功能→预期蛋白质结构→推测氨基酸序列→推知基因的核苷酸序列→修饰(合成)相应基因→表达出相应蛋白质
36.(8分)【物理―物理3―3】
解:(1)一个分子的直径-----理科综合.files/image296.gif)
由题意得-----理科综合.files/image298.gif)
解得:-----理科综合.files/image300.gif)
(2)① a→b 过程
②理想气体由c到d,温度升高,内能增加;体积增大,对外做功;由热力学第一定律可知气体吸热。
37.(8分)【物理―物理3―4】
解:由图知:入射角-----理科综合.files/image302.gif) 折射角
折射角-----理科综合.files/image304.gif)
-----理科综合.files/image306.gif)
(2)若发生全反射,入射角C应满足
-----理科综合.files/image308.gif)
C=45°
亮斑半径-----理科综合.files/image310.gif)
亮斑面积-----理科综合.files/image312.gif)
38.(8分)【物理―物理3―5】
解:(1)-----理科综合.files/image314.gif)
(2)用-----理科综合.files/image316.gif) 分别表示中子(
分别表示中子(-----理科综合.files/image318.gif) )、氦核(
)、氦核(-----理科综合.files/image320.gif) )和氚核(
)和氚核(-----理科综合.files/image322.gif) )的质量,由动量守恒定律得
)的质量,由动量守恒定律得-----理科综合.files/image324.gif)
代入数值,得-----理科综合.files/image326.gif)
即反应后生成的氚核的速度大小为-----理科综合.files/image328.gif)
方向与反应前中子的速度方向相反
工业上以黄铜矿为原料,采用火法熔炼工艺生产铜。
(1)该工艺的中间过程会发生反应:![]() ,反应的氧化剂是_____________________。
,反应的氧化剂是_____________________。
(2)尾气中的SO2经处理可得到有价值的化学品,写出其中1种酸和1种盐的名称
____________________________。
(3)黄铜矿熔炼后得到的粗铜含少量Fe、Zn、Ag、Au等金属杂质,需进一步采用电解法精制。在精炼铜时,阳极材料是________,阴极电极反应式是_____________________。
(4)在精炼铜的过程中,电解液中![]() 逐渐下降,
逐渐下降,![]() 、
、![]() 会逐渐增人,所以需定时除去其中的
会逐渐增人,所以需定时除去其中的![]() 、
、![]() 。下表为几种物质的溶度积。
。下表为几种物质的溶度积。
| 物质 |
|
|
|
|
| 溶度积 |
|
|
|
|
甲同学设计了如下除杂方案:
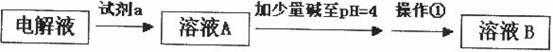
试剂a是__________,其目的是____________________________________;根据溶度积该方
案能够除去的杂质金属阳离子是____________。
乙同学在查阅资料时发现,“工业原料氯化铵中含杂质氯化铁,使其溶入水,再加入氨水
调节pH至7~8,可使![]() 生成
生成![]() 。沉淀而除去。”乙同学认为甲同学的方案中也
。沉淀而除去。”乙同学认为甲同学的方案中也
应该将溶液pH调至7~8。你认为乙同学的建议是否正确?________(填“是”或“否”),
理由是___________________________________________________________。
查看习题详情和答案>>工业上以黄铜矿为原料,采用火法熔炼工艺生产粗钢。
(1)该工艺的中间过程会发生反应:2Cu2O+Cu2S 6Cu+SO2↑,反应的氧化剂是 。
6Cu+SO2↑,反应的氧化剂是 。
(2)火法熔炼的粗铜含杂质较多。某化学研究性学习小组在实验室条件下用CuSO4溶液作电解液来实现粗铜的提纯,并对电解后溶液进行净化除杂和含量测定。
实验一 粗铜的提纯粗铜中含有少量的锌、铁、银、金等金属和少量矿物杂质(与酸不反应),电解时粗铜应与电源的 极相连,阴极上的电极反应式为 。
实验二 电解后溶液的净化除杂在精炼铜的过程中,电解液中c(Cu2+)逐渐下降,c(Fe2+)、c(Zn2+)会逐渐增大,所以需定时除去其中的Fe2+、Zn2+。甲同学参考下表的数据,设计了如下方案:
试剂a是 (填化学式),其目的是 ;该方案能够除去的杂质离子是 (填离子符号)。
实验三 电解后溶液离子含量的测定
乙同学设计了如下方案: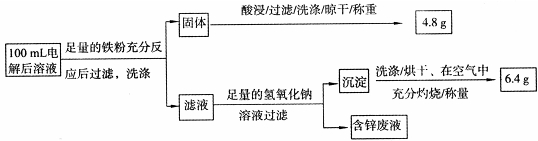
则100mL溶液中Cu2+的浓度为 mol·L-1,Fe2+的浓度为 mol·L-1。
(1)该工艺的中间过程会发生反应:2Cu2O+Cu2S
 6Cu+SO2↑,反应的氧化剂是 。
6Cu+SO2↑,反应的氧化剂是 。(2)火法熔炼的粗铜含杂质较多。某化学研究性学习小组在实验室条件下用CuSO4溶液作电解液来实现粗铜的提纯,并对电解后溶液进行净化除杂和含量测定。
实验一 粗铜的提纯粗铜中含有少量的锌、铁、银、金等金属和少量矿物杂质(与酸不反应),电解时粗铜应与电源的 极相连,阴极上的电极反应式为 。
实验二 电解后溶液的净化除杂在精炼铜的过程中,电解液中c(Cu2+)逐渐下降,c(Fe2+)、c(Zn2+)会逐渐增大,所以需定时除去其中的Fe2+、Zn2+。甲同学参考下表的数据,设计了如下方案:

试剂a是 (填化学式),其目的是 ;该方案能够除去的杂质离子是 (填离子符号)。
实验三 电解后溶液离子含量的测定
乙同学设计了如下方案:
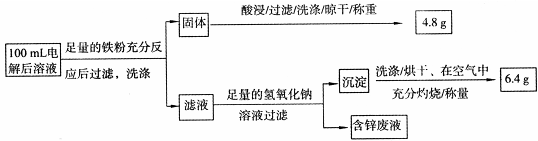
则100mL溶液中Cu2+的浓度为 mol·L-1,Fe2+的浓度为 mol·L-1。
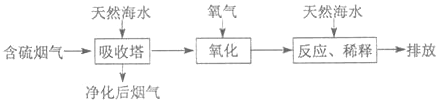
(1)天然海水呈碱性,写出SO2与OH-反应的离子方程式
(2)天然海水吸收了含硫烟气后会溶有H2SO3分子,使用氧气将其氧化的化学原理是
(3)为了测定炉气中SO2的体积百分含量,把500mL的炉气通入20mL 0.05mol/L的高锰酸钾溶液中,恰好使紫色刚好褪去.请回答:
①配平方程式:
②测定结果炉气中SO2的含量为
(4)已知工业上利用可逆反应2SO2+O2
| 加热 | △ |
A.当单位时间内消耗2mol SO2的同时生成2mol SO3,说明该反应达到平衡
B.升高温度,可以增大正反应速率
C.恒容,通入氩气增大压强,促使平衡向右移动
D.工业上通过鼓入大量的空气而提高SO2的转化率
(5)某科研小组利用SO2、O2和稀H2SO4设计成原电池,该电池的负极反应为:
2Cu2S(s)+3O2(g)=2Cu2O(s)十2SO2(g)△H=-768.2KJ?mol-1
2Cu2O(s)+Cu2S(s)=6Cu(s)+SO2(g)△H=+116.0KJ?mol-1
反应Cu2S(s)+O2(g)=2Cu(s)+SO2(g)的△H=
在上述工业生产过程中产生的SO2气体直接排放会污染大气.工业上常用氨水吸收SO2,反应的化学方程式为
Ⅱ大气污染的另一个重要问题是臭氧层的破坏.为妥善处理氯甲烷生产企业的副产物CCl4,以减少其对臭氧层的破坏.化学家研究在催化条件下,通过下列反应,使CCl4转化为重要的化工原料氯仿(CHCl3).CCl4(g)+H2(g)
| 催化剂 |
| △ |
如果不考虑反应过程中的副反应,在一个密闭容器中发生上述反应,该反应达到平衡后,测得下表中的数据.
| 实验序号 | 温度℃ | 初始CCl4浓度(mol?L-1) | 初始H2浓度(mol?L-1) | CCl4的转化率 |
| 1 | 110 | 0.8 | 1.2 | a |
| 2 | 110 | 1 | 1 | 50% |
| 3 | 120 | 1 | 2 | x |
| 4 | 120 | 1 | 4 |
(1)实验1中,CCl4的转化率a
(2)在实验2的平衡体系中,再加入0.5mol?L-1CCl4和1mol?L-1HCl,平衡将向
(3)120℃,在相同条件的密闭容器中,分别进行实验3、4,测得CCl4的转化率(x)和生成物中CHCl3的体积分数(y)随时间(t)的变化关系如图(图中实线是CCl4转化率变化曲线,虚线是产物中CHCl3的体积分数变化曲线).
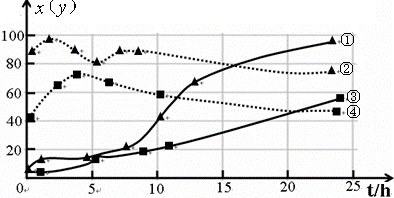
图中的四条线中,表示H2起始浓度为2mol?L-1实验中CCl4的转化率(x)变化曲线是