网址:http://m.1010jiajiao.com/timu_id_66730[举报]
一、选择题
题号
1
2
3
4
5
6
7
8
答案
C
D
B
C
D
C
A
B
二、非选择题
.files/image014.jpg) 26. (1)HClO4
(2分)
26. (1)HClO4
(2分)
(2) (2分)离子键和非极性共价键(2分)
(3) Cl2+2OH-==Cl-+ClO-+H2O (3分) (4) 2Cl-+2H2O电解Cl2+H2+2OH- (3分)
(5) 2HCl(g)==H2(g)+Cl2(g);DH=+184.6kJ×mol-1 (3分)
27.(1)沸腾炉(2分) H2O2 (2分)O=C=O(2分)
(2)4FeS2+11O2高温2Fe2O3+8SO2 (2分) (3) C+H2O高温CO+H2 (2分)
(4) bh (2分) (5) CO2 +2NH3 高压CO(NH2)2+H2O (3分)
28.(1)检查装置气密性(2分)
(2)药品:碱石灰 (2分) 作用:吸收NH4Cl 受热分解产生的HCl(3分)
(3)防止倒吸(2分) (4)D (2分)
(5)A中石蕊变红且不褪色说明生成了HCl;(2分)D中酚酞变红说明生成了NH3
29.(1)①②④(3分) (2)羧基(2分)
(3)CH3CH2CH2CH=CH2+Br2 ®CH3CH2CH2CHBrCH2Br (3分)
(4) CH3CH(CH3)CH2COOH CH3CH2CH(CH3)COOH (4分)
(5) (3分)
CH3CH2CH2CH2CHO+2Ag(NH3)2OH.files/image016.jpg) CH3CH2CH2CH2COONH4+3NH3+2Ag¯+H2O
CH3CH2CH2CH2COONH4+3NH3+2Ag¯+H2O
 短周期元素A、B、C、D原子序数依次增大,且C元素最高价氧化物对应的水化物,能电离出电子数相等的阴、阳离子.A、C位于同一主族,A为非金属元素,B的最外层电子数是次外层的3倍,B、C的最外层电子数之和与D的最外层电子数相等.E单质是生活中常见金属,其制品在潮湿空气中易被腐蚀或损坏.
短周期元素A、B、C、D原子序数依次增大,且C元素最高价氧化物对应的水化物,能电离出电子数相等的阴、阳离子.A、C位于同一主族,A为非金属元素,B的最外层电子数是次外层的3倍,B、C的最外层电子数之和与D的最外层电子数相等.E单质是生活中常见金属,其制品在潮湿空气中易被腐蚀或损坏.请回答下列问题:
(1)C的最高价氧化物对应水化物电子式为
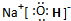
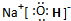
(2)由上述A、B、C、D四种元素中的三种组成某种盐,水溶液显碱性,是家用消毒剂的主要成分.将该盐溶液滴入KI淀粉溶液中,溶液变为蓝色,则反应的离子方程式为
(3)用石墨电极电解CD的饱和溶液,若反应后溶液的体积为200mL,测得pH为13,则阳极得到的气体的物质的量为
(4)E元素与D元素可形成ED2和ED3两种化合物,下列说法正确的是(填序号)
①保存ED2溶液时,需向溶液中加入少量E单质
②ED2只能通过置换反应生成,ED3只能通过化合反应生成
③铜片、碳棒和ED3溶液组成原电池,电子由铜片沿导线流向碳棒④向淀粉碘化钾溶液和苯酚溶液中分别滴加几滴ED3的浓溶液,原无色溶液都变成紫色
(5)25℃时,将pH=4.00的A元素与D元素形成化合物AD的水溶液稀释1.00×103倍,则稀释后溶液中各离子浓度必遵循的定量等式关系式是
(6)将一定量的D单质通入一定浓度的苛性钾溶液,两者恰好完全反应(已知反应过程放热),生成物中有三种含D元素的离子,其中两种离子的物质的量(n)与反应时间(t)的变化示意图如图所示.该苛性钾溶液中KOH的质量是
(1)D的最高价氧化物对应水化物名称为
(2)C2B2的电子式为
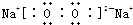
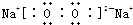
(3)由上述四种元素中的三种组成某种盐,水溶液显碱性,是家用消毒剂的主要成分.将该盐溶液滴入KI淀粉溶液中,溶液变为蓝色,则反应离子方程式为
(4)用石墨电极电解CD的饱和溶液,反应的离子方程式为
| ||
| ||
若反应后溶液的体积为200mL,测得pH为13,则阳极得到的气体质量为
(5)实验室欲检验CD溶液中所含的D-,操作方法和现象为
(1)化合物C2B2中含有的化学键类型为
(2)化合物CDB是家用消毒剂的主要成分,其水溶液显碱性.显碱性的原因用离子方程式表示为
(3)往CD溶液中滴加硝酸银溶液生成白色沉淀后,再滴加碘化钠溶液,可观察到的现象是
(1)D的最高价氧化物对应的水化物名称为_______________。
(2)G为由A、B、C三种元素组成的化合物,其电子式为_______________,其中含有的化学键类型为_______________。
(3)A单质与D单质反应可生成化合物E,E分子中的电子数与A元素和B元素组成的F分子中的电子数相等。写出F+D单质→E的化学方程式:_______________。
(4)由上述四种元素中的三种组成某种盐,其水溶液显碱性,常用作家用消毒液。将该盐溶液滴入KI淀粉溶液中,溶液变为蓝色,则反应的离子方程式为_________________________。
(5)用石墨电极电解质量分数为5.2%的G溶液1 L(密度为