摘要:A C (2)AlO2― + H+ + H2O = Al(OH)3↓4- + H+ = Al(OH)3↓+ H2O) SiO32―+ 2H+ + = H2SiO3↓(或SiO32―+ 2H+ + H2O = H4SiO4↓) (3)2CrO42-+2H+= Cr2O72-+H2O (4)蒸发浓缩.Na2SO4 (答Na2SO4•10H2O也给分).冷却结晶.过滤.Na2Cr2O7?2H2O (5)预热过滤装置(或用常压热过滤漏斗进行过滤).
网址:http://m.1010jiajiao.com/timu_id_577062[举报]
A、B、C、D四种短周期元素的原子序数依次增大,A元素的气态氢化物与A元素的最高价氧化物对应的水化物能反应生成盐;B、C、D同周期,它们的最高价氧化物对应的水化物两两之间都能反应生成盐和水,B和D可组成化合物BD,回答下列问题.
(1)B的最高价氧化物对应的水化物与C的氧化物在溶液中反应的离子方程式为:
(2)B、D的最高价氧化物对应的水化物在稀溶液中反应,若生成0.25mol水时放出Q kJ的热量,则该反应的热化学方程式为
(3)在BHCO3的水溶液中,c(B+)-c(H2CO3)=
(4)在一定条件下,将2molA2和3molH2在一固定体积的密闭容器中反应达到平衡状态,此时容器中混合气体的平均相对分子质量为15.5,则H2的转化率为
查看习题详情和答案>>
(1)B的最高价氧化物对应的水化物与C的氧化物在溶液中反应的离子方程式为:
Al(OH)3+OH-=AlO2-+2H2O
Al(OH)3+OH-=AlO2-+2H2O
.(2)B、D的最高价氧化物对应的水化物在稀溶液中反应,若生成0.25mol水时放出Q kJ的热量,则该反应的热化学方程式为
NaOH(aq)+HClO4(aq)=NaClO4(aq)+H2O(l)△H=-4QKJ/mol
NaOH(aq)+HClO4(aq)=NaClO4(aq)+H2O(l)△H=-4QKJ/mol
.(3)在BHCO3的水溶液中,c(B+)-c(H2CO3)=
c(Na+)-c(H2CO3)=C(HCO3-)+C(CO32-)
c(Na+)-c(H2CO3)=C(HCO3-)+C(CO32-)
.(4)在一定条件下,将2molA2和3molH2在一固定体积的密闭容器中反应达到平衡状态,此时容器中混合气体的平均相对分子质量为15.5,则H2的转化率为
50%
50%
.若平衡后,再按n(A2):n(H2):n(AH3)=3:3:2向该密闭容器中充入气体,当重新达到平衡后,A2在平衡混合气中的百分含量较原平衡小
小
(填“大”、“小”或“不变”).下表为元素周期表的一部分,请参照元素①~⑧在表中的位置,用化学用语回答下列问题:
(1)④、⑤、⑥的原子半径由大到小的顺序是
(2)②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是
(3)①、④、⑤、⑧中的某些元素可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的电子式: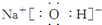 或
或 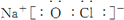
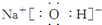 或
或 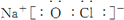 .
.
(4)由表中两种元素的原子按1:1组成的常见液态化合物的稀溶液易被催化分解,可使用的催化剂为
a.MnO2 b.FeCl3 c.Na2SO3 d.KMnO4
(5)写出⑥的最高价氧化物对应水化物的电离方程式
查看习题详情和答案>>
| 族 周期 |
ⅠA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
Na>Al>O
Na>Al>O
.(2)②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是
HNO3>H2CO3>H2SiO3
HNO3>H2CO3>H2SiO3
.(3)①、④、⑤、⑧中的某些元素可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的电子式:
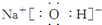 或
或 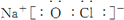
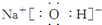 或
或 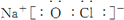
(4)由表中两种元素的原子按1:1组成的常见液态化合物的稀溶液易被催化分解,可使用的催化剂为
ab
ab
(填序号).a.MnO2 b.FeCl3 c.Na2SO3 d.KMnO4
(5)写出⑥的最高价氧化物对应水化物的电离方程式
AlO2-+H++H2O?Al(OH)3?Al3++3OH-
AlO2-+H++H2O?Al(OH)3?Al3++3OH-
.(2008?淮南一模)现有四瓶丢失标签的NaOH、Na2CO3、AlCl3、NH4HSO4溶液,为鉴别四瓶溶液,将四瓶溶液编号为A、B、C、D进行实验.实验过程和记录如下图所示(无关物质已经略去):
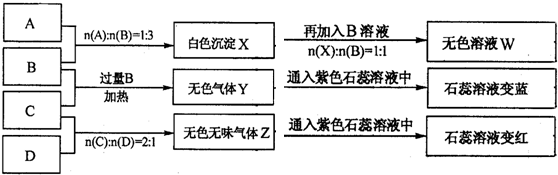
请回答:
(1)Y、Z的化学式分别为:Y
(2)D溶液pH
(3)等物质的量浓度的A、B、C、D溶液pH由大到小的顺序是
(4)请写出C与过量B反应(加热)的离子方程式
(5)若B、C的稀溶液混合后(不加热)溶液呈中性,则该溶液中离子浓度从大到小的顺序是
查看习题详情和答案>>

请回答:
(1)Y、Z的化学式分别为:Y
NH3
NH3
;ZCO2
CO2
.X与B反应的离子方程式为Al(OH)3+OH-=AlO2-+2H2O
Al(OH)3+OH-=AlO2-+2H2O
.(2)D溶液pH
大于
大于
(填“大于”、“小于”或“等于”),原因是(用离子方程式表示)CO32-+H2O?HCO3-+OH-
CO32-+H2O?HCO3-+OH-
.(3)等物质的量浓度的A、B、C、D溶液pH由大到小的顺序是
NaOH>Na2CO3>AlCl3>NH4HSO4
NaOH>Na2CO3>AlCl3>NH4HSO4
.(用化学式表示)(4)请写出C与过量B反应(加热)的离子方程式
NH4++H++2OH-
NH3↑+2H2O
| ||
NH4++H++2OH-
NH3↑+2H2O
.
| ||
(5)若B、C的稀溶液混合后(不加热)溶液呈中性,则该溶液中离子浓度从大到小的顺序是
c(Na+)>c(SO42-)>c(NH4+)>c(H+)=c(OH-)
c(Na+)>c(SO42-)>c(NH4+)>c(H+)=c(OH-)
.现有A、B、C、D四种物质,B、D的焰色反应均为黄色.C是一种强酸的酸式盐,将C加入BaCl2溶液有不溶于盐酸的白色沉淀生成,D晶体在干燥空气中容易逐渐失去结晶水变成白色粉末.对A、B、C、D进行下列实验,实验过程和记录如图所示(无关物质已略去),请回答:
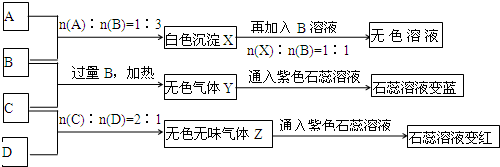
(1)X与B反应的离子方程式为
(2)D溶液pH值大于7,原因是(用离子方程式表示)
(3)写出C与过量B反应(加热)的离子方程式
(4)若B、C的稀溶液混合后(不加热)溶液呈中性,则该溶液中离子浓度从大到小的顺序
(5)Y在同主族的同类物质中分子稳定性最强
(6)若向三份足量的B的稀溶液中分别加入少量稀醋酸、稀硝酸、浓硫酸,均生成1molH2O时的反应热分别为△H1,△H2,△H3,则三者由大到小排序为:
查看习题详情和答案>>

(1)X与B反应的离子方程式为
Al(OH)3+OH-=AlO2-+2H2O
Al(OH)3+OH-=AlO2-+2H2O
.(2)D溶液pH值大于7,原因是(用离子方程式表示)
CO32-+H2O  HCO3-+OH-HCO3-+H2O?H2CO3+OH-
HCO3-+OH-HCO3-+H2O?H2CO3+OH-
 HCO3-+OH-HCO3-+H2O?H2CO3+OH-
HCO3-+OH-HCO3-+H2O?H2CO3+OH-CO32-+H2O  HCO3-+OH-HCO3-+H2O?H2CO3+OH-
HCO3-+OH-HCO3-+H2O?H2CO3+OH-
. HCO3-+OH-HCO3-+H2O?H2CO3+OH-
HCO3-+OH-HCO3-+H2O?H2CO3+OH-(3)写出C与过量B反应(加热)的离子方程式
NH4++H++2OH-
NH3↑+2H2O
| ||
NH4++H++2OH-
NH3↑+2H2O
.
| ||
(4)若B、C的稀溶液混合后(不加热)溶液呈中性,则该溶液中离子浓度从大到小的顺序
C(Na+)>C(SO42-)>C(NH4+)>C(H+)=C(OH-)
C(Na+)>C(SO42-)>C(NH4+)>C(H+)=C(OH-)
.(5)Y在同主族的同类物质中分子稳定性最强
是
是
,也是沸点最高的是
是
.(判断正误填“是“或“否“)(6)若向三份足量的B的稀溶液中分别加入少量稀醋酸、稀硝酸、浓硫酸,均生成1molH2O时的反应热分别为△H1,△H2,△H3,则三者由大到小排序为:
△H1>△H2>△H3
△H1>△H2>△H3
.下表是元素周期表的一部分,回答下列有关问题: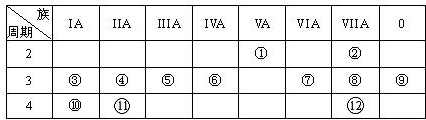
(1)写出下列元素符号:①
(2)画出原子的结构示意图:④
 ,⑧
,⑧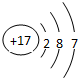
 ;
;
(3)在①~12元素中,金属性最强的元素是
(4)元素3、10、11的氢氧化物碱性由强到弱的顺序
(5)第三周期中有一种元素,其最高价氧化物的水化物与同周期其它元素最高价氧化物的水化物所属物质类型都不同,用离子方程式表示该水化物分别与烧碱溶液和稀硫酸的反应:
(6)与①和⑥都相邻的一种元素A,它有多种不同形态的单质,其中一种常用作原电池的电极,它与⑦的最高价氧化物的水化物浓溶液在加热时能反应,写出化学反应方程式:
查看习题详情和答案>>

(1)写出下列元素符号:①
N
N
,⑥Si
Si
,⑦S
S
.(2)画出原子的结构示意图:④




(3)在①~12元素中,金属性最强的元素是
钾
钾
,非金属性最强的元素是氟
氟
,最不活泼的元素是氩
氩
.(均填元素名称)(4)元素3、10、11的氢氧化物碱性由强到弱的顺序
KOH>Ca(OH)2>NaOH
KOH>Ca(OH)2>NaOH
;元素6、7、8的氢化物稳定性由弱到强的顺序SiH4<H2S<HCl
SiH4<H2S<HCl
(均用化学式填空)(5)第三周期中有一种元素,其最高价氧化物的水化物与同周期其它元素最高价氧化物的水化物所属物质类型都不同,用离子方程式表示该水化物分别与烧碱溶液和稀硫酸的反应:
Al(OH)3+OH-═AlO2-+2H2O
Al(OH)3+OH-═AlO2-+2H2O
;Al(OH)3+3H+═Al3++3H2O
Al(OH)3+3H+═Al3++3H2O
(6)与①和⑥都相邻的一种元素A,它有多种不同形态的单质,其中一种常用作原电池的电极,它与⑦的最高价氧化物的水化物浓溶液在加热时能反应,写出化学反应方程式:
C+2H2SO4(浓)
CO2↑+2SO2↑+2H2O
| ||
C+2H2SO4(浓)
CO2↑+2SO2↑+2H2O
.写出能验证⑦的非金属性强于A的化学反应的离子方程式:
| ||
2H++CO32-═CO2↑+H2O或H++HCO3-═CO2↑+H2O
2H++CO32-═CO2↑+H2O或H++HCO3-═CO2↑+H2O
.