摘要:A.Al3+ B.Al(OH)3 C.AlO2- D.Al3+ 和Al(OH)3
网址:http://m.1010jiajiao.com/timu_id_575663[举报]
A、B、C、D、E是中学化学常见单质,构成它们的元素的原子序数分别为a、b、c、d、е;且3(a+b)=2(a+c)=3(d-a);X、Y、Z、M、N、W、H、K是常见化合物,X是B和C的化合产物,它们之间有如下转化关系(图中反应物和产物中的H2O已略去):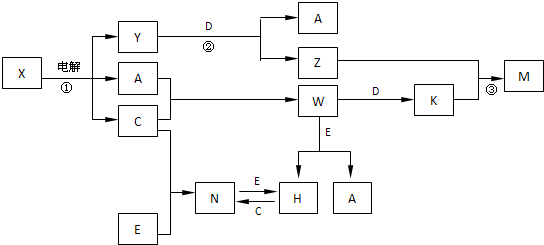
(1)Y的电子式为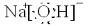
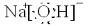 ,构成E单质的元素的原子结构示意图为:
,构成E单质的元素的原子结构示意图为: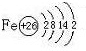
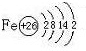 .
.
(2)反应③的离子方程式为
(3)E的氧化物与D在一定条件下反应的化学方程式为:
(4)已知常温下,1gA的单质与C的单质在点燃条件下完全反应,放出的热量为92.3kJ,写出W分解生成A和C的热化学方程式
(5)用离子方程式表示Z溶液显碱性的原因:
(6)固体N常温下即挥发,183℃升华,几乎溶于所有的有机溶剂和H2O中,据此判断N为
(7)25℃时,PH=5的W和N的水溶液中由H2O电离出来的H+离子浓度之比为
查看习题详情和答案>>

(1)Y的电子式为
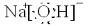
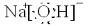
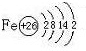
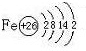
(2)反应③的离子方程式为
Al3++3AlO2-+6H2O=4Al(OH)3↓
Al3++3AlO2-+6H2O=4Al(OH)3↓
.(3)E的氧化物与D在一定条件下反应的化学方程式为:
Fe2O3+2Al
2Fe+Al2O3
| ||
Fe2O3+2Al
2Fe+Al2O3
,在实验室中,引发该反应的实验操作为
| ||
将铝粉与氧化铁粉末混合均匀,在混合物上方撒少量氯酸钾,插上一根镁条,并点燃镁条
将铝粉与氧化铁粉末混合均匀,在混合物上方撒少量氯酸钾,插上一根镁条,并点燃镁条
.(4)已知常温下,1gA的单质与C的单质在点燃条件下完全反应,放出的热量为92.3kJ,写出W分解生成A和C的热化学方程式
2HCl(g)═H2(g)+Cl2(g)△H=+184.6kJ/mol
2HCl(g)═H2(g)+Cl2(g)△H=+184.6kJ/mol
.(5)用离子方程式表示Z溶液显碱性的原因:
AlO2-+2H2O?Al(OH)3+OH-
AlO2-+2H2O?Al(OH)3+OH-
.(6)固体N常温下即挥发,183℃升华,几乎溶于所有的有机溶剂和H2O中,据此判断N为
分子
分子
晶体.(7)25℃时,PH=5的W和N的水溶液中由H2O电离出来的H+离子浓度之比为
1:104
1:104
.已知:⑴Al(OH)3的电离方程式为:AlO2-+H++H2O![]() Al(OH)3
Al(OH)3![]() Al3++3OH-;⑵无水AlCl3晶体的沸点为182.9℃,溶于水的电离方程式为:AlCl3=Al3++3Cl-;⑶PbSO4难溶于水,易溶于醋酸钠溶液,反应的化学方程式为:PbSO4+2CH3COONa=Na2SO4+(CH3COO)2Pb。下列关于Al(OH)3、AlCl3和(CH3COO)2Pb的说法中正确的是
Al3++3OH-;⑵无水AlCl3晶体的沸点为182.9℃,溶于水的电离方程式为:AlCl3=Al3++3Cl-;⑶PbSO4难溶于水,易溶于醋酸钠溶液,反应的化学方程式为:PbSO4+2CH3COONa=Na2SO4+(CH3COO)2Pb。下列关于Al(OH)3、AlCl3和(CH3COO)2Pb的说法中正确的是
A.均为强电解质 B.均为弱电解质
C.均为离子化合物 D.均为共价化合物
查看习题详情和答案>>欲使Al(OH)3全部转化为Al3+,最好加入下列试剂中的( )
欲使Al(OH)3全部转化为AlO2-,最好加入下列试剂中的( )
A.NaOH B.NH3.H2O C.HCl溶液 D.CO2和水
查看习题详情和答案>>
欲使Al(OH)3全部转化为Al3+,最好加入下列试剂中的( )
欲使Al(OH)3全部转化为AlO2-,最好加入下列试剂中的( )
A.NaOH B.NH3.H2O C.HCl溶液 D.CO2和水
查看习题详情和答案>>
用A、B、C、D、E和F表示含有10个电子的微粒(离子或分子),请回答:
(1)A离子为单核离子且A原子在所在周期中原子半径最大,A离子是
(2)C是由两种元素组成的分子,其水溶液呈碱性,其分子式是
(3)D是由两种元素组成的三原子分子,电子式是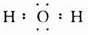
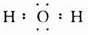
(4)向B中加入F先出现白色沉淀继续加入F沉淀溶解,写出该过程的离子方程式
(5)E+F→C+D写出该方程式
查看习题详情和答案>>
(1)A离子为单核离子且A原子在所在周期中原子半径最大,A离子是
Na+
Na+
(2)C是由两种元素组成的分子,其水溶液呈碱性,其分子式是
NH3
NH3
(3)D是由两种元素组成的三原子分子,电子式是
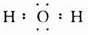
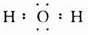
(4)向B中加入F先出现白色沉淀继续加入F沉淀溶解,写出该过程的离子方程式
Al3++3OH-=Al(OH)3↓Al(OH)3+OH-=AlO2-+H2O
Al3++3OH-=Al(OH)3↓Al(OH)3+OH-=AlO2-+H2O
(5)E+F→C+D写出该方程式
NH4++OH-=NH3+H2O
NH4++OH-=NH3+H2O
.