网址:http://m.1010jiajiao.com/timu_id_557370[举报]
选择题(1―10题每小题2分,11-25题每小题3分,共65分)
题目
1
2
3
4
5
6
7
8
9
10
11
12
13
答案
B
D
C
B
D
A
B
D
A
A
D
A
C
题目
14
15
16
17
18
19
20
21
22
23
24
25
答案
C
B
C
D
B
A
C
C
B
D
C
C
三、填空题(共35分,除注明分数外,其余每个给分点为1分)
26.(6分)(1)10+m 8 (2)28+n 36 (3)离子键 (4)

27.(9分)(1)Mg O (2)Na>Mg>C>O>H (3)Mg(OH)2<NaOH
(4)H2O2、Na2O2、O3、C(活性炭)等任意三个
(5)(2分)NaHCO3+H2O NaOH+H2CO3
NaOH+H2CO3
28.(7分)(1)Cu2+、Ba2+、Fe3+ (2)AlO2-、HCO3-、SO42-、Na+
29.(13分)(1)H2O2 MnO2
(2)2KMnO4+16HCl==2KCl+2MnCl2+5Cl2↑+8H2O 溶液由无色变橙色
(3)①CaO+H2O==Ca(OH)2,反应放热,NH3?H2O NH3↑+H2O
NH3↑+H2O
②用玻璃棒蘸取少许浓盐酸靠近收集NH3的烧瓶口,若产生白烟,说明烧瓶已收集满NH3,反之,则没有收集满或用湿润的红色石蕊试纸变蓝,则说明NH3已收集满,反之,则没有收集满
(4)①挤出胶头滴管中的水(1分),打开止水夹(1分),
极易溶解于水(1分)和其水溶液呈碱性(1分)
② (2分)
(2分)
下列物质的性质递变规律与化学键无关的是 ( )
A.还原性:Rb>K>Na>Li
B.沸点:CHI3>CHBr3>CHCl3>CHF3
C.硬度:金刚石>碳化硅>晶体硅
D.稳定性:H2O>H2S>H2Se>H2Te
查看习题详情和答案>>| A.还原性:Rb>K>Na>Li |
| B.沸点:CHI3>CHBr3>CHCl3>CHF3 |
| C.硬度:金刚石>碳化硅>晶体硅 |
| D.稳定性:H2O>H2S>H2Se>H2Te |
请回答下列问题:
(1)CO可以和很多过渡金属形成配合物,CO分子中C原子上有一对孤对电子,C、O原子都符合8电子稳定结构,CO分子里的共价键的类型按原子轨道的重叠方向分有
(2)第四周期元素的第一电离能随原子序数的增大,总趋势是逐渐增大的.但
31 |
30 |
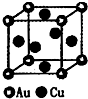
(3)如图是金与铜形成的金属互化物合金,它的化学式可表示为
(4)已知Ti3+可形成配位数为6的配合物;现有含钛的两种颜色的晶体,一种为紫色,另一为绿色,但相关实验证明,两种晶体 的组成皆为TiCl3?6H2O.为测定这两种晶体的化学式,设计了如下实验:
a.分别取等质量的两种晶体样品配成待测溶液;
b.分别向待测溶液中滴入AgNO3溶液,均产生白色沉淀;
c.沉淀完全后分别过滤得两份沉淀,经洗涤干燥后称量,发现原绿色晶体的水 溶液与AgNO3溶液反应得到的白色沉淀质量为紫色晶体的水溶液反应得到沉淀质量的
| 2 |
| 3 |
则绿色晶体配合物的化学式为
(5)二氧化钛作光催化剂能将居室污染物甲醛、苯等有害气体可转化为二氧化碳和水,达到无害化.有关甲醛、苯、二氧化碳及水说法正确的是
A.苯与B3N3H6互为等电子体
B.甲醛、苯和二氧化碳中碳原子均采用Sp2杂化
C.苯、二氧化碳是非极性分子,水和甲醛是极性分子
D.水的沸点比甲酸高得多,是因为水分子间形成了氢键.
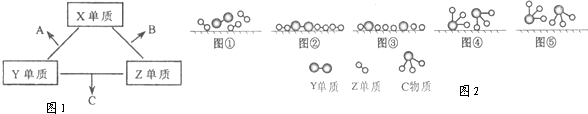
(1)X元素在周期表中的位置是
(2)分析同主族元素性质的递变规律,发现B、C物质沸点反常,这是因为它们
(3)C的电子式是
图①至⑤中表示在催化剂表面Z单质与Y单质中化学键断裂是
(4)在一定条件下,1L密闭容器中充入1mol Y单质和3mol Z单质进行反应,经过20min达到平衡时,Y单质的物质的量为0.8mol,用题中所给数据列出平衡常数表达式(不必计算结果),K=
(5)为幵发新能源,有关部门拟用甲醇(CH3OH)替代汽油作为公交车的燃料.写出由CO和Z单质在一定条件下生成甲醇的化学方程式
又知:4H2(g)+2CO(g)+3O2(g)=2CO2(g)+4H2O(g)△H=-1188.2kL/mol
H2O(g)=H2O(l)△H=-44.0kL/mol
请写出表达液态甲醇燃烧热的热化学方程式