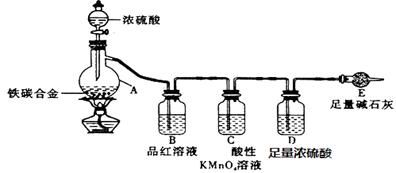
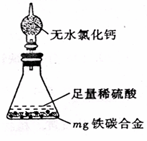
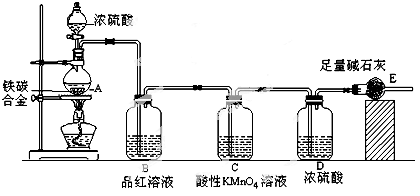
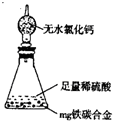
网址:http://m.1010jiajiao.com/timu_id_531543[举报]
化学参考答案:
6
7
8
9
10
11
12
13
C
C
C
B
B
A
A
D
26.(1) X H Y Na M Cl N O-----------各1分
H2 (g) + Cl2 (g) = 2HCl (g) ; △H = ?184.6 kJ?mol ?1 --------------------- 4分
(2) 电解
2NaCl + 2H2O ? 2NaOH + Cl2↑+ H2↑--------------------------------------------- 2分
B. NaCl C. NaClO3 --------------------------------------------------各1分
(3) 2ClO3- + 2H+ +HOOC-COOH = 2ClO2 + 2CO2 + 2H2O -------------------- 2分

物理参考答案:
题号
14
15
16
17
18
19
20
21
答案
C
BCD
AB
BD
B
BC
C
ABD
22 (6分) (1). C F A D
(10分)(2)①A、C、E ②C
23.(16分)解答:(1)由(b)图可知,木块所受到的滑动摩擦力Ff =3.12N (2分)
由Ff =μFN (1分)
得μ= =
= =
= =0.4
(1分)
=0.4
(1分)
(2)物体受重力G、支持力FN、拉力F和摩擦力Ff作用.将F分解为水平和竖直两方向,根据牛顿运动定律
Fcosθ-Ff=ma (2分)
Fsinθ +FN= mg (1分)
Ff =μFN (1分)
联立各式得F=4.5N (1分)
(3)全过程应用动能定理
WF+Wf=0 (2分)
WF=Fxcosθ (2分)
x= (2分)
(2分)
代入数据得Wf=-14.4J (1分)
24.(19分)解答:(7分)(1)30V
 (提示:见右图,离子在磁场中偏转90°,因此轨迹半径r=R=
(提示:见右图,离子在磁场中偏转90°,因此轨迹半径r=R= c
c ,可得U。)
,可得U。)
 (12分)(2)
(12分)(2) 可得r1=
可得r1= =
= 可得r2=
可得r2= =
=
25.(1)设子弹、小物块、长木板的质量分别为m0、M、m,子弹的初速度为v0,子弹击中小物块后二者的共同速度为v1,由动量守恒定律
m0 v0=(M+ m0) v1-------------------------------------------------------------------------------①
子弹击中小物块后物块的质量为M′,且M′= M+ m0.设当物块滑至第n块木板时,木板才开始运动
μ
其中μ1、μ2分别表示物块与木板间、木板与地面间的动摩擦因数.
由式解得n>4.3
即物块滑上第五块木板时,木板才开始在地面上滑动.
(2)设物块刚滑上第五块木板时的速度为v2,每块木板的长度为L,由动能定理
-μ
由①②式解得 v2=
物块在第五块木板表面做匀减速直线运动,木板做匀加速直线运动,设经历时间t,物块与木板能获得相同的速度v3,由动量定理
-μ
〔μ1 M′g-μ2(M′+m)〕t=m v3--------------------------------------------------------------⑥
由⑤⑥式解得v3=m/s-----------------------------------------------------------------------⑦
在此过程中,物块发生的位移为s1,由动能定理
-μ
解得s1=m<
即物块与木板获得m/s的共同速度,之后整体向前匀减速运动s2后静止.
由动能定理
-μ2 (M′+m)g s2=-(M′+m)v32 ------------------------------------------------------⑨
解得s2=m
所以物块总共发生的位移s=
解得s≈
本题共21分,其中①②③各3分,⑤⑥⑧⑨各2分,④⑦⑩⑾各1分。其他方法正确也给分。
生物参考答案
1.B 2.C 3.B 4.C 5.D
30.(20分)
(1)①不是(1分)
②是(1分) 取白化苗的离体组织进行植物组织培养,得到的后代全是白化苗(用基因检测的方法证实叶绿体的DNA分子发生了变异)(2分)
③杂交后代不出现一定的性状分离比(2分)
(一部分仍为白化苗,一部分成为条斑苗,一部分成为绿色苗(2分)
(2)①如右图。(2分)

②叶龄(生长发育状况)相同、大小(面积)相同(2分)。
能延缓(减慢、减少、抑制)叶片中叶绿素的分解(降解)(2分)。
(3)①如右图(2分)

②少(2分)
③呈“花环型”的两圈细胞(2分)
31.(22分)
(1)①种群密度(种群数量)(1分) 性别比例(1分) 寄生(1分)
②人工合成基因(反转录法、化学合成法)(1分)
B、C、D(2分)
水稻植株表现出抗虫性状(水稻细胞中具有了目的基因的表达产物)(2分)
③3/4(2分)
(2)①X(2分) 隐(2分)
正常个体多于患病个体(2分)
②1/4(2分)
③该病为伴X隐性遗传病,正常的父亲不能可能生出患病的女儿(2分)
父亲产生精子的过程中发生了基因突变(或女儿的体细胞发生了基因突变)(2分)
(如果答成是环境因素引起的,给1分)