网址:http://m.1010jiajiao.com/timu_id_516129[举报]
(18分)某研究性学习小组在CO还原Fe2O3的实验中,用磁铁吸出生成的黑色粉末X,他们认为X不一定是Fe,若温度不均时会生成Fe3O4,也能被磁铁吸引。为了探究X的组成,他们进行了如下实验。
I、定性检验
|
实验编号 |
实验操作 |
实验现象 |
|
① |
取少量黑色粉末X放入试管1中,注入浓盐酸,微热 |
黑色粉末逐渐溶解,溶液呈黄绿色,有少量气泡产生 |
|
② |
另取少量黑色粉末X放入试管2中,注入足量硫酸铜溶液,振荡,静置 |
有极少量红色物质析出,仍有较多黑色固体未溶解 |
由上述实验现象推断,黑色粉末X的成分是 。
II定量测定

⑴操作Z的名称是 。
下列仪器中,在灼烧沉淀时必须用到的是 (填字母)。




A B C D E F
⑵写出溶液Y中滴加H2O2溶液时发生反应的离子方程式 。
⑶将沉淀物加热,并置于干燥器中冷却至室温,用托盘天平称量其质量为b1g,再次加热并冷却至室温称量其质量为b2g,若b1 —b2 = 0.3g,则接下来还应进行的操作是
。
⑷有同学认为:上述流程若不加入H2O2,其它步骤不变,只要在空气中充分放置仍可达到目的。他的理由是 。(用化学方程式表示)
⑸通过以上数据,得出2.376g黑色粉末中各成分的物质的量为 。
查看习题详情和答案>>
某研究性学习小组在CO还原Fe2O3的实验中,用磁铁吸出生成的黑色粉末X,他们认为X不一定是Fe,若温度不均时会生成Fe3O4,也能被磁铁吸引。为了探究X的组成,他们进行了如下实验。
I、定性检验
| 实验编号 | 实验操作 | 实验现象 |
| ① | 取少量黑色粉末X放入试管1中,注入浓盐酸,微热 | 黑色粉末逐渐溶解,溶液呈黄绿色,有少量气泡产生 |
| ② | 另取少量黑色粉末X放入试管2中,注入足量硫酸铜溶液,振荡,静置 | 有极少量红色物质析出,仍有较多黑色固体未溶解 |
由上述实验现象推断,黑色粉末X的成分是 。
II定量测定

⑴操作Z的名称是 。
下列仪器中,在灼烧沉淀时必须用到的是 (填字母)。




A B C D E F
⑵写出溶液Y中滴加H2O2溶液时发生反应的离子方程式 。
⑶将沉淀物加热,并置于干燥器中冷却至室温,用托盘天平称量其质量为b1g,再次加热并冷却至室温称量其质量为b2g,若b1 —b2 = 0.3g,则接下来还应进行的操作是
。
⑷有同学认为:上述流程若不加入H2O2,其它步骤不变,只要在空气中充分放置仍可达到目的。他的理由是 。(用化学方程式表示)
⑸通过以上数据,得出2.376g黑色粉末中各成分的物质的量为 。
查看习题详情和答案>>(18分)某研究性学习小组在CO还原Fe2O3的实验中,用磁铁吸出生成的黑色粉末X,他们认为X不一定是Fe,若温度不均时会生成Fe3O4,也能被磁铁吸引。为了探究X的组成,他们进行了如下实验。
I、定性检验
| 实验编号 | 实验操作 | 实验现象 |
| ① | 取少量黑色粉末X放入试管1中,注入浓盐酸,微热 | 黑色粉末逐渐溶解,溶液呈黄绿色,有少量气泡产生 |
| ② | 另取少量黑色粉末X放入试管2中,注入足量硫酸铜溶液,振荡,静置 | 有极少量红色物质析出,仍有较多黑色固体未溶解 |
II定量测定

⑴操作Z的名称是 。
下列仪器中,在灼烧沉淀时必须用到的是 (填字母)。




A B C D E F
⑵写出溶液Y中滴加H2O2溶液时发生反应的离子方程式 。
⑶将沉淀物加热,并置于干燥器中冷却至室温,用托盘天平称量其质量为b1g,再次加热并冷却至室温称量其质量为b2g,若b1—b2 = 0.3g,则接下来还应进行的操作是
 。
。⑷有同学认为:上述流程若不加入H2O2,其它步骤不变,只要在空气中充分放置仍可达到目的。他的理由是 。(用化学方程式表示)
⑸通过以上数据,得出2.376g黑色粉末中各成分的物质的量为 。 查看习题详情和答案>>
(18分)某研究性学习小组在CO还原Fe2O3的实验中,用磁铁吸出生成的黑色粉末X,他们认为X不一定是Fe,若温度不均时会生成Fe3O4,也能被磁铁吸引。为了探究X的组成,他们进行了如下实验。
I、定性检验
| 实验编号 | 实验操作 | 实验现象 |
| ① | 取少量黑色粉末X放入试管1中,注入浓盐酸,微热 | 黑色粉末逐渐溶解,溶液呈黄绿色,有少量气泡产生 |
| ② | 另取少量黑色粉末X放入试管2中,注入足量硫酸铜溶液,振荡,静置 | 有极少量红色物质析出,仍有较多黑色固体未溶解 |
由上述实验现象推断,黑色粉末X的成分是 。
II定量测定
⑴操作Z的名称是 。
下列仪器中,在灼烧沉淀时必须用到的是 (填字母)。


A B C D E F
⑵写出溶液Y中滴加H2O2溶液时发生反应的离子方程式 。
⑶将沉淀物加热,并置于干燥器中冷却至室温,用托盘天平称量其质量为b1g,再次加热并冷却至室温称量其质量为b2g,若b1 —b2 = 0.3g,则接下来还应进行的操作是
。
⑷有同学认为:上述流程若不加入H2O2,其它步骤不变,只要在空气中充分放置仍可达到目的。他的理由是 。(用化学方程式表示)
⑸通过以上数据,得出2.376g黑色粉末中各成分的物质的量为 。
查看习题详情和答案>>
(1)完成并配平离子反应方程式:
(2)请完成相应的实验步骤:
步骤1:称取35.60g草酸三氢钾试样,加水溶解,配成250mL溶液.
步骤2:用移液管量取两份此溶液各25.00mL,分别置于两个锥形瓶中.
步骤3:第1份溶液加硫酸酸化后,用0.1000mol?L-1的高锰酸钾溶液滴定,至滴定终点消耗高锰酸钾溶液12.00mL.
步骤4:在第2份溶液中
(3)根据(2)中的实验步骤回答:
①步骤1用到的实验仪器有:电子天平、药匙、烧杯、玻璃棒、
②如何判断步骤3中的滴定终点?
③3.560g试样中含有还原剂(草酸根)的物质的量共为
(4)热重分析法(TG)是在程序控制温度下,测量物质的质量与温度的关系的一种实验技术.热重分析仪的基本构造由精密天平、程序控温加热炉和记录仪组成;记录仪画出剩余固体质量(m)~炉温(T)曲线,即热重(TG)曲线图.如图为CaC2O4?H2O在N2和O2气氛中的热重曲线.
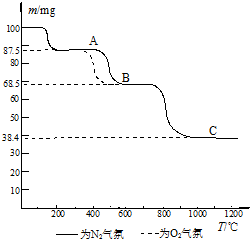
①C点所得固体的化学式为
②CaC2O4?H2O的分解分三个阶段,由图可看出,第二阶段在O2气氛中的反应速率要比在N2气氛中的快,原因是