网址:http://m.1010jiajiao.com/timu_id_50743[举报]
说明:1. 文字简答题以关键词到位为准,按点给分;
2. 化学用语书写:(1)方程式未配平不得分、无条件扣一半分值;
(2)化学式书写错误得0分;
3. 写名称或化学式正确的正常给分; 4. 其他合理解法正常给分。
第Ⅰ卷(选择题,共48分)
题号
1
2
3
4
5
6
7
8
9
10
11
12
13
14
答案
C
D
A
D
C
B
B
C
CD
B
CD
B
AD
A
第Ⅱ卷(非选择题 共72分)
三、(本题包括2小题,共22分)
15.(6分)(1)镁条表面产生气泡(2分)(2)A,B或C或D(2分,各1分)
(3)Mg+Cu2++2H2O=Mg2++Cu(OH)2↓+H2↑ Mg+Cu2+= Mg2++Cu (各1分,共2分)
16.(16分)(1)烧杯、玻璃棒,过滤,换过滤器并重新进行过滤操作(4分,每空1分)
(2)NaOH、Na2CO3(2分) (3)NaOH C (2分,各1分)
(4)除去NaOH和Na2CO3(2分) (5)蒸发皿,蒸发皿中有大量固体析出(2分,各1分)
(6)加快沉淀生成 5.61×10―8 mol?L―1。(4分,各2分)
四、(本题包括2小题,共18分)
17.(8分)(1)小,工业制备硫酸。 (2)MnO2 + 2Fe2+ + 4H+ = Mn2+ + 2Fe3+ + 2H2O。
使Fe2+ 转变为Fe3+,Fe3+完全沉淀的pH较低(或Fe3+更易沉淀)。
(3)与溶液中的酸反应,使溶液中的Fe3+、Al3+转化为氢氧化物沉淀。
(4)使MnCO3沉淀完全。MnCO3沉淀量少,NH4HCO3与酸反应。
(或MnCO3、NH4HCO3与酸反应溶解)
(5)节约能源、治理含SO2的工业废气等。(答对1个即可)(每空1分)
18.(10分)(1)接触室,防止催化剂中毒。(各1分,共2分)
(2)SO2+V2O5 SO3+ V2O4 4VOSO4+O2
SO3+ V2O4 4VOSO4+O2 2V2O5+4SO3(各1分,共2分)
2V2O5+4SO3(各1分,共2分)
(3)400 L?mol―1,使用常压SO2就可以达到较高的转化率。(前者2分,后者1分,共3分)
(4)①②,V2O5+ SO32―+4H+=2VO2++SO42―+2H2O。4和80℃。(各1分,共3分)
五、(本题包括1小题,共14分)
19.(14分)(1)4(2分)
(2) (2分)
(2分) (2分)
(2分)
(3)保护醛基不被还原。(2分)
(4)RCHO + 2Ag(NH3)2+
+ 2OH-  RCOO― +NH4+ +2Ag↓+3NH3 + H2O
(2分)
RCOO― +NH4+ +2Ag↓+3NH3 + H2O
(2分)
(5)(4分,对1步给2分,对2步给3分,全对给4分)

六、(本题包括1小题,共8分)
20.(8分)解:(1)6Fe2++ClO3-+6H+===6Fe3++Cl-+3H2O (2分)
(2)n(Fe)=2.80g/160g?mol-1×2=0.035mol
n(SO42-)=10.48 g /233 g?mol-1=0.045mol
n(OH-)=3×n(Fe)-2×n(SO42-)=3×0.035-2×0.045=0.015mol (2分)
盐基度=n(OH-)/3n(Fe)×100%
= 0.015 mol/(3×0.035 mol) ×100%
=14.29% (2分)
(3)n(H2O)=(7.51g―0.035mol×56g?mol -1-0.045mol×96 g?mol-1-0.015mol×17 g?mol-1)/18 g?mol-1=0.054 mol
化学式: Fe35(OH)15(SO4)45?54H2O (2分)
七、选做题(下面两题分别对应于“物质结构与性质”和“实验化学”两个选修课程模块的内容,请你选择其中一题作答,如果你两题全做,按第一题评分。每题均为10分。)
22. (A) (1)第四周期,第Ⅷ族 (1分) (2)CN― C22- sp3 液态氨汽化时需吸收大量的热 2 (各1分,共4分)
(3) [Ar]3d7;或 (1分)2NiO(OH) + 6HCl(浓)=2NiCl2+Cl2↑+4H2O;(1分)
(1分)2NiO(OH) + 6HCl(浓)=2NiCl2+Cl2↑+4H2O;(1分)
(4)x=5(1分) LaNi5H6+6OH- -6e-==LaNi5+6H2O (2分)
21.(B)22(B)(1)固定试管(2分) 容量瓶 酸式滴定管 烧杯(共2分,答对1-2个给1分,全对给2分)
(2)Al2O3 + 2NaOH =2NaAlO2 +H2O, 作用:去除铝箔表面的氧化膜 2Al + 3HgCl2 =2AlCl3 + 3Hg ,Al + Hg =Al (Hg) (铝汞齐), 作用:形成铝汞齐破坏致密氧化膜的形成(共2分)
(3)打开橡皮塞,用火柴点燃,出现轻微“噗”声或尖锐爆鸣声皆能说明有H2生成。(2分)
(4)原因分别是:浓硫酸具有吸水性,溢出后吸收空气的水变成稀硫酸,而稀硫酸与铝的氧化膜及铝本身皆发生反应;浓硝酸具有挥发性,溢出后因挥发同样会变稀,变稀的硝酸与氧化膜及铝本身亦发生反应。(各1分,2分)
 (1)如图所示为冰晶石(化学式为Na3AlF6)的晶胞.图中●位于大立方体顶点和面心,○位于大立方体的12条棱的中点和8个小立方体的体心,▽是图中●、○中的一种.图中●、○分别指代哪种粒子
(1)如图所示为冰晶石(化学式为Na3AlF6)的晶胞.图中●位于大立方体顶点和面心,○位于大立方体的12条棱的中点和8个小立方体的体心,▽是图中●、○中的一种.图中●、○分别指代哪种粒子(2)H2S和H2O2的主要物理性质比较如下:
| 熔点/K | 沸点/K | 标准状况时在水中的溶解度 | |
| H2S | 187 | 202 | 2.6 |
| H2O2 | 272 | 423 | 以任意比互溶 |
(3)向盛有硫酸铜水溶液的试管里加入氨水,首先形成难溶物,继续加氨水,难溶物溶解,得到深蓝色的透明溶液;若加入极性较小的溶剂(如乙醇),将析出深蓝色的晶体.与铜同一周期的副族元素的基态原子中最外层电子数与铜原子相同的元素有
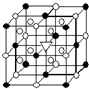 A.(1)右图所示为冰晶石(化学式为Na3AlF6)的晶胞.图中●位于大立方体顶点和面心,○位于大立方体的12条棱的中点和8个小立方体的体心,▽图中●、○中的一种.图中●、○分别指代哪种粒子
A.(1)右图所示为冰晶石(化学式为Na3AlF6)的晶胞.图中●位于大立方体顶点和面心,○位于大立方体的12条棱的中点和8个小立方体的体心,▽图中●、○中的一种.图中●、○分别指代哪种粒子(2)H2S和H2O2的主要物理性质比较如下:
| 熔点/K | 沸点/K | 标准状况时在水中的溶解度 | |
| H2S | 187 | 202 | 2.6 |
| H2O2 | 272 | 423 | 以任意比互溶 |
(3)向盛有硫酸铜水溶液的试管里加入氨水,首先形成难溶物,继续加氨水,难溶物溶解,得到深蓝色的透明溶液;若加入极性较小的溶剂(如乙醇),将析出深蓝色的晶体.写出铜原子价电子层的电子排布式
B.用含少量铁的氧化铜制取氯化铜晶体(CuCl2?xH2O).有如下操作:
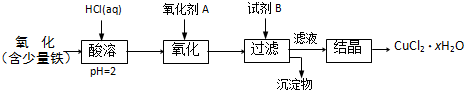
已知:在pH为4~5时,Fe3+几乎完全水解而沉淀,Cu2+却不水解.
(1)加热酸溶过程中发生反应的离子方程式有:
(2)氧化剂A可选用
①Cl2 ②KMnO4 ③HNO3
(3)要得到较纯的产品,试剂B可选用
①NaOH ②FeO ③CuO
(4)试剂B的作用是
①提高溶液的pH ②降低溶液的pH ③使Fe3+完全沉淀 ④使Cu2+完全沉淀
(5)从滤液经过结晶得到氯化铜晶体的方法是
①过滤 ②蒸发浓缩 ③蒸发至干 ④冷却
(6)为了测定制得的氯化铜晶体(CuCl2?xH2O)中x值,某兴趣小组设计了两种实验方案:
方案一:称取m g晶体灼烧至质量不再减轻为止、冷却、称量所得无水CuCl2的质量为n g.
方案二:称取m g晶体、加入足量氢氧化钠溶液、过滤、沉淀洗涤后用小火加热至质量不再减轻为止、冷却、称量所得固体的质量为n g.
试评价上述两种实验方案,其中正确的方案是
| 80m-135n |
| 18n |
| 80m-135n |
| 18n |
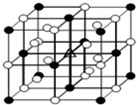 (2011?常州三模)如图所示为冰晶石(化学式为Na3AlF6)的晶胞.图中●位于大立方体顶点和面心,○位于大立方体的12条棱的中点和8个小立方体的体心.则下列说法正确的是( )
(2011?常州三模)如图所示为冰晶石(化学式为Na3AlF6)的晶胞.图中●位于大立方体顶点和面心,○位于大立方体的12条棱的中点和8个小立方体的体心.则下列说法正确的是( )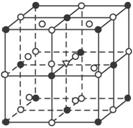
·位于大立方体的顶点和面心
。位于大立方体的12条棱的中点和8个小立方体的体心
那么大立方体的体心处?所代表的粒子应为( )
A.Na+ B.Al3+ C.F- D. ![]()
(15分)
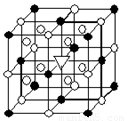
(1)如图所示为冰晶石(化学式为Na3AlF6)的晶胞。图中●位于大立方体顶点和面心,○位于大立方体的12条棱的中点和8个小立方体的体心,▽是图中●、○中的一种。图中●、○分别指代哪种粒子 、 ;大立方体的体心处▽所代表的是 (用化学式表示)。
(2)H2S和H2O2的主要物理性质比较如下:
|
|
熔点/K |
沸点/K |
标准状况时在水中的溶解度 |
|
H2S |
187 |
202 |
2.6 |
|
H2O2 |
272 |
423 |
以任意比互溶 |
H2S和H2O2的相对分子质量基本相同,造成上述物理性质差异的主要原因
。
(3)向盛有硫酸铜水溶液的试管里加入氨水,首先形成难溶物,继续加氨水,难溶物溶解,得到深蓝色的透明溶液;若加入极性较小的溶剂(如乙醇),将析出深蓝色的晶体。与铜同一周期的副族元素的基态原子中最外层电子数与铜原子相同的元素有_______(填元素符号)。实验时形成的深蓝色溶液中的阳离子内存在的全部化学键类型有 。实验过程中加入C2H5OH后可观察到析出深蓝色Cu(NH3)4SO4·H2O晶体。实验中所加C2H5OH的作用是 。
查看习题详情和答案>>