网址:http://m.1010jiajiao.com/timu_id_467792[举报]
一、选择题(本题包括13小题。每小题只有一个符合题意)
1.C 2.A 3.B 4.B 5.D 6.B 7.D 8.C 9.A 10.D 11.A 12.C 13B
二、选择题(本题包括8小题,每小题给的四个选项中,有的只有一个选项正确,有的有多个选项正确,全部选对的得6分,选对但不全的得3分,有选错或不答的得0分)
14.BC 15.BD 16.CD 17.D 18.A 19.B 20.C 21.AC
(2)①C (2分)
②电路如图所示。(5分)
③doc.files/image162.gif) ,(2分)
,(2分)doc.files/image164.gif) 为电压表读数,
为电压表读数,doc.files/image166.gif) 为电压表内阻。(2分)
为电压表内阻。(2分)
doc.files/image168.jpg) 23.(16分)解:
23.(16分)解:
受力分析如图,据牛顿第二定律有
减速上升250m与加速下降250m互逆
据题意doc.files/image172.gif) ②
②
doc.files/image174.gif) ③
③
代入数据可得
doc.files/image176.gif) ④
④
doc.files/image178.gif) ⑤
⑤
设计师应设计发射速度doc.files/image180.gif)
同时数码点火控制时间应设定doc.files/image182.gif)
评分参考:①②③式分别得4分,④④式分别得2分
24.(19分)解:(1)衰变方程:doc.files/image184.gif) ①
①
(2)由题意知衰变放出的质量较小的粒子doc.files/image186.gif) 在磁场中做匀速圆周运动的轨道半径;
在磁场中做匀速圆周运动的轨道半径;
doc.files/image188.gif) ②
②
由doc.files/image190.gif) ③
③
代入数据得doc.files/image192.gif) ④
④
(3)衰变过程中的动量守恒doc.files/image194.gif) ⑤
⑤
由doc.files/image196.gif)
所以doc.files/image198.gif) ⑥
⑥
doc.files/image200.gif)
所以doc.files/image202.gif) ⑦
⑦
评分参考:①②③⑤⑥式分别得3分,④⑦式得2分
25.(20分)解:(1)木块A和滑板B均向左做匀加速直线运动
doc.files/image204.gif) ①
①
doc.files/image206.gif)
doc.files/image208.gif) ②
②
doc.files/image210.gif)
根据题意有doc.files/image212.gif) ③
③
即doc.files/image214.gif) ④
④
(2)1s末木块A和滑板B的速度分别为
doc.files/image218.gif) ⑥
⑥
doc.files/image220.gif) ⑦
⑦
撤去F后,当木块A和滑板B的速度相同时,
弹簧压缩量最大,具有最大弹性势能 ⑧
根据动量守恒定律有doc.files/image222.gif) ⑨
⑨
代入数据求得doc.files/image224.gif) ⑩
⑩
由机械能守恒定律得
doc.files/image226.gif) 11
11
代入数据求得doc.files/image228.gif) 12
12
评分参考:①②③④⑥⑦⑨11式分别得2分,⑤⑧⑩12式分别得1分
26.(14分,每空2分)
(1) 分子 (2)doc.files/image230.gif)
doc.files/image231.jpg)
(3)①非极性 ②镁条在二氧化碳中剧烈燃烧,生成白色粉末,在瓶的内壁有黑色固体附着
(4)盛有冷水的广口瓶 doc.files/image233.gif)
27.(15分,每空3分)
(1)doc.files/image235.gif) (2分)
(2分)
(3)30% 大 (4)doc.files/image237.gif)
28.(16分)
(1)①ac(2分) ②除去doc.files/image005.gif) 中的
中的doc.files/image240.gif) (2分) ③
(2分) ③doc.files/image242.gif) (2分)
(2分)
④将湿润的红色石蕊试纸放在D出口处,若试纸变蓝,则证明有氨气逸出,若试纸不变蓝,则证明没有氨气逸出。(或用蘸有浓盐酸的玻璃棒靠近D出口处,若有白烟。则证明有氨气逸出;若没有白烟,则证明没有氨气逸出。) (2分)
(2)①A (2分) ②过滤、洗涤、干燥(3分) ③doc.files/image244.gif) (3分)
(3分)
29.(15分)(1)氧化反应(2分),酯化反应(2分)
(2)doc.files/image245.jpg) (2分)
(2分)
(3)doc.files/image246.jpg)
(4)doc.files/image248.jpg)
(5)4(3分)
30.(共25分)
(I)(12分,每空1分)
(I)较高 较低 较高(2)较低 较高(3)增加 增加 较低(4)大于 小 大于 小于
(Ⅱ)(13分)
(1)D(2分) (2)doc.files/image005.gif) (2分) 含碳有机物(2分)(3)分解者的分解作用(2分)
(2分) 含碳有机物(2分)(3)分解者的分解作用(2分)
(4)8(2分)(5)害虫的抗药性经过(杀虫剂)选择逐代增强 化学杀虫剂导致害虫天敌大量死亡破坏了生态系统原有的营养结构(3分)
31.(共17分)
(1)X射线(doc.files/image251.gif) 射线、
射线、doc.files/image253.gif) 射线、
射线、doc.files/image255.gif) 射线、紫外线等)辐射(2分)
射线、紫外线等)辐射(2分)
(2)雌性红眼:雄性白眼=1:1 (2分)
(3)doc.files/image257.gif) (2分)
(2分)
(4)1/16(2分)
(5)雌果蝇,减数第一次分裂或减数第二次分裂过程中(3分);雄果蝇,减数第一次分裂过程中。(3分)
(6)取果蝇分裂期的体细胞,制作有丝分裂装片,在光学显微镜下观察,找出分裂中期的性染色体。(3分)
本资料由《七彩教育网》www.7caiedu.cn 提供!
过碳酸钠(Na2CO3·3H2O2),有固体双氧水的俗称,该晶体具有Na2CO3和H2O2的双重性质,被大量应用于洗涤、印染、纺织、造纸、医药卫生等领域中,过碳酸钠的某生产流程如下图所示。
已知:2Na2CO3+3H2O2=2Na2CO3·3H2O △H<0;回答下列问题: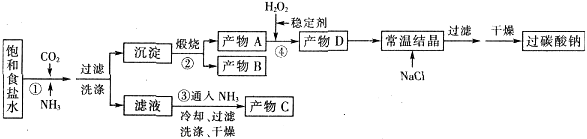
(1)下列物质可使过碳酸钠较快失效的是(填序号)_________。
| A.FeCl3溶液 | B.H2S | C.稀硫酸 | D.NaHCO3溶液 |
(3)在上述流程中,向反应前的H2O2中加入稳定剂的作用是____________________。
(4)该生产流程中可循环使用的物质是______________________________(填化学式)。
(5)生产过碳酸钠的流程中遗漏了一步,造成所得产品纯度偏低,请简述该步操作过程___________。
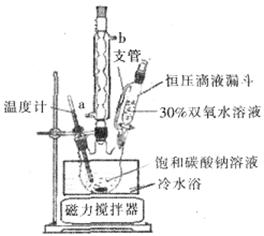
(6)实验室利用下图装置制备过碳酸钠,该装置中恒压滴液漏斗中支管的作用是_______,冷凝管应从__________处进水。
(7)由实验测定反应温度对产物的影响如下表:根据下表数据,你认为反应最佳的温度选择的范围是_______________。
| T/℃ | 活性氧百分含量 | 产率 |
| 5~10 | 13.94 | 85.49 |
| 10~15 | 14.02 | 85.78 |
| 15~20 | 15.05 | 88.38 |
| 20~25 | 14.46 | 83.01 |
 、
查看习题详情和答案>>
、
查看习题详情和答案>>
已知:2Na2CO3+3H2O2=2Na2CO3·3H2O △H<0;回答下列问题:
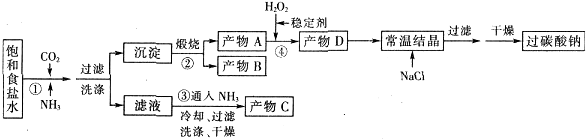
(1)下列物质可使过碳酸钠较快失效的是(填序号)_________。
| A.FeCl3溶液 | B.H2S | C.稀硫酸 | D.NaHCO3溶液 |
(3)在上述流程中,向反应前的H2O2中加入稳定剂的作用是____________________。
(4)该生产流程中可循环使用的物质是______________________________(填化学式)。
(5)生产过碳酸钠的流程中遗漏了一步,造成所得产品纯度偏低,请简述该步操作过程___________。
(6)实验室利用下图装置制备过碳酸钠,该装置中恒压滴液漏斗中支管的作用是_______,冷凝管应从__________处进水。
(7)由实验测定反应温度对产物的影响如下表:根据下表数据,你认为反应最佳的温度选择的范围是_______________。
| T/℃ | 活性氧百分含量 | 产率 |
| 5~10 | 13.94 | 85.49 |
| 10~15 | 14.02 | 85.78 |
| 15~20 | 15.05 | 88.38 |
| 20~25 | 14.46 | 83.01 |
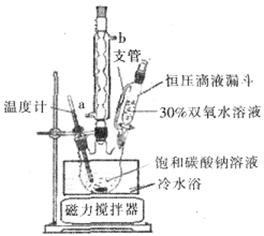 、
、根据上述材料,回答下列问题:
(1)H2O2的结构式为________,分子中氧元素的化合价为 ________。
(2)H2O2的结构特点决定了H2O2具有多重性质。
①双氧水有多种性质:Na2O2+2HCl===H2O2+2NaCl,这个反应体现了双氧水的________性。
②向含有酚酞的NaOH溶液中滴加H2O2,溶液红色褪去,体现了H2O2的________性。
③将H2O2加入经酸化的KMnO4溶液中,溶液的紫红色消失,这体现了H2O2的________性
(3)H2O2被称为绿色氧化剂的理由是____________________________。
(4)下列物质不会使过碳酸钠失效的是________(填写字母序号)。
A.MnO2 B. H2S C.CH3COOH D. NaHCO3
(5)H2O2不稳定,易分解,在催化剂作用下分解更快。
①实验室用H2O2制O2的化学方程式为:_______________________________。
②已知下列反应在一定条件下可以发生:
a.H2O2+2Fe2++2H+===2Fe3++2H2O; b.H2O2+2Fe3+===2Fe2++O2↑+2H+;在以上反应中Fe2+实际上起着________作用,总反应式为__________________________。
过氧化氢(H2O2)是一种无色透明粘稠状液体,它的水溶液俗称双氧水,呈弱酸性,一种强氧化剂,漂白剂,消毒剂,是生产过氧化物的原料.
(1)写出H2O2的电子式_________________,
(2)H2O2与强碱反应可生成正盐,一定条件下也生成酸式盐,写出NaOH与H2O2反应生成酸式盐的化学方程式:____________________.
(3)在H2O2中加入少量苯,再滴人数滴K2Cr2O7的硫酸溶液,振荡静置,苯层呈蓝色,这是由于反应生成过氧化铬(CrO5)溶于苯的缘故,已知过氧化铬的结构式为:①写出该反应的离子方程式:________________
②这个反应是否是氧化还原反应?________,其理由是________
(4)双氧水属于________(A强电解质、B弱电解质、C非电解质、D以上都错),它被称为“绿色氧化剂”,理由是__________________________________.
doc.files/image159.jpg) 22.(17分)(1)1.0
22.(17分)(1)1.0doc.files/image055.gif)
doc.files/image170.gif)
doc.files/image216.gif)