网址:http://m.1010jiajiao.com/timu_id_4436893[举报]
高中阶段常用化学反应方程式
- 钠在空气中燃烧(黄色的火焰)
- 钠与水反应(浮、熔、游、响、红)
- 过氧化钠与水的反应
- 过氧化钠与二氧化碳的反应
- 苏打(纯碱)与盐酸反应
- 小苏打受热分解
- *固体氢氧化钠、碳酸氢钠混合物在密闭容器中加热
- 金属锂在空气中燃烧
- 铜丝在氯气中剧烈燃烧(棕色烟)
- 铁在氯气中剧烈燃烧
- 氢气在氯气中燃烧(苍白色火焰,瓶口白雾)
- 氯气溶于水及新制氯水的成分:
- 次氯酸见光分解(强氧化剂、杀菌消毒、漂白剂)
- 工业制漂白粉原理
- 氯气实验室制法(主仪器:分液漏斗、圆底烧瓶等)
- 新制氯水注入盛溴化钠溶液的试管中
- 用电子式表示溴化镁、氯化氢分子的形成
- 铁与硫加热反应
- 硫化氢充分燃烧
- 硫化氢不完全燃烧
- 硫化亚铁与稀盐酸反应
- 二氧化硫制三氧化硫(无色固体,熔点16.8℃,44.8℃)
- 浓硫酸与铜反应
- 浓硫酸与非金属碳的反应
- 工业制单质硅(碳在高温下还原二氧化硅)
- 二氧化硅与氢氧化钠反应
- 氮气和氢气反应
- 氮气与氧气放电条件下反应
- 二氧化氮溶于水
- NO2、O2混合气通入水中无剩余气体
- 一定量的NO、O2混合通入水中无剩余气体
- 五氧化二磷与热水反应
- 磷在氯气中充分燃烧
- 氨的催化氧化
- 碳酸氢铵受热分解
- 用浓盐酸检验氨气(白烟生成)
- 硫酸铵溶液与氢氧化钠溶液混合加热
- 硝酸铵溶液与氢氧化钠溶液混合(不加热)
- 铝箔在氧气中剧烈燃烧
- 铝片与稀盐酸反应
- 铝与氢氧化钠溶液反应
- 铝与三氧化二铁高温下反应(铝热反应)
- 镁在二氧化碳中燃
- 氧化铝溶于氢氧化钠溶液
- 硫酸铝溶液中滴过量氨水
- 氢氧化铝溶液中加盐酸
- *高温下铁与水反应
- 铁与盐酸反应
- 氧化铁溶于盐酸中
- 化铁中滴入氢氧化钠溶液(红褐色沉淀)
- 氢氧化亚铁在空气中氧化
- 氯化亚铁溶液中通入氯气
- 氯化铁溶液中加入铁粉
- 甲烷与氯气取代生成四氯化碳
- 乙烯实验室制法(浓硫酸作催化剂,脱水剂)
- 乙烯通入溴水中
- 制取聚乙烯、聚丙烯
- 乙制取
- 由乙炔制聚乙烯
- 与液溴反应(需铁作催化剂)
- 苯的硝化反应
- 与氢气加成生成环己烷
- 甲苯发生硝化反应
- 乙烷水解
- 乙烷消去反应
- 醇与钠反应
- 乙醇催化氧化
- 苯酚与氢氧化钠溶液反应
- 苯酚钠溶液中通入二氧化碳
- 苯酚的定性检验定量测定方法:
- 醛制1-丙醇
- 醛制乙酸
- 乙醛的银镜反应
- 醛与新制氢氧化铜悬浊液
- *乙酸与氢氧化铜悬浊液
- 酸乙酯制取(用饱和碳酸钠溶液收集)
- 葡萄糖结构简式
- 蔗水解方程式
- 淀粉水解
- 硬脂酸甘油酯皂化反应
A.《化学与生活》
(1)现有下列五种物质:(a)食盐 (b)食醋 (c)苹果汁 (d)葡萄糖 (e)青霉素,请按下列要求填空(填序号).
富含维生素C的是______;可直接进入血液补充能量的是______;应用最广泛的抗生素之一的是______;即可作为调味剂,又可预防感冒的是______;食用过多会引起血压升高、肾脏受损的______.
(2)防治环境污染,改善生态环境已成为全球的共识.
①空气质量报告的各项指标可以反映出各地空气的质量.下列气体已纳入我国空气质量报告的是______ (填字母).
a.CO2 b.N2 c.NO2
②垃圾应分类收集.导致“白色污染”的生活垃圾应放置于贴有______ (填字母)标志的垃圾筒内.
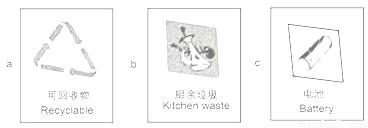
③工业废水需处理达标后才能排放.下列废水处理的方法合理的是______ (填字母).
a.用中和法除去废水中的酸
b.用混凝剂除去废水中的重金属离子
c.用氯气除去废水中的悬浮物
(3)材料是人类赖以生存的重要物质基础,而化学是材料科学发展的基础.请填写下列空格.
①生活中的陶瓷、水泥和______属于传统无机硅酸盐材料,其中生产不需要用石灰石作原料的是______.
②在原子反应堆中得以广泛应用的钠钾合金在常温下呈液态,说明合金的熔点比其成分金属的熔点______(填“高”或“低”).
③下列对金属制品采取的防护方法不正确的是______(填序号).
A.在电线的外面包上一层塑料层 B.在自行车钢圈上镀上一层金属铬
C.在海轮的铁制外壳上焊上铜块
(4)某肉制品包装上印有相关配料:精选瘦肉、食盐、亚硝酸钠、苯甲酸钠.其中属于调味剂的是______,属于发色剂的是______,属于防腐剂的是______.
B.《有机化学基础》(我校学生统一不选做)
(1)(3分)根据结构对有机物进行分类,有助于对其性质的掌握.
①下列有机物属于芳香烃的是______ (填字母).
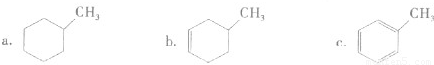
②下列有机物属于酚类的是______ (填字母).
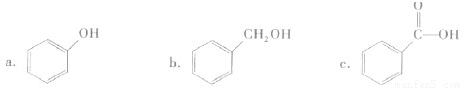
③下列有机物属于糖类的是______ (填字母).
a.油脂 b.纤维素 c.蛋白质
(2)化合物X的结构简式为:
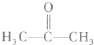
①X的核磁共振氢谱图(H核磁共振谱图)上有______个吸收峰.
②X的一种同分异构体Y能发生银镜反应,请写出Y的结构简式:______.
③X的另一种同分异构体z的结构简式为H2C═CHCH2OH,请写出Z与Br2发生加成反应的化学方程式:______.
(3)2010年上海世博会充分体现了绿色生活理念,节能环保材料在园区内随处可见.如一次性餐盒是由一种生物可降解的高分子合成材料制得.其结构简式如下:
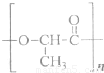
①该高分子材料是由一种单体通过______ 反应(填反应类型)制备而成,其单体的结构简式为______.
②若两分子的该单体发生反应,既可能得到环状化合物M,也可能得到链状化合物N.其结构简式如下:
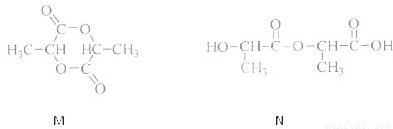
请用两种方法鉴别M和N.方法一:______;方法二:______.
查看习题详情和答案>>
A.《化学与生活》
(1)现有下列五种物质:(a)食盐 (b)食醋 (c)苹果汁 (d)葡萄糖 (e)青霉素,请按下列要求填空(填序号).
富含维生素C的是
(2)防治环境污染,改善生态环境已成为全球的共识.
①空气质量报告的各项指标可以反映出各地空气的质量.下列气体已纳入我国空气质量报告的是
a.CO2 b.N2 c.NO2
②垃圾应分类收集.导致“白色污染”的生活垃圾应放置于贴有
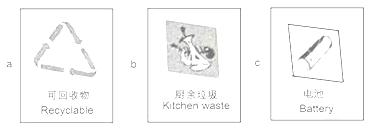
③工业废水需处理达标后才能排放.下列废水处理的方法合理的是
a.用中和法除去废水中的酸
b.用混凝剂除去废水中的重金属离子
c.用氯气除去废水中的悬浮物
(3)材料是人类赖以生存的重要物质基础,而化学是材料科学发展的基础.请填写下列空格.
①生活中的陶瓷、水泥和
②在原子反应堆中得以广泛应用的钠钾合金在常温下呈液态,说明合金的熔点比其成分金属的熔点
③下列对金属制品采取的防护方法不正确的是
A.在电线的外面包上一层塑料层 B.在自行车钢圈上镀上一层金属铬
C.在海轮的铁制外壳上焊上铜块
(4)某肉制品包装上印有相关配料:精选瘦肉、食盐、亚硝酸钠、苯甲酸钠.其中属于调味剂的是
B.《有机化学基础》(我校学生统一不选做)
(1)(3分)根据结构对有机物进行分类,有助于对其性质的掌握.
①下列有机物属于芳香烃的是
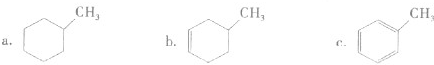
②下列有机物属于酚类的是
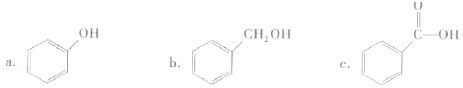
③下列有机物属于糖类的是
a.油脂 b.纤维素 c.蛋白质
(2)化合物X的结构简式为:
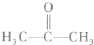
①X的核磁共振氢谱图(H核磁共振谱图)上有
②X的一种同分异构体Y能发生银镜反应,请写出Y的结构简式:
③X的另一种同分异构体z的结构简式为H2C═CHCH2OH,请写出Z与Br2发生加成反应的化学方程式:
(3)2010年上海世博会充分体现了绿色生活理念,节能环保材料在园区内随处可见.如一次性餐盒是由一种生物可降解的高分子合成材料制得.其结构简式如下:
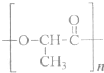
①该高分子材料是由一种单体通过


②若两分子的该单体发生反应,既可能得到环状化合物M,也可能得到链状化合物N.其结构简式如下:
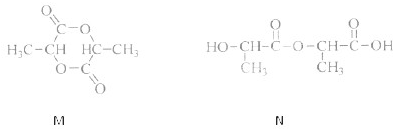
请用两种方法鉴别M和N.方法一:
A.《化学与生活》
(1)食品和药品关系人的生存和健康.
①市场上销售的食盐品种很多.下列食盐中,所添加的元素不属于人体必需微量元素的是
A.加锌盐 B.加碘盐 C.加钙盐
②纤维素被称为“第七营养素”.食物中的纤维素虽然不能为人体提供能量,但能促进肠道蠕动、吸附排出有害物质.从化学成分看,纤维素是一种
A.多糖 B.蛋白质 C.脂肪
③某同学感冒发烧,他可服用下列哪种药品进行治疗
A.麻黄碱 B.阿司匹林 C.抗酸药
(2)蛋白质是生命的基础,没有蛋白质就没有生命.请回答下列问题:
①油脂被摄入人体后,在酶的作用下水解为高级脂肪酸和
②人体摄入的蛋白质在胃蛋白酶和胰蛋白酶的作用下,水解成
③维生素C是一种重要维生素,能防治坏血病.用淀粉溶液、碘水为试剂,验证维生素C具有还原性的实验操作和现象是
(3)材料是人类赖以生存和发展的重要物质基础.
①普通玻璃是生活中常用的硅酸盐材料,其主要成分是Na2SiO3、CaSiO3和
| ||
| ||
②通常使用的钢铁是铁和
③天然橡胶(生胶)是线型高分子,因高分子链上有双键易老化,工业上常将它与含硫物质作用转变成为体型的网状分子的
B.《有机化学》
(1)有机物含有的官能团不同,性质也有差异.
①1mol下列有机物可与2mol溴单质发生加成反应的是
A.乙烯 B.乙炔 C.乙烷
②下列有机物中,核磁共振氢谱只有一个吸收峰的是
A.苯 B.苯酚 C.苯甲酸
③下列有机物中,能发生银镜反应的是
A.乙酸乙酯 B.乙醇 C.葡萄糖
(2)分子式为C4H10O,属于醇的同分异构体有




(3)科学家常采用将药物连接在高分子载体上,制成缓释长效药物.已知某种解热镇痛类药物,其结构简式如图甲,把它连接到高分子聚合物B上,形成缓释长效药物C如图乙.
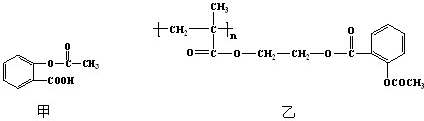
①分子聚合物B的结构简式为


②A与B反应生成C的有机反应类型是
③A可水解成


某学校同学进行乙醇的化学性质实验探究学习,以下为他们的学习过程。
(一)结构分析
(1)写出乙醇的结构式 ;官能团的电子式 。
(二)性质预测
(2)对比乙醇和乙烷的结构,经过讨论,同学们认为乙醇分子中氧原子吸引电子能力较强,预测在一定条件下分子中 键(填写具体共价键)容易发生断裂。为此,他们查阅了相关资料,获得了以下乙醇性质的部分事实。
|
下列关于乙醇结构和性质的分析、理解错误的是
A.-OH对-C2H5的影响使乙醇与钠的反应比水与钠的反应速率慢ks5u
B. 乙醇在浓硫酸催化下,170℃时脱水生成乙烯的反应为消去反应
C. 乙醇的核磁共振氢谱图上有3个吸收峰,其强度之比为3︰2︰1,与钠反应的是
吸收强度最小的氢原子
 D. 乙醇与甲醚互为官能团异构体
D. 乙醇与甲醚互为官能团异构体
(三)设计方案、进行实验
甲同学用4mL 95%的乙醇、8mL90%浓硫酸、
6g溴化钠研究乙醇转化为溴乙烷的反应。右图
是他设计的实验装置图(已省略部分夹持仪器)。
请回答有关问题。
(3)预计实验时装置Ⅰ主要发生两个反应,写出反应②的化学方程式。
![]() ①2NaBr + H2SO4 2HBr + Na2SO4,
①2NaBr + H2SO4 2HBr + Na2SO4,
②
(4)实验过程中,观察到反应后期烧瓶内液体颜色变棕黑,U形管右边与大气相通的导管口产生大量有刺激性气味的白雾,U形管内有少量淡黄色液体,该液体的有机成分是 。若要获得纯净的溴乙烷,方法是:实验结束后 。
(四)反思与改进
(5)乙同学认为:实验所用浓硫酸必须进行稀释,目的是 (填字母),稀释后的浓硫酸应放在 (填实验仪器名称)中。
A.减少HBr的挥发 B.防止浓硫酸分解产生SO2
C.减少副产物乙烯和乙醚的生成 D.减少Br2的生成
(6)丙同学提出应该对实验装置进行改进,请为两部分装置选择正确的措施:
A.不作改变 B.保留酒精灯加热,增加温度计且温度计水银球插入反应液中
C.水浴加热 D.冰水混合物冷却
装置Ⅰ ;装置Ⅱ 。请你再提出一条改进措施 。
查看习题详情和答案>>