题目内容
 某些废旧塑料可采用下列方法处理:将废塑料隔绝空气加强热,使其变成有用的物质,实验装置如图.加热聚丙烯废塑料得到的产物如表:
某些废旧塑料可采用下列方法处理:将废塑料隔绝空气加强热,使其变成有用的物质,实验装置如图.加热聚丙烯废塑料得到的产物如表:| 产物 | 氢气 | 甲烷 | 乙烯 | 丙烯 | 苯 | 甲苯 | 碳 |
| 质量分数(%) | 12 | 24 | 12 | 16 | 20 | 10 | 6 |

写出反应②的化学方程式.
CaC2+2H2O→Ca(OH)2+C2H2↑
CaC2+2H2O→Ca(OH)2+C2H2↑
(2)试管B收集到的产品中,其中有一种物质M能使酸性高锰酸钾溶液褪色.
①试写出体现该物质重要用途的一个反应方程式


②如该物质发生一氯取代,则生成物的同分异构体共有有
4
4
种;③另有M的同系物,分子式为C10Hn,则n=
14
14
,该物质结构中有2个乙基,则其所有可能的结构简式为 、
、 、
、
 、
、 、
、
(3)锥形瓶C中观察到的现象
棕黄色溶液变无色或褪色
棕黄色溶液变无色或褪色
.经溴水充分吸收,剩余气体经干燥后的平均相对分子质量为4.8
4.8
(4)写出C中逸出的气体在工业上的两种用途
合成氨原料
合成氨原料
、作燃料(或有机化工原料)
作燃料(或有机化工原料)
.分析:(1)碳化钙和水反应制取乙炔的方程式;
(2)①根据表格中的产物,判断出M是什么物质,然后写出用途及反应方程式;
②根据甲苯在苯环和侧链上的氢原子位置进行分析;
③根据笨的同系物通式计算出n;含有两个乙基,苯环上两个氢原子苯两个乙基
(3)产物中的乙烯、丙烯能够与溴水发生加成反应;剩余气体为甲烷和氢气,质量比为2:1,计算出物质的量之比,再计算出平均摩尔质量即可;
(4)C中最后逸出的气体是甲烷和氢气,根据所学知识找出二者用途.
(2)①根据表格中的产物,判断出M是什么物质,然后写出用途及反应方程式;
②根据甲苯在苯环和侧链上的氢原子位置进行分析;
③根据笨的同系物通式计算出n;含有两个乙基,苯环上两个氢原子苯两个乙基
(3)产物中的乙烯、丙烯能够与溴水发生加成反应;剩余气体为甲烷和氢气,质量比为2:1,计算出物质的量之比,再计算出平均摩尔质量即可;
(4)C中最后逸出的气体是甲烷和氢气,根据所学知识找出二者用途.
解答:解:(1)反应②是碳化钙与水反应,反应的化学方程式为:CaC2+2H2O→Ca(OH)2+C2H2↑,
故答案为:CaC2+2H2O→Ca(OH)2+C2H2↑;
(2)①试管B中含有苯和甲苯,苯不能使高锰酸钾褪色,甲苯可以使高锰酸钾褪色,M是甲苯,甲苯可以与硝酸反应制取TNT,反应的方程式为: ,
,
故答案为:
 ;
;
②一氯甲苯的同分异构体有:
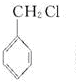
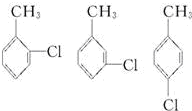 ,总计4种,
,总计4种,
故答案为:4;
③苯的同系物通式为CnH2n-6(n≥6),将n=10带人得n=14;分子中含有2个乙基,即苯环上的两个氢原子被乙基取代,有三种同分异构体,分别为: 、
、 、
、 ,
,
故答案为:14; 、
、 、
、
(3)产物中的乙烯、丙烯分子中含有碳碳双键,能够与溴水发生反应,溴水褪色;
经溴水充分吸收后剩余气体为甲烷和氢气,二者质量比为24%:12%=2:1,物质的量比为:
:
=1:4,平均摩尔质量为:
g/mol=4.8g/mol
所以甲烷和氢气的平均相对分子质量为4.8,
故答案为:棕黄色溶液变无色或褪色; 4.8;
(4)最后得到的气体是甲烷和氢气,氢气可以用于合成氨工业,甲烷可以做燃料,
故答案为:合成氨原料,作燃料或有机化工原料(或其他合理答案).
故答案为:CaC2+2H2O→Ca(OH)2+C2H2↑;
(2)①试管B中含有苯和甲苯,苯不能使高锰酸钾褪色,甲苯可以使高锰酸钾褪色,M是甲苯,甲苯可以与硝酸反应制取TNT,反应的方程式为:
 ,
,故答案为:
 ;
;②一氯甲苯的同分异构体有:

 ,总计4种,
,总计4种,故答案为:4;
③苯的同系物通式为CnH2n-6(n≥6),将n=10带人得n=14;分子中含有2个乙基,即苯环上的两个氢原子被乙基取代,有三种同分异构体,分别为:
 、
、 、
、 ,
,故答案为:14;
 、
、 、
、
(3)产物中的乙烯、丙烯分子中含有碳碳双键,能够与溴水发生反应,溴水褪色;
经溴水充分吸收后剩余气体为甲烷和氢气,二者质量比为24%:12%=2:1,物质的量比为:
| 2 |
| 16 |
| 1 |
| 2 |
| 16×1+4×2 |
| 1+4 |
所以甲烷和氢气的平均相对分子质量为4.8,
故答案为:棕黄色溶液变无色或褪色; 4.8;
(4)最后得到的气体是甲烷和氢气,氢气可以用于合成氨工业,甲烷可以做燃料,
故答案为:合成氨原料,作燃料或有机化工原料(或其他合理答案).
点评:本题考查了乙炔的性质实验,是一道实验综合题,知识点较多,难度不大,考查了学生分析问题的能力.

练习册系列答案
 期末金牌卷系列答案
期末金牌卷系列答案 轻松课堂标准练系列答案
轻松课堂标准练系列答案
相关题目
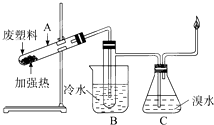 某些废旧塑料可采用下列方法处理:将废塑料隔绝空气加强热,使其变成有用的物质,实验装置如下图.加热聚丙烯废塑料得到的产物如下表:
某些废旧塑料可采用下列方法处理:将废塑料隔绝空气加强热,使其变成有用的物质,实验装置如下图.加热聚丙烯废塑料得到的产物如下表:| 产物 | 氢气 | 甲烷 | 乙烯 | 丙烯 | 苯 | 甲苯 | 碳 |
| 质量分数(%) | 12 | 24 | 12 | 16 | 20 | 10 | 6 |
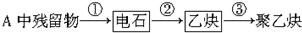
写出反应②③的化学方程式:
(2)试管B收集到的产品中,能使高锰酸钾酸性溶液褪色的物质,其一氯代物有
(3)锥形瓶C中观察到的现象
(4)写出C中逸出的气体在工业上的两种用途:
某些废旧塑料可采用下列方法处理:将废塑料隔绝空气加强热,使其变成有用的物质,实验装置如下图。加热聚丙烯废塑料得到的产物如下表:

产物 | 氢气 | 甲烷 | 乙烯 | 丙烯 | 苯 | 甲苯 | 碳 |
质量分数/% | 12 | 24 | 12 | 16 | 20 | 10 | 6 |
(1)试管A中残余物有多种用途,如下列转化就可制取高聚物聚乙炔。
![]()
写出反应②的化学方程式_________________________。
(2)试管B收集到的产品中,能使酸性高锰酸钾溶液褪色的物质,其一氯代物有________种。
(3)锥形瓶C中观察到的现象__________________。经溴水充分吸收,剩余气体经干燥后的平均相对分子质量为__________。
(4)写出C中逸出的气体在工业上的两种用途_________、_________。
某些废旧塑料可采用下列方法处理:将废塑料隔绝空气加强热,使其变成有用的物质,实验装置如下图。

加热聚丙烯废塑料得到的产物如下表:
产物 | 氢气 | 甲烷 | 乙烯 | 丙烯 | 苯 | 甲苯 | 碳 |
质量分数(%) | 12 | 24 | 12 | 16 | 20 | 10 | 6 |
(1)试管A中残余物有多种用途,如下列转化就可制取高聚物聚乙炔。
![]()
A中残留物①电石②乙炔③聚乙炔
写出反应②③的化学方程式_______________________________________________________、____________________________________________。
(2)试管B收集到的产品中,能使高锰酸钾酸性溶液褪色的物质,其一氯代物有______种。
(3)锥形瓶C中观察到的现象______________________________。经溴水充分吸收,剩余气体经干燥后的平均相对分子质量为___________。
(4)写出C中逸出的气体在工业上的两种用途________、________。
 某些废旧塑料可采用下列方法处理:将废塑料隔绝空气加强热,使其变成有用的物质,实验装置如图所示.
某些废旧塑料可采用下列方法处理:将废塑料隔绝空气加强热,使其变成有用的物质,实验装置如图所示.