摘要:BC.2.AC.3.无.4.AC.5.B.6.B.7.C.8.A.
网址:http://m.1010jiajiao.com/timu_id_4425862[举报]
根据下图所示的A、B、C、D、E五种物质的相互转化关系,按如下要求填写相应的物质和有关反应的化学方程式.
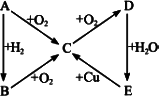
当A是气体单质时,应为________(填写化学式).
(1)A![]() C化学方程式为:________;
C化学方程式为:________;
(2)B![]() C化学方程式为:________;
C化学方程式为:________;
(3)E![]() C化学方程式为:________.
C化学方程式为:________.
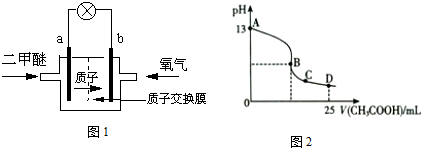 (1)二甲醚燃料电池的正极反应式为
(1)二甲醚燃料电池的正极反应式为O2+4H++4e-═2H2O
O2+4H++4e-═2H2O
.电池在放电过程中,负极周围溶液的pH减小
减小
.(填“增大”、“减小”或“不变”)(2)以上述电池为电源,通过导线电解池相连.两极为石墨,电解质溶液为1L 0.1mol/L KCl溶液,写出电解总反应的离子方程式为
2Cl-+2H2O
H2↑+Cl2↑+2OH-
| ||
2Cl-+2H2O
H2↑+Cl2↑+2OH-
.
| ||
(3)室温时,按上述(2)电解一段时间后,取25mL上述电解后溶液,滴加0.2mol/L 醋酸得到如图2.不考虑能量损失和气体溶于水,溶液体积变化忽略不计).
①若图2中的B点pH=7,则滴定终点在
AB
AB
区间(填“AB”、“BC”或“CD”).B点溶液中离子浓度大小为c(CH3COO-)=c(K+)>c(H+)=c(OH-)
c(CH3COO-)=c(K+)>c(H+)=c(OH-)
.②D点溶液中c(HAc)
<
<
c(Ac-)(填>、<或=).已知可逆反应CO+H2O(g)?CO2+H2,在一定条件下达到平衡状态.
(1)T℃时,若起始时:c(CO)=2mol/L,c(H2O)=3mol/L,平衡时CO的转化率为60%,此时平衡常数K值为
(2)T℃时,若起始时:c(CO)=2mol/L,c(H2O)=6mol/L,则水蒸气的转化率为
(3)若T℃时,起始浓度c(CO)=amol/L,c(H2O)=bmol/L,平衡时H2的浓度c(H2)=cmol/L,则a、b、c之间的关系式是
查看习题详情和答案>>
(1)T℃时,若起始时:c(CO)=2mol/L,c(H2O)=3mol/L,平衡时CO的转化率为60%,此时平衡常数K值为
1
1
;水蒸气的转化率为40%
40%
.(2)T℃时,若起始时:c(CO)=2mol/L,c(H2O)=6mol/L,则水蒸气的转化率为
25%
25%
(3)若T℃时,起始浓度c(CO)=amol/L,c(H2O)=bmol/L,平衡时H2的浓度c(H2)=cmol/L,则a、b、c之间的关系式是
ab=ac+bc
ab=ac+bc
.已知可逆反应CO+H2O(g) CO2+H2,达到平衡时,
CO2+H2,达到平衡时,
(1)830K时,若起始时:c (CO)=2mol/L,c (H2O)=3mol/L,平衡时CO的转化率为60%,水蒸气的转化率为
(2)830K,若只将起始时c (H2O)改为6mol/L,则水蒸气的为
(3)若830K时,起始浓度c (CO)=a mol/L,c (H2O)=b mol/L,H2的平衡浓度c (H2)=c mol/L,①a、b、c之间的关系式是
查看习题详情和答案>>
 CO2+H2,达到平衡时,
CO2+H2,达到平衡时,(1)830K时,若起始时:c (CO)=2mol/L,c (H2O)=3mol/L,平衡时CO的转化率为60%,水蒸气的转化率为
40%
40%
;K值为1
1
.(2)830K,若只将起始时c (H2O)改为6mol/L,则水蒸气的为
25%
25%
.(3)若830K时,起始浓度c (CO)=a mol/L,c (H2O)=b mol/L,H2的平衡浓度c (H2)=c mol/L,①a、b、c之间的关系式是
ab=ac+bc
ab=ac+bc
;②当a=b时,a=2
2
c.已知A、B、C是第二周期的非金属元素,其原子序数依次增大,且它们之间可以形成AC和BC以及AC2和BC2分子,D元素是一种短周期元素,它与A、B、C可分别形成电子总数相等的三种分子.请填空:
(1)写出A、B、C、D对应的元素符号:A 、B 、C 、D .
(2)写出工业生产中BD3与氧气反应的化学方程式: .
(3)你认为B、C、D元素形成的化合物之间 (填“能”或“不能”)发生下面的反应BC+BD3-→DBC2+D2C,得出上面结论的理由是 .
(4)Ⅰ.恒温恒压下,在一体积可变的密闭容器中发生下列反应:4AC(g)+2BC2(g)?4AC2(g)+B2(g)在上述条件下,向容器中充入AC和BC2各1mol达平衡时,生成AC2和B2共a mol,则AC的转化率是 (用含a的代数式表示).
Ⅱ.若维持温度不变,在一个与Ⅰ反应前的起始体积相同,容积固定的密闭容器中发生Ⅰ中所述的化学反应,开始时仍向容器中充入AC和BC2各1mol,达平衡时生成AC2和B2共b mol,将b与Ⅰ中的a进行比较,则a b(填“>”“<”“=”或“不能确定”).
查看习题详情和答案>>
(1)写出A、B、C、D对应的元素符号:A
(2)写出工业生产中BD3与氧气反应的化学方程式:
(3)你认为B、C、D元素形成的化合物之间
(4)Ⅰ.恒温恒压下,在一体积可变的密闭容器中发生下列反应:4AC(g)+2BC2(g)?4AC2(g)+B2(g)在上述条件下,向容器中充入AC和BC2各1mol达平衡时,生成AC2和B2共a mol,则AC的转化率是
Ⅱ.若维持温度不变,在一个与Ⅰ反应前的起始体积相同,容积固定的密闭容器中发生Ⅰ中所述的化学反应,开始时仍向容器中充入AC和BC2各1mol,达平衡时生成AC2和B2共b mol,将b与Ⅰ中的a进行比较,则a