摘要:15.一定温度下.难溶电解质的饱和溶液中各离子浓度幂的乘积是一个常数.这个常数称为该难溶电解质的溶度积.用符号Ksp表示. 如:AmBn(s) mAn+(aq)+nBm- = c(An+)m·c(Bm-)n 已知:某温度时.Ksp=1.8×10-10.Ksp(Ag2CrO4)=1.1×10-12 试求: ⑴此温度下AgCl饱和溶液的物质的量浓度为 .Ag2CrO4饱和溶液的物质的量浓度为 . ⑵此温度下.在0.010mo1·L-1的AgNO3溶液中.AgCl与Ag2CrO4分别能达到的最大物质的量浓度分别为 . .
网址:http://m.1010jiajiao.com/timu_id_4422281[举报]
(2010?启东市模拟)在水溶液中高价金属离子如:Fe3+、Al3+等会发生强烈水解,同样二价金属离子如Cu2+、Pb2+、Zn2+等离子在一定的pH范围内也可以水解.金属氢氧化物的沉淀直接受溶液pH的控制,利用这一方法可以除去工业污水中的某些金属离子.下图是Zn(OH)2的在某温度时的沉淀区域曲线图
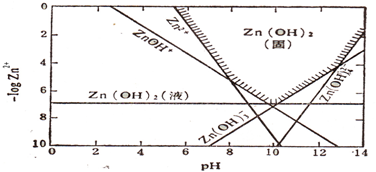
请回答下列问题:
(1)向一定浓度的Zn2+的溶液中加入足量的NaOH固体,下列说法正确的是
A、一定产生沉淀 B、先产生沉淀,后沉淀消失
C、一定不产生沉淀 D、可能不产生沉淀
(2)当pH=6、c(Zn2+)=0.01mol?L-1,Zn2+主要存在形式为
(3)向c(Zn2+)=1×10-5mol?L-1的溶液中加入固体NaOH到pH=10和pH=13,写出有关反应的离子方程式:①
(4)已知该温度下的Ksp[Zn(OH)2]=1×10-17,计算:当溶液中的c(Zn2+)=1×10-5mol?L-1,向溶液中加入NaOH固体,产生沉淀的pH,并对照该图判断是否真的产生沉淀?原因可能是什么?
查看习题详情和答案>>

请回答下列问题:
(1)向一定浓度的Zn2+的溶液中加入足量的NaOH固体,下列说法正确的是
D
D
A、一定产生沉淀 B、先产生沉淀,后沉淀消失
C、一定不产生沉淀 D、可能不产生沉淀
(2)当pH=6、c(Zn2+)=0.01mol?L-1,Zn2+主要存在形式为
ZnOH+
ZnOH+
、Zn(OH)2液体
Zn(OH)2液体
.(3)向c(Zn2+)=1×10-5mol?L-1的溶液中加入固体NaOH到pH=10和pH=13,写出有关反应的离子方程式:①
Zn2++2OH-═Zn(OH)2↓
Zn2++2OH-═Zn(OH)2↓
;②Zn2++4OH-═Zn(OH)2-4
Zn2++4OH-═Zn(OH)2-4
(4)已知该温度下的Ksp[Zn(OH)2]=1×10-17,计算:当溶液中的c(Zn2+)=1×10-5mol?L-1,向溶液中加入NaOH固体,产生沉淀的pH,并对照该图判断是否真的产生沉淀?原因可能是什么?
(2010?启东市模拟)某种芳香族化合物A,其蒸气密度是相同条件下H2密度的82倍.A由碳、氢、氧三种元素组成,经测定碳、氢的质量分数分别为
73.2%和7.32%.
(1)A的分子式是
(2)已知:
ⅰ. (R1、R2、R3代表烃基)
(R1、R2、R3代表烃基)
ⅱ.
又知,A在一定条件下能发生如下转化,某些生成物(如H2O等)已略去.

请回答:
①步骤Ⅰ的目的是
②若G为碳酸,则E的结构简式是
④F在一定条件下可发生酯化反应,生成M(M与FeCl3反应,溶液呈紫色;且分子结构中含有苯环和一个七元环)请写出该反应的化学方程式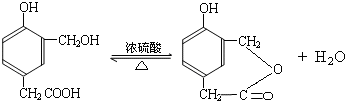
 ;
;
⑤A的结构简式是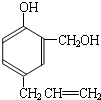
 ;上述转化中B→D的化学方程式是
;上述转化中B→D的化学方程式是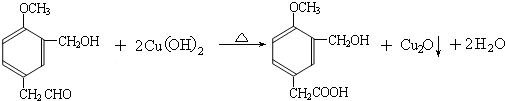
 .
.
(3)已知A的某种同分异构体N具有如下性质:
①N与FeCl3反应,溶液呈紫色;
②N在一定条件下可发生银镜反应,N与H2在苯环侧链上按照物质的量之比1:1作用后的生成物不能发生消去反应;
③在通常情况下,1mol N能与含1mol Br2的浓溴水发生取代反应;
④N分子中苯环上的取代基上无支链.
请写出:N可能的结构简式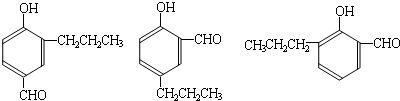
 (写一种即可).
(写一种即可).
(4)请设计合理方案,完成从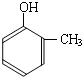 到的合成
到的合成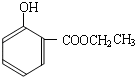 路线(用合成路线流程图表示,并注明反应条件).
路线(用合成路线流程图表示,并注明反应条件).
提示:①;合成过程中无机试剂任选;②合成路线流程图示例如下:
CH3CH2OH
CH2=CH2

查看习题详情和答案>>
73.2%和7.32%.
(1)A的分子式是
C10H12O2
C10H12O2
.(2)已知:
ⅰ.
 (R1、R2、R3代表烃基)
(R1、R2、R3代表烃基)ⅱ.

又知,A在一定条件下能发生如下转化,某些生成物(如H2O等)已略去.

请回答:
①步骤Ⅰ的目的是
保护酚羟基
保护酚羟基
;②若G为碳酸,则E的结构简式是
HCOOH
HCOOH
③F→H的反应类型是缩聚反应
缩聚反应
;④F在一定条件下可发生酯化反应,生成M(M与FeCl3反应,溶液呈紫色;且分子结构中含有苯环和一个七元环)请写出该反应的化学方程式


⑤A的结构简式是




(3)已知A的某种同分异构体N具有如下性质:
①N与FeCl3反应,溶液呈紫色;
②N在一定条件下可发生银镜反应,N与H2在苯环侧链上按照物质的量之比1:1作用后的生成物不能发生消去反应;
③在通常情况下,1mol N能与含1mol Br2的浓溴水发生取代反应;
④N分子中苯环上的取代基上无支链.
请写出:N可能的结构简式


(4)请设计合理方案,完成从
 到的合成
到的合成 路线(用合成路线流程图表示,并注明反应条件).
路线(用合成路线流程图表示,并注明反应条件).提示:①;合成过程中无机试剂任选;②合成路线流程图示例如下:
CH3CH2OH
| 浓H2SO4 |
| 170℃ |
| 高温、高压 |
| 催化剂 |

(2010?启东市模拟)联合国气候变化大会于2009年12月7-18日在哥本哈根召开.中国政府承诺,到2020
年,单位GDP二氧化碳排放比2005年下降40%~45%.
(1)有效“减碳”的手段之一是节能.下列制氢方法最节能的是
A.电解水制氢:2H2O
2H2↑+O2↑ B.高温使水分解制氢:2H2O
2H2↑+O2↑
C.太阳光催化分解水制氢:2H2O
2H2↑+O2↑
D.天然气制氢:CH4+H2O
CO+3H2
(2)CO2可转化成有机物实现碳循环.在体积为1L的密闭容器中,充入1mol CO2和3mol H2,一定条件下发生反应: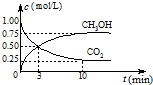
CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ/mol,测得CO2和CH3OH(g)的浓度随时间变化如图所示.
①从3min到10min,v(H2)=
②能说明上述反应达到平衡状态的是
A.反应中CO2与CH3OH的物质的量浓度之比为1:1(即图中交叉点)
B.混合气体的密度不随时间的变化而变化
C.单位时间内每消耗3mol H2,同时生成1mol H2O
D.CO2的体积分数在混合气体中保持不变
③下列措施中能使n (CH3OH)/n (CO2)增大的是
A.升高温度B.恒温恒容充入He(g)
C.将H2O(g)从体系中分离 D.恒温恒容再充入1mol CO2和3mol H2
④相同温度下,如果要使氢气的平衡浓度为1mol/L,则起始时应向容器中充入1mol CO2和
(参考数据:
=2.64;
=21.166.计算结果请保留3位有效数字.)
(3)CO2加氢合成DME(二甲醚)是解决能源危机的研究方向之一.
2CO2(g)+6H2(g)→CH3OCH3(g)+3H2O.有人设想利用二甲醚制作燃料电池,
以KOH溶液做电解质溶液,试写出该电池工作时负极反应的电极反应方程式
查看习题详情和答案>>
年,单位GDP二氧化碳排放比2005年下降40%~45%.
(1)有效“减碳”的手段之一是节能.下列制氢方法最节能的是
C
C
.(填字母序号)A.电解水制氢:2H2O
| ||
| ||
C.太阳光催化分解水制氢:2H2O
| ||
| 太阳光 |
D.天然气制氢:CH4+H2O
| 高温 |
(2)CO2可转化成有机物实现碳循环.在体积为1L的密闭容器中,充入1mol CO2和3mol H2,一定条件下发生反应:

CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ/mol,测得CO2和CH3OH(g)的浓度随时间变化如图所示.
①从3min到10min,v(H2)=
0.11
0.11
mol/(L?min).②能说明上述反应达到平衡状态的是
D
D
(选填编号).A.反应中CO2与CH3OH的物质的量浓度之比为1:1(即图中交叉点)
B.混合气体的密度不随时间的变化而变化
C.单位时间内每消耗3mol H2,同时生成1mol H2O
D.CO2的体积分数在混合气体中保持不变
③下列措施中能使n (CH3OH)/n (CO2)增大的是
CD
CD
(选填编号).A.升高温度B.恒温恒容充入He(g)
C.将H2O(g)从体系中分离 D.恒温恒容再充入1mol CO2和3mol H2
④相同温度下,如果要使氢气的平衡浓度为1mol/L,则起始时应向容器中充入1mol CO2和
3.58
3.58
mol H2,平衡时CO2的转化率为86.1%
86.1%
.(参考数据:
| 7 |
| 448 |
(3)CO2加氢合成DME(二甲醚)是解决能源危机的研究方向之一.
2CO2(g)+6H2(g)→CH3OCH3(g)+3H2O.有人设想利用二甲醚制作燃料电池,
以KOH溶液做电解质溶液,试写出该电池工作时负极反应的电极反应方程式
C2H6O+16OH--12e-═2CO32-+11H2O
C2H6O+16OH--12e-═2CO32-+11H2O
.(2010?启东市模拟)过碳酸钠是一种有多用途的新型氧系漂白剂,化学式可表示为aNa2CO3?bH2O2.现将一定质量的过碳酸钠粉末溶于水配成稀溶液,再向其中加入适量MnO2粉末,充分反应后生成672mL气体(标准状况).反应后的混合物经过滤、洗涤后,将滤液和洗涤液混合并加水配成100mL溶液A.现向三份体积为10mL、浓度为cmol/L的稀硫酸中分别逐滴滴入溶液A,边滴边振荡,充分反应后,测得实验数据如下表所示:
(1)计算稀硫酸的物质的量浓度.
(2)通过计算确定过碳酸钠的化学式.
(3)工业上常以所含活性氧的质量分数[w(活性氧)=
×100%]来衡量过碳酸钠产品的优劣,13%以上者为优等品.现将0.2g某厂家生产的过碳酸钠样品(所含杂质不参与后面的氧化还原反应)溶于水配成溶液,加入15.0mL 1mol/L硫酸,再加入足量KI,摇匀后置于暗处,充分反应后,加入少量淀粉试液,用0.1mol/L Na2S2O3溶液滴定到蓝色恰好消失时,共消耗30.00mL,试计算判断该样品是否为优等品.(已知:2Na2S2O3+I2→Na2S4O6+2NaI)
查看习题详情和答案>>
| 实验序号 | Ⅰ | Ⅱ | Ⅲ |
| 滴加溶液A的体积/mL | 10.0 | 20.0 | 30.0 |
| 生成气体的体积/mL(标准状况) | 89.6 | 179.2 | 224 |
(2)通过计算确定过碳酸钠的化学式.
(3)工业上常以所含活性氧的质量分数[w(活性氧)=
| 16n(H2O2) |
| m(样品) |