摘要:1.构造原理:绝大多数基态原子核外电子的排布都遵循下列顺序: 1s.2s.2p.3s.3p. . .4p.5s.4d.5p.6s.4f-- 构造原理揭示了原子核外电子的能级分布.从中可以看出.不同能层的能级有交错现象.如E(3d)>E(4s).E(4d)>E(5s).E(5d)>E(6s).E(6d)>E(7s).E(4f)>E(5p).E(4f)>E(6s)等. 构造原理是书写基态原子电子排布式的依据.也是绘制基态原子电子排布图的主要依据之一. 思考:如何快速判断不同能级的能量高低?
网址:http://m.1010jiajiao.com/timu_id_4421358[举报]
下列说法中正确的是:( )
①所有基态原子的核外电子排布都遵循构造原理
②同一周期从左到右,元素的第一电离能、电负性都是越来越大
③金属键、共价键和氢键都具有相同的特征:方向性和饱和性
④所有的配合物都存在配位键,所有含配位键的化合物都是配合物
⑤所有含极性键的分子都是极性分子
⑥所有金属晶体中都含有金属键
⑦所有的金属晶体熔点肯定高于分子晶体.
①所有基态原子的核外电子排布都遵循构造原理
②同一周期从左到右,元素的第一电离能、电负性都是越来越大
③金属键、共价键和氢键都具有相同的特征:方向性和饱和性
④所有的配合物都存在配位键,所有含配位键的化合物都是配合物
⑤所有含极性键的分子都是极性分子
⑥所有金属晶体中都含有金属键
⑦所有的金属晶体熔点肯定高于分子晶体.
| A、③⑥⑦ | B、⑥ | C、③④⑤ | D、①②⑥⑦ |
 (1)多电子原子核外电子能量是不同的,其中能层序数(n)越小,该能层能量
(1)多电子原子核外电子能量是不同的,其中能层序数(n)越小,该能层能量越低
越低
,在同一能层中,各能级的能量按ns、np、nd、nf的次序递增
递增
.(2)原子的电子排布遵循构造原理能使整个原子的能量处于最低状态,处于最低能量的原子叫做
基态
基态
原子,当这些原子吸收
吸收
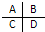
能量后电子跃迁到较高能级后就变成激发态.(3)如图是周期表中短周期主族元素的一部分,其中电负性最大的元素是
B
B
.第一电离能最小的元素是C或D
C或D
.(1)实验室由纯净的铜屑制胆矾(CuSO4?5H2O)的实验流程如下:
溶解铜屑一种方案是:将铜屑加入到稀硫酸与双氧水的混和液中并用30~40℃水浴加热,一段时间后,铜完全溶解,得到硫酸铜溶液.该反应的化学方程式为
(2)目前我国的火力发电机组绝大多数为燃煤机组,而以燃煤为主的电力生产所造成的环境污染是制约电力工业发展的一个重要因素,其中氮氧化物(NOx)是继粉尘和二氧化硫之后燃煤电站环保治理的重点.
①燃煤烟气脱硫的方法很多,如石灰石-石膏法、氨水法等.其中石灰石-石膏法脱硫的原理第一步是SO2+Ca(OH)2=CaSO3+H2O,然后再将产物氧化制成石膏,写出该反应的化学方程式
②燃煤烟气脱硝可采用氨(NH3)作为还原介质,在催化剂及氧气存在的条件下,氮氧化物(NOx)与还原剂发生反应,生成无害的氮气和水,写出二氧化氮与氨反应的化学方程式
查看习题详情和答案>>

溶解铜屑一种方案是:将铜屑加入到稀硫酸与双氧水的混和液中并用30~40℃水浴加热,一段时间后,铜完全溶解,得到硫酸铜溶液.该反应的化学方程式为
H2SO4+H2O2+Cu=CuSO4+2H2O
H2SO4+H2O2+Cu=CuSO4+2H2O
,反应温度不能超过40℃的原因是防止双氧水分解
防止双氧水分解
,由硫酸铜溶液获得胆矾的操作依次为蒸发(浓缩)
蒸发(浓缩)
、冷却结晶、过滤
过滤
、洗涤、干燥.(2)目前我国的火力发电机组绝大多数为燃煤机组,而以燃煤为主的电力生产所造成的环境污染是制约电力工业发展的一个重要因素,其中氮氧化物(NOx)是继粉尘和二氧化硫之后燃煤电站环保治理的重点.
①燃煤烟气脱硫的方法很多,如石灰石-石膏法、氨水法等.其中石灰石-石膏法脱硫的原理第一步是SO2+Ca(OH)2=CaSO3+H2O,然后再将产物氧化制成石膏,写出该反应的化学方程式
2CaSO3+O2=2CaSO4
2CaSO3+O2=2CaSO4
.②燃煤烟气脱硝可采用氨(NH3)作为还原介质,在催化剂及氧气存在的条件下,氮氧化物(NOx)与还原剂发生反应,生成无害的氮气和水,写出二氧化氮与氨反应的化学方程式
6NO2+8NH3=7N2+12H2O
6NO2+8NH3=7N2+12H2O
.下列有关说法正确的是( )
| A、同一原子的S能级电子云形状完全一样 | B、原子的价层电子发生跃迁只能吸收能量,得到吸收光谱 | C、某基态原子电子排布式为1s22s22p63s23px23py1违反了泡利原理 | D、某基态原子电子排布式为1s22s22p63s23p63d54s1违反了构造原理,但符合能量最低原理 |
下列说法中正确的是( )
| A、SO2和O3、PO43-和C1O4-互为等电子体 | B、甲烷分子失去一个H+,形成CH3-,其碳原子的杂化类型发生了改变 | C、CH4、BCl3、SO2都是含有极性键的非极性分子 | D、所有元素的基态原子核外电子排布都遵循构造原理 |