摘要:[例4]试从不同角度解释:乙醇(C2H5OH)和二甲醚(CH3OCH3)的化学组成均为C2H6O.但乙醇的沸点为78.5℃.而二甲醚的沸点为-23℃? 解析:乙醇(C2H5OH)和二甲醚(CH3OCH3)的化学组成相同.两者的相对分子质量也相同.不同的是二者的极性.对称性不同.且乙醇能满足氢键的形成条件.从不同点加以解释. 答案:①乙醇的极性强.分子间作用力大.沸腾时需要提供更多的能量去破坏分子间作用力②乙醇分子之间能形成氢键.使分子间产生了较强的结合力.沸腾时需要提供更多的能量去破坏分子间氢键.而二甲醚分子间没有氢键.上述两点使乙醇的沸点比二甲醚的高.
网址:http://m.1010jiajiao.com/timu_id_441927[举报]
我国高校目前联合研究一种稀土制冷材料,其主要成分是LaCaMnO.
(1)猛原子的基态价层电子排布式为
(2)S与O为同主族元素,其中电负性较大的是 ; H2S分子中S原子杂化轨道类型为 ;试从结构角度解释H2SO4的酸性大于H2SO3的酸性: .
(3)据报道,Ca在空气中点燃生成CaO和少量Ca2N2.
①Ca2N2和水反应生成NH2-NH2,NH2-NH2能否作配体? (填“能”或“否”)
②CaO形成的晶体与NaCl晶体一样,为面心立方最密堆积,则一个CaO晶胞中含 有Ca2+数为 ;欲比较CaO与NaCl的晶格能大小,需考虑的数据是 .
查看习题详情和答案>>
(1)猛原子的基态价层电子排布式为
(2)S与O为同主族元素,其中电负性较大的是
(3)据报道,Ca在空气中点燃生成CaO和少量Ca2N2.
①Ca2N2和水反应生成NH2-NH2,NH2-NH2能否作配体?
②CaO形成的晶体与NaCl晶体一样,为面心立方最密堆积,则一个CaO晶胞中含 有Ca2+数为
我国高校目前联合研究一种稀土制冷材料,其主要成分是LaCaMnO。
(1)锰原子的基态价层电子排布式为______
(2)S与O为同主族元素,其中电负性较大的是____________; H2S分子中S原子杂化轨道类型为______;试从结构角度解释H2SO4的酸性大于H2SO3的酸性:_______。
(3)据报道,Ca在空气中点燃生成CaO和少量Ca2N2。
①Ca2N2和水反应生成NH2-NH2,NH2—NH2能否作配体?______(填“能”或“否”)
②CaO形成的晶体与NaCl晶体一样,为面心立方最密堆积,则一个CaO晶胞中含 有Ca2+数为______ ;欲比较CaO与NaCl的晶格能大小,需考虑的数据是______。
查看习题详情和答案>>
(三选一)【物质结构与性质】
(1)金属钛(22Ti)将是继铜、铁、铝之后人类广泛使用的第四种金属,写出钛元素的基态原核外电子排布式:_______________
(2)日常生活中广泛应用的不锈钢,在其生产过程中添加了铬元素,该元素基态原子未成对电子数为_____________。
(3)COCl2俗称光气,分子中碳原子采取_____________杂化成键;其中碳氧原子之间的共价键含有____(填字母)。
a.2个σ键 b.2个π键 c.1个σ键、1个π键
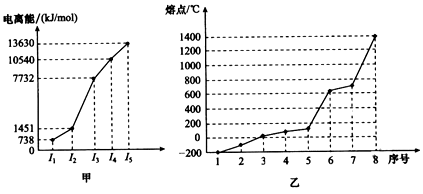
(4)①短周期某主族元素M的逐级电离能情况如图甲所示,则M元素形成化合物时表现的主要化合价为______价。
②第三周期8种元素按单质熔点高低的顺序如图乙所示,其中序号“8”代表_______(填元素符号,下同);其中电负性最大的是_________。
(1)金属钛(22Ti)将是继铜、铁、铝之后人类广泛使用的第四种金属,写出钛元素的基态原核外电子排布式:_______________
(2)日常生活中广泛应用的不锈钢,在其生产过程中添加了铬元素,该元素基态原子未成对电子数为_____________。
(3)COCl2俗称光气,分子中碳原子采取_____________杂化成键;其中碳氧原子之间的共价键含有____(填字母)。
a.2个σ键 b.2个π键 c.1个σ键、1个π键
(4)①短周期某主族元素M的逐级电离能情况如图甲所示,则M元素形成化合物时表现的主要化合价为______价。
②第三周期8种元素按单质熔点高低的顺序如图乙所示,其中序号“8”代表_______(填元素符号,下同);其中电负性最大的是_________。
(5)由碳原子跟硅原子以1:1相互交替结合而形成的晶体,晶型与晶体Si相同。两者相比熔点更高的是________(填化学式),试从结构角度加以解释:______________
(6)在配合物Fe(SCN)2+中,提供空轨道接受孤对电子的微粒是_________________
查看习题详情和答案>>
(6)在配合物Fe(SCN)2+中,提供空轨道接受孤对电子的微粒是_________________
(10分)今有下列两组单质,试将每组单质从不同角度进行“分类”,每种“分类”都可分别挑出一种单质,它跟其他三种单质属于不同的“类”,将挑出的单质(写化学符号)和挑选依据(写编码)列在下面相应的表格内:
两组单质为:Ⅰ.O2、F2、S、N2 Ⅱ.Fe、Na、Al、Si
“挑选依据”仅限于下述六种。该被挑出的单质跟其他三种单质不同,是由于:(A)其组成元素不属于金属(或非金属);(B)其组成元素不属于周期表中的同一族;(C)其组成元素不属于周期表中的同一周期;(D)其组成元素不属于主族(或副族)元素;(E)在常温常压下呈不同物态;(F)在常温下遇水能(或不能)迅速产生气体。
|
|
答案1 |
答案2 |
答案3 |
答案4 |
答案5 |
答案6 |
|
单质 |
Si |
|
|
|
|
|
|
挑选依据 |
A |
|
|
|
|
|
查看习题详情和答案>>