网址:http://m.1010jiajiao.com/timu_id_438661[举报]
第I卷(选择题,共48分)
一、选择题(共48分,每小题2 分,共24小题,每小题只有一个正确答案)
13 D 14 D
第II卷(非选择题,共52 分)
二、填空题(共23个空,每空2分,共46分)
25. CO2 NH3 CO2
26. ⑴ ②④ ;⑵ ①⑥; ⑶ ⑤
27.氧化剂 酸性 还原剂,酸性
28.不褪色 SO2 + Cl2 + 2H2O = 2HCl + H2SO4
29. H+ + HCO3― = H2O+ CO2↑
CO2 + 2OH― = H2O + CO32―
CO2 + CO32― + H2O = 2HCO3―
 30.(1) A:BaCl2 B:FeSO
30.(1) A:BaCl2 B:FeSO
(2) FeSO4 + 2NaOH = Fe(OH)2↓+ Na2SO4, 4 Fe(OH)2 + O2 + 2H2O = 4Fe(OH)3
(3)Al3+ + 3OH- = Al(OH)3↓, Al(OH)3 + OH- = AlO2- + 2H2O
三、计算题(写出必要的计算过程。6分)
31.解:设原NaNO3溶液的质量为x,则22%x=(100+x)14%,解得x=
所以,m(NaNO3) =
c(NaNO3) = n(NaNO3)/V(aq)
= 3.02mol/L …………………………………………… ……... 3分
 w.w.w.k.s.5.u.c.o.m
w.w.w.k.s.5.u.c.o.m
www.ks5u.com
|
下列各物质中,所含氧原子个数最多的是 | |
| [ ] | |
A. |
1 mol KClO3 |
B. |
49 g H2SO4 |
C. |
22.4 L O2(标准状况下) |
D. |
3.01×1023个CO2 |
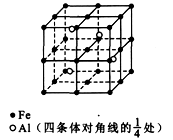
(2)若晶体的密度为ρg/cm3,则此合金中最近的两个Fe原子之间的距离(用含ρ的代数式表示,不必化简)为____cm。
(3)取2.78 g该合金粉末溶于100 mL某稀硝酸溶液中,待反应完全后得到1.12 L NO气体(标准状况,且设两者恰好完全反应),则原硝酸溶液的物质的量浓度为______moL/L,反应后溶液中Fe3+的物质的量浓度为__________mol/L。
某化学课外兴趣小组探究铜与浓硫酸的反应情况及某些产物的性质。
(Ⅰ)甲、乙两同学进行了下列实验:取一定量的铜片和20 mL 18 mol/L的浓硫酸放在圆底烧瓶中共热,直至反应完毕,最后发现烧瓶中还有铜片剩余,同时根据所学的知识认为还有较多硫酸剩余。
(1)铜与浓硫酸反应的化学方程式是:
可以证明有余酸的实验方案是_ (填字母)。
a.再加入适量NaNO3固体B.再滴入BaCl2溶液 C.再加入银 D.再滴入Na2CO3溶液
(2)甲同学设计求余酸浓度的实验方案是测定产生气体的量。下列方案中不可行的是 (填字母)。
a.将产生的气体缓缓通过预先称量的盛有碱石灰的干燥管,反应结束后再次称量
b.将产生的气体缓缓通入酸性高锰酸钾溶液,再加入足量BaCl2溶液,过滤、洗涤、干燥、称量沉淀
c.用排水法测定其产生气体的体积(折算成标准状况)
d.用排饱和NaHSO3溶液的方法测出其产生气体的体积(折算成标准状况)
(3)乙同学设计测定余酸浓度的实验方案是:测定反应后的混合液中Cu2+的量。在反应后的溶液中加入足量Na2S溶液,充分反应后,过滤、洗涤、干燥、称量沉淀的质量为W g,测得反应后溶液的体积为V mL。则剩余硫酸的物质的量浓度为 mol/L(用含W、V的代数式表示)。
(Ⅱ)丙同学探究SO2与BaCl2溶液能否反应生成白色BaSO3沉淀。
丙同学先将产生的气体通过盛有饱和NaHSO3溶液的洗气瓶,再缓缓通入BaCl2溶液中,观察到有少量白色沉淀生成,检验白色沉淀,发现沉淀全部不溶于稀盐酸,该沉淀的生成表明SO2具有 性。用一个离子方程式解释生成此沉淀的原因 。
查看习题详情和答案>>
某化学课外兴趣小组探究铜与浓硫酸的反应情况及某些产物的性质。
(Ⅰ)甲、乙两同学进行了下列实验:取一定量的铜片和20 mL 18 mol/L的浓硫酸放在圆底烧瓶中共热,直至反应完毕,最后发现烧瓶中还有铜片剩余,同时根据所学的知识认为还有较多硫酸剩余。
(1)铜与浓硫酸反应的化学方程式是:
可以证明有余酸的实验方案是_ (填字母)。
a.再加入适量NaNO3固体B.再滴入BaCl2溶液 C.再加入银 D.再滴入Na2CO3溶液
(2)甲同学设计求余酸浓度的实验方案是测定产生气体的量。下列方案中不可行的是 (填字母)。
a.将产生的气体缓缓通过预先称量的盛有碱石灰的干燥管,反应结束后再次称量
b.将产生的气体缓缓通入酸性高锰酸钾溶液,再加入足量BaCl2溶液,过滤、洗涤、干燥、称量沉淀
c.用排水法测定其产生气体的体积(折算成标准状况)
d.用排饱和NaHSO3溶液的方法测出其产生气体的体积(折算成标准状况)
(3)乙同学设计测定余酸浓度的实验方案是:测定反应后的混合液中Cu2+的量。在反应后的溶液中加入足量Na2S溶液,充分反应后,过滤、洗涤、干燥、称量沉淀的质量为W g,测得反应后溶液的体积为V mL。则剩余硫酸的物质的量浓度为 mol/L(用含W、V的代数式表示)。
(Ⅱ)丙同学探究SO2与BaCl2溶液能否反应生成白色BaSO3沉淀。
丙同学先将产生的气体通过盛有饱和NaHSO3溶液的洗气瓶,再缓缓通入BaCl2溶液中,观察到有少量白色沉淀生成,检验白色沉淀,发现沉淀全部不溶于稀盐酸,该沉淀的生成表明SO2具有 性。用一个离子方程式解释生成此沉淀的原因 。