网址:http://m.1010jiajiao.com/timu_id_437329[举报]
一、(每题2分,共10分)w.w.w.k.s.5.u.c.o.m
1.D 2.B 3.C 4.D 5.A
二、(每题3分,共36分)
6.B 7.B 8.A 9.C 10.A 11.D 12.C 13.D 14.C 15.D 16.B 17.A
三、(每题4分,共20分)
18.B、D 19.B、C 20.A、C 21.A、D 22.B、C
四、(本题共24分)
23.(本题8分,每格1分)(1)1s22s22p3 第2周期ⅣA族
(2)
(3)两性
H++AlO2?+H2O.files/image034.gif) Al(OH)3
Al(OH)3.files/image034.gif) Al3++3OH?
Al3++3OH?
(4)非极性 CH4(g)+2O2(g) → CO2(g) +2H2O(l) +890.3kJ
24.(本题8分)
(1) 24e
.files/image035.gif) ↓ │
(配平2分,电子转移方向和数目各1分,共4分)
↓ │
(配平2分,电子转移方向和数目各1分,共4分)
12Cl2+15NH3→ 4 N2+ 7 NH4Cl + 17 HCl
(2)NH3(1分),NH4Cl 和HCl(各1分,共2分) (3)0.08(1分)
25.(本题8分,除指明外,每格1分)(1)0.05 mol/(L•min) (无单位不得分) >
(2)1 扩大容器体积(或减小压强) (3)= (4)放热 (2分) (5)20~40
五、(本题共24分)
26.(本题10分,除指明外,每格1分)
(1)CN-+ClO-→CNO-+Cl? ,2CNO-+6ClO?+8H+→N2↑+2CO2↑+3Cl2↑+4H2O
(2)浓硫酸, 除去Cl2 , 吸收CO2 , 防止空气中的CO2、水蒸气进入,干扰实验
(3)偏低,装置中残留有CO2未被完全吸收 (4)80%(2分)
27.(本题14分,除指明外,每格1分)
(1)反应速率突然减小(或铁片表面生成的气泡突然减少) e .files/image037.gif)
(2)洗涤、烘干(或干燥) 过滤
(3)b、d(各1分,共2分),加快铁片与硫酸的反应速率,Fe和Cu(1分,有缺不得分)
(4)抑制Fe2+、NH4+水解 (5)避免加热过程中晶体受热分解(或被氧化)
(6)b、d(各1分,共2分)
.files/image039.gif) 六、(本题共20分)
六、(本题共20分).files/image023.gif) w.w.w.k.s.5.u.c.o.m
w.w.w.k.s.5.u.c.o.m
28.(本题8分,除指明外,每格1分)(1)取代反应,加聚反应 (2) CH2== CH2
.files/image041.gif) (3)CH2== CH―CH2Cl + Br2 →
(3)CH2== CH―CH2Cl + Br2 →.files/image043.gif) (2分) (4)5 、
(2分) (4)5 、
29.(本题12分)(1)1,2―二溴乙烷(1分), .files/image045.gif) (1分)
(1分)
(2)取代反应(1分),NaOH醇溶液、加热(1分)
.files/image046.gif) (3)n
(3)n.files/image048.gif)
.files/image050.gif) (2分)
(2分)
.files/image051.gif) (4)
(4).files/image053.gif) +
+ .files/image045.gif)
.files/image055.gif) +
H2O(2分)
+
H2O(2分)
(5).files/image057.gif) (2分) (6)5(2分)
(2分) (6)5(2分)
七、(本题共16分).files/image023.gif) w.w.w.k.s.5.u.c.o.m
w.w.w.k.s.5.u.c.o.m
30. (1)1:3 (2分) (2)3.2(2分) (3)6048 (2分)
解:(1)Fe+2HCl→FeCl2+H2↑ n(H2)=.files/image059.gif) =0.005(mol) ∴ n(Fe)=0.005(mol)
=0.005(mol) ∴ n(Fe)=0.005(mol)
m(Fe) =0.005×56=0.28(g) ∴ m(FeS)=1.6?0.28=1.32(g) n(FeS) =.files/image061.gif) =0.015(mol)
=0.015(mol)
∴ n(Fe):n(FeS) = 0.005:0.015= 1:3
(2)300mL溶液种最多溶解H2S:n(H2S) =0.1×0.3=0.03(mol)
∴ n(FeS)= n(H2S)=0.03(mol) n(Fe)=0.01(mol)
∴ m(Fe)+m(FeS)= 0.01×56+0.03×88=3.2(g)
(3)当a=
若全部反应需盐酸:2×(0.3+0.1) =0.8 (mol) > 2×0.3=0.6(mol)
∴ 盐酸不足,以盐酸的量为计算标准
∴ 产生的H2、H2S共为:n(气体)=.files/image063.gif) n(HCl) =
n(HCl) =.files/image063.gif) ×0.6=0.3(mol),
×0.6=0.3(mol),
其中0.03mol的H2S溶解于溶液
∴ 收集到的气体为:0.3?0.03=0.27 (mol)
V(气体)=0.27×22.4=6.048(L)=6048mL
31.(1)c、d (2分) (2)①2NO2 + Na2CO3 → NaNO2 + NaNO3 + CO2(1分)
②.files/image065.gif) ≥
≥.files/image067.gif) (或
(或.files/image069.gif) (2分)③1:5 (3分)
(2分)③1:5 (3分)
解:(2)②将20%的N2O4看作成2份NO2,即NO2共有
若气体恰好被吸收则:.files/image065.gif) ≥
≥.files/image067.gif)
生成的产物NaNO2、NaNO3中钠原子与氮原子均为1:1,所以由原子守恒得:
n(Na2CO3)=.files/image063.gif) n(Na)=
n(Na)=.files/image063.gif) n(N)=
n(N)=.files/image063.gif) [n(NO2)+n(NO)]=
[n(NO2)+n(NO)]=.files/image063.gif) ×
×.files/image071.gif) =
=.files/image073.gif) (mol)
(mol)
∴ c(Na2CO3)= .files/image073.gif) ÷0.2=
÷0.2=.files/image076.gif) (mol/L)
(mol/L)
③设:
.files/image077.gif) x+y+z=
x+y+z=.files/image079.gif) =0.09
解得: x=0.01(mol)
=0.09
解得: x=0.01(mol)
2x+y+3z=.files/image081.gif) ×4 (得失电子守恒)
y=0.05(mol)
×4 (得失电子守恒)
y=0.05(mol)
.files/image077.gif) 2x+y+z=0.05×2 (氮原子、钠原子守恒) z=0.03(mol)
2x+y+z=0.05×2 (氮原子、钠原子守恒) z=0.03(mol)
∴ V(N2O4):V(NO2) = n(N2O4):n(NO2) =x:y= 1:5
①实验室配制氯化亚铁溶液时,将氯化亚铁先溶解在盐酸中,然后用蒸馏水稀释并加入少量铁粉.
②配制一定浓度的溶液时,俯视容量瓶的刻线,会使配制的浓度偏高;实验室测定中和热时,过早读数会使测定结果偏低.
③将Fe2(SO4)3溶液加热蒸发至干并灼烧,最后得到红棕色粉末
④实验室用铜片与稀硝酸反应产生的气体可用排水法收集
⑤试管中加入少量淀粉,再加入一定量稀硫酸,加热3-4分钟,然后加入银氨溶液,片刻后管壁上有“银镜”出现
⑥向氨水中滴加Al2(SO4)3溶液和向Al2(SO4)3溶液中滴加氨水现象相同
⑦苯与溴水在铁粉的催化作用下制备溴苯
⑧分别向体积和pH均相同的盐酸和醋酸中滴加等浓度的氢氧化钠溶液,完全中和时消耗的氢氧化钠溶液的体积一样多
Ⅱ氟化钠是一种重要的氟盐,主要用于农作物杀菌、杀虫、木材的防腐.实验室可通过下图所示的流程以氟硅酸(H2SiF6)等物质为原料制取氟化钠,并得到副产品氯化铵;
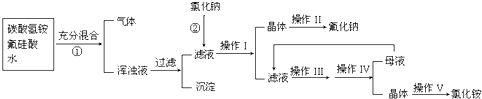
已知:20℃时氯化铵的溶解度为37.2g,氟化钠的溶解度为4g.Na2SiF6微溶于水.请回答下列问题:
(1)上述流程①中产生浑浊的原因是生成了
A.NH4F B.H2SiO3C.(NH4)2SiF6 D.(NH4)2CO3
(2)写出流程②中相关的化学方程式:
(3)操作I和操作
(4)流程①中NH4HCO3必须过量,其原因是
(Ⅰ)下列实验操作或对实验事实的描述正确的是 (填序号);
① 实验室配制氯化亚铁溶液时,将氯化亚铁先溶解在盐酸中,然后用蒸馏水稀释并加入少量铁粉。
② 配制一定浓度的溶液时,俯视容量瓶的刻度线,会使配制的浓度偏高;实验室测定中和热时,过早读数会使测定结果偏低。
③ 将Fe2(SO4)3溶液加热蒸发至干并灼烧,最后得到红棕色粉末
④ 实验室用铜片与稀硝酸反应产生的气体可用排水法收集
⑤ 试管中加入少量淀粉,再加入一定量稀硫酸,加热3-4分钟,然后加入银氨溶液,片刻后管壁上有“银镜”出现
⑥ 向氨水中滴加Al2(SO4)3溶液和向Al2(SO4)3溶液中滴加氨水现象相同
⑦ 苯与溴水在铁粉的催化作用下制备溴苯
⑧ 分别向体积和pH均相同的盐酸和醋酸中滴加等浓度的氢氧化钠溶液,完全中和时消耗的氢氧化钠溶液的体积一样多
Ⅱ.在中学化学实验中,通常用无水硫酸铜来检验少量水的存在。由于无水硫酸铜吸湿性很强,需要现制现用。
方法甲:取2药匙细小的硫酸铜晶体置于_______中研碎后放入坩埚,将坩埚放在______上用小火慢慢加热并用玻璃棒不停搅拌,最后将坩埚移入___________中进行冷却(请选用合适仪器填空:表面皿、研钵、烧杯、通风橱、试管夹、干燥器、泥三角)。
方法乙:取2药匙研碎的硫酸铜晶体于小烧杯中,加入20 mL浓硫酸(质量分数不低于98%),并用玻璃棒搅拌,静置5 min后倾去浓硫酸,用无水乙醇洗涤数次,倒在滤纸上晾干。
【交流与讨论】
(1)方法甲中,加热温度稍高时会出现变黑现象,原因是_________(用化学方程式表示)。
(2)方法乙中,浓硫酸的作用是__________;为了不浪费药品,对无水乙醇洗涤液进行再生的方法是______ ,所用的主要玻璃仪器有烧瓶、接液管、锥形瓶、酒精灯________________等。
(3)用制得的无水硫酸铜检验某双氧水中是否含水时,除了发现固体变蓝外,还发现该双氧水中有气泡产生,对此你有何猜想______________。
 (4)目前工业上正积极探索用浓HNO3作氧化剂,用Cu与浓H2SO4、浓HNO3反应,采取间歇加热、逐渐加入浓HNO3的方法来制备CuSO4•5H2O的新工艺。模拟制备装置如下图所示。
(4)目前工业上正积极探索用浓HNO3作氧化剂,用Cu与浓H2SO4、浓HNO3反应,采取间歇加热、逐渐加入浓HNO3的方法来制备CuSO4•5H2O的新工艺。模拟制备装置如下图所示。
【问题一】如图装置中,分液漏斗内装的液体是________,反应结束时,获取CuSO4•5H2O的操作过程是先________________,趁热将三颈瓶中的液体倒入烧杯中冷却,析出晶体CuSO4?5H2O ,过滤、晾干。
【问题二】工业上用石灰乳吸收尾气,除了防止环境污染外,还能得到了有经济实用价值的副产品―― 亚硝酸钙。尾气吸收生成亚硝酸钙的化学方程式是_______________。
查看习题详情和答案>>(12分)硫酸亚铁铵(NH4)2SO4•FeSO4•6H2O是一种重要化学试剂,实验室用除去锌镀层的铁片来制取硫酸亚铁铵,流程如下:
请回答下列问题:
(1)确定锌镀层被除去的标志是 ;
计算上述铁片锌镀层的厚度,不需要的数据是 (填编号)。
a.锌的密度ρ(g/cm3) b.镀锌铁片质量m 1(g) c.纯铁片质量m 2(g)
d.镀锌铁片面积S(cm2) e.镀锌铁片厚度h(cm)
(2)上述流程中:操作Ⅰ是取出铁片、 、 、称量。
(3)A物质可以为 (填编号)。
a.CuCl2 b.CuO c.Cu(NO3)2 d.CuSO4
(4)用无水乙醇洗涤潮湿的硫酸亚铁铵晶体是为了除去晶体表面残留的水分,不用加热烘干的原因是 。
(5)鉴定所得晶体中含有Fe2+、NH4+、SO42-离子的实验方法正确的是 (填编号)。
a.取少量样品于试管,加水溶解,通入适量Cl2,再加KSCN溶液,观察现象
b.取少量样品于试管,加水溶解,加入NaOH溶液,露置于空气中,观察现象
c.取少量样品于试管,加水溶解,加入浓NaOH溶液并加热,用湿润的红色石蕊试纸置于试管口,观察试纸颜色的变化
d.取少量样品于试管,加水溶解,加入盐酸后再加入BaCl2溶液,观察现象
查看习题详情和答案>>
(12分)硫酸亚铁铵(NH4)2SO4?FeSO4?6H2O是一种重要化学试剂,实验室用除去锌镀层的铁片来制取硫酸亚铁铵,流程如下:
请回答下列问题:
(1)确定锌镀层被除去的标志是 ;
计算上述铁片锌镀层的厚度,不需要的数据是 (填编号)。
a.锌的密度ρ(g/cm3) b.镀锌铁片质量m 1(g) c.纯铁片质量m 2(g)
d.镀锌铁片面积S(cm2) e.镀锌铁片厚度h(cm)
(2)上述流程中:操作Ⅰ是取出铁片、 、 、称量。
(3)A物质可以为 (填编号)。
a.CuCl2 b.CuO c.Cu(NO3)2 d.CuSO4
(4)用无水乙醇洗涤潮湿的硫酸亚铁铵晶体是为了除去晶体表面残留的水分,不用加热烘干的原因是 。
(5)鉴定所得晶体中含有Fe2+、NH4+、SO42-离子的实验方法正确的是 (填编号)。
a.取少量样品于试管,加水溶解,通入适量Cl2,再加KSCN溶液,观察现象
b.取少量样品于试管,加水溶解,加入NaOH溶液,露置于空气中,观察现象
c.取少量样品于试管,加水溶解,加入浓NaOH溶液并加热,用湿润的红色石蕊试纸置于试管口,观察试纸颜色的变化
d.取少量样品于试管,加水溶解,加入盐酸后再加入BaCl2溶液,观察现象
(12分)硫酸亚铁铵(NH4)2SO4•FeSO4•6H2O是一种重要化学试剂,实验室用除去锌镀层的铁片来制取硫酸亚铁铵,流程如下:
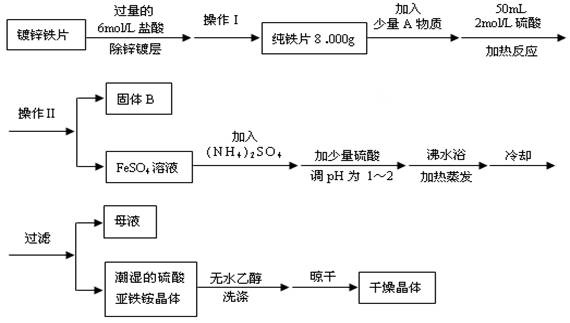
请回答下列问题:
(1)确定锌镀层被除去的标志是 ;
计算上述铁片锌镀层的厚度,不需要的数据是 (填编号)。
a.锌的密度ρ(g/cm3) b.镀锌铁片质量m 1(g) c.纯铁片质量m 2(g)
d.镀锌铁片面积S(cm2) e.镀锌铁片厚度h(cm)
(2)上述流程中:操作Ⅰ是取出铁片、 、 、称量。
(3)A物质可以为 (填编号)。
a.CuCl2 b.CuO c.Cu(NO3)2 d.CuSO4
(4)用无水乙醇洗涤潮湿的硫酸亚铁铵晶体是为了除去晶体表面残留的水分,不用加热烘干的原因是 。
(5)鉴定所得晶体中含有Fe2+、NH4+、SO42-离子的实验方法正确的是 (填编号)。
a.取少量样品于试管,加水溶解,通入适量Cl2,再加KSCN溶液,观察现象
b.取少量样品于试管,加水溶解,加入NaOH溶液,露置于空气中,观察现象
c.取少量样品于试管,加水溶解,加入浓NaOH溶液并加热,用湿润的红色石蕊试纸置于试管口,观察试纸颜色的变化
d.取少量样品于试管,加水溶解,加入盐酸后再加入BaCl2溶液,观察现象
查看习题详情和答案>>