网址:http://m.1010jiajiao.com/timu_id_41463[举报]
一、选择题:(共44分)
1.D 2.A 3.D 4.B 5.A 6.D 7.C 8.C 9.A 10.C 11.B
12.D 13.B 14.A 15.C 16.C 17.A 18.B 19.A 20.C 21.B 22.B
二. 填空题(本题共4小题,共48分)
23.(8分,每空2分) K2Cr2O7 是氧化剂, HCl 是还原剂,
Cl 元素被氧化, Cr 元素被还原,
Cl2 是氧化产物, CrCl3 是还原产物。
 |
K2Cr2O7 +14HCl=2KCl+2CrCl3+3Cl2↑+7H2O(标出电子转移方向和数目)
24.(14分,每空2分)
(1)化学式:A Ba(OH)2 B H2SO
(2)反应①、②、⑤的离子方程式
① SO42-+ 2H++ ba2++2oh-= baSo4↓+2H2O
② CO32-+ 2H+ = CO2 ↑+ H2O
⑤ Mg2+ + 2oh- = Mg(OH)2↓
25.(14分,每空2分)三种离子: OH- 、 K+ 、 Cl- 。
铁粉 , 银 ,
Ag+ 、 Fe3+ , NO3- 、 K+ 。
26.(12分,每空2分) (1)
(2)500mL容量瓶、烧杯、玻璃棒、胶头滴管。
(3)A、_无影响____ B、____偏高_
C、__偏低____ D、 _偏低_ 。
三. 计算题(本题共1小题,共8分)
27.(1)氧化剂是 MnO2 (2分 )
(2) ①168mL(3分 )
②1mol (3分 )
(1)某小组同学欲用4mol/L的盐酸配制230mL 0.4mol/L 盐酸溶液,需取用4mol/L盐酸
(2)下列实验操作使配制的溶液浓度偏低的是
A.容量瓶洗涤后未干燥
B.移液时,有少量溶液溅出
C.定容时,加水不慎超过刻度线,又倒出一些
D.定容时,俯视刻度线
E.装入试剂瓶时,有少量溶液溅出
(Ⅱ)瑞典化学家舍勒将软锰矿(主要成分为MnO2)与浓盐酸混合加热,在世界上首先得到了氯气.已知Cl2和碱溶液在不同条件下,得到的产物不同,某兴趣小组用下图所示装置制取氯酸钾、次氯酸钠和探究氯水的性质.( 3Cl2+6KOH
| ||
请填写下列空白:
(1)制取氯气时,在圆底烧瓶里加入一定质量的二氧化锰,通过
| ||
| ||
(2)反应完毕经冷却后,B的试管中有大量晶体析出.图中符合该晶体溶解度曲线的是
(3)实验中可观察到D的试管里溶液的颜色发生了如下变化,请填写下表中的空白:
| 实验现象 | 原因 |
| 溶液最初从紫色逐渐变为 红 红 色 |
氯气与水反应生成的H+使石蕊变色 |
| 随后溶液逐渐变为无色 | 氯气与水反应生成的HClO将石蕊氧化为无色物质 氯气与水反应生成的HClO将石蕊氧化为无色物质 |
实验室中盐酸的用途十分广泛,常常用来制备气体。
(1)某小组同学欲用4 mol/L的盐酸配制230 mL 0.4mol/L 盐酸溶液,需取用4 mol/L盐酸 mL,实验中需要用到的玻璃仪器有 、 、量筒、 烧杯、胶头滴管。
(2)下列实验操作使配制的溶液浓度偏低的是
A.容量瓶洗涤后未干燥
B.移液时,有少量溶液溅出
C.定容时,加水不慎超过刻度线,又倒出一些
D.定容时,俯视刻度线
E.装入试剂瓶时,有少量溶液溅出
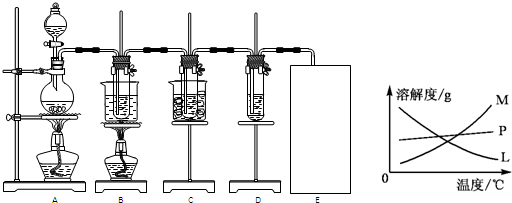
(Ⅱ)(16分)瑞典化学家舍勒将软锰矿(主要成分为MnO2)与浓盐酸混合加热,在世界上首先得到了氯气。已知Cl2和碱溶液在不同条件下,得到的产物不同,某兴趣小组用下图所示装置制取氯酸钾、次氯酸钠和探究氯水的性质。( 3Cl2+6KOH ![]() KClO3+5KCl+3H2O )
KClO3+5KCl+3H2O )
 |
图中:A为氯气发生装置;B的试管里盛有15 mL 30% KOH溶液,并置于水浴中;C的试管里盛有15 mL 8% NaOH溶液,并置于冰水浴中;D的试管里加有紫色石蕊试液。
请填写下列空白:
(1)制取氯气时,在圆底烧瓶里加入一定质量的二氧化锰,通过 (填仪器名称)向圆底烧瓶中加入适量的浓盐酸。装置A中反应的离子方程式 。
(2) 反应完毕经冷却后,B的试管中有大量晶体析出。右图中符合该晶体溶解度曲线的是 (填编号字母);从B的试管中分离出该晶体的方法是 (填实验操作名称)。该小组同学发现制得的氯酸钾产量偏低,可能的一种原因是Cl2中含有杂质,该杂质成分 (除水蒸气外,填化学式),如何改进 ;
反应完毕经冷却后,B的试管中有大量晶体析出。右图中符合该晶体溶解度曲线的是 (填编号字母);从B的试管中分离出该晶体的方法是 (填实验操作名称)。该小组同学发现制得的氯酸钾产量偏低,可能的一种原因是Cl2中含有杂质,该杂质成分 (除水蒸气外,填化学式),如何改进 ;
(3)实验中可观察到D的试管里溶液的颜色发生了如下变化,请填写下表中的空白:
| 实验现象 | 原因 |
| 溶液最初从紫色逐渐变为 色 | 氯气与水反应生成的H+使石蕊变色 |
| 随后溶液逐渐变为无色 |
|
(4)请在装置图方框中画出缺少的实验装置,并注明试剂。
查看习题详情和答案>>
右图为农夫山泉矿泉水瓶上的部分说明文字,列出了该饮用天然水理化指标。这里的钙、镁、钾、钠是指
|
饮用天然水理化指标 矿物元素 测定结果 钙≥4.0 mg/L 镁≥0.5 mg/L 钾≥0.35 mg/L 钠≥0.8 mg/L 偏硅酸≥1.8 mg/L pH (25℃) 7.1
【答案】D 【解析】略 【题型】选择题 【适用】较易 【标题】2010年湖南浏阳一中高一上学期期中考试化学试卷 【关键字标签】农夫山泉,指标 【结束】 3【题文】下列实验操作中,错误的是
【答案】D 【解析】略 【题型】选择题 【适用】较易 【标题】2010年湖南浏阳一中高一上学期期中考试化学试卷 【关键字标签】实验操作 【结束】 4【题文】下列说法中正确的是
【答案】B 【解析】略 【题型】选择题 【适用】较易 【标题】2010年湖南浏阳一中高一上学期期中考试化学试卷 【关键字标签】分子数,原子数 【结束】 5【题文】下列有关0.2mol·L-1 BaCl2溶液的说法不正确的是
【答案】A 【解析】略 【题型】选择题 【适用】较易 【标题】2010年湖南浏阳一中高一上学期期中考试化学试卷 【关键字标签】溶液,离子浓度 【结束】 6【题文】下列离子方程式中书写正确的是( )
【答案】B 【解析】略 【题型】选择题 【适用】较易 【标题】2010年湖南浏阳一中高一上学期期中考试化学试卷 【关键字标签】离子方程式,氢氧化钡 【结束】 7【题文】已知有如下反应:①2Fe3++2I-===2Fe2++I2 ②2Fe2++Br2===2Fe3++2Br- ③2Fe(CN)+I2===2Fe(CN)+2I-,试判断氧化性强弱顺序正确的是
【答案】C 【解析】略 【题型】选择题 【适用】较易 【标题】2010年湖南浏阳一中高一上学期期中考试化学试卷 【关键字标签】氧化性,顺序 【结束】 8【题文】实验室制取少量N2常利用的反应是NaNO2+NH4ClNaCl+N2↑+2H2O,关于该反应的说法正确的是
【答案】A 【解析】略 【题型】选择题 【适用】较易 【标题】2010年湖南浏阳一中高一上学期期中考试化学试卷 【关键字标签】实验室,氧化剂 【结束】 9【题文】用托盘天平称量固体物质时,若将样品和砝码放在托盘上的位置颠倒,平衡时托盘上的砝码质量为10g,游码为0.5g,则样品的质量为
【答案】D 【解析】略 【题型】选择题 【适用】较易 【标题】2010年湖南浏阳一中高一上学期期中考试化学试卷 【关键字标签】托盘天平,砝码 【结束】 10【题文】将26克含有SiO2和CaCO3固体在高温下加热至质量不再改变,冷却后称重为17.2克。(已知:SiO2 + CaCO3 CaSiO3 + CO2↑,SiO2和CaSiO3均为固体) (1)求生成的CO2的体积(标准状况下) (2)求原混合物中所含SiO2的质量。 【答案】(1)4.48L (2)6克 【解析】略 【题型】计算题 【适用】较易 【标题】2010年湖南浏阳一中高一上学期期中考试化学试卷 【关键字标签】高温,体积 【结束】 |
查看习题详情和答案>>
右图为农夫山泉矿泉水瓶上的部分说明文字,列出了该饮用天然水理化指标。这里的钙、镁、钾、钠是指
|
饮用天然水理化指标 矿物元素 测定结果 钙≥4.0 mg/L 镁≥0.5 mg/L 钾≥0.35 mg/L 钠≥0.8 mg/L 偏硅酸≥1.8 mg/L pH (25℃) 7.1
【答案】D 【解析】略 【题型】选择题 【适用】较易 【标题】2010年湖南浏阳一中高一上学期期中考试化学试卷 【关键字标签】农夫山泉,指标 【结束】 3【题文】下列实验操作中,错误的是
【答案】D 【解析】略 【题型】选择题 【适用】较易 【标题】2010年湖南浏阳一中高一上学期期中考试化学试卷 【关键字标签】实验操作 【结束】 4【题文】下列说法中正确的是
【答案】B 【解析】略 【题型】选择题 【适用】较易 【标题】2010年湖南浏阳一中高一上学期期中考试化学试卷 【关键字标签】分子数,原子数 【结束】 5【题文】下列有关0.2mol·L-1 BaCl2溶液的说法不正确的是
【答案】A 【解析】略 【题型】选择题 【适用】较易 【标题】2010年湖南浏阳一中高一上学期期中考试化学试卷 【关键字标签】溶液,离子浓度 【结束】 6【题文】下列离子方程式中书写正确的是( )
【答案】B 【解析】略 【题型】选择题 【适用】较易 【标题】2010年湖南浏阳一中高一上学期期中考试化学试卷 【关键字标签】离子方程式,氢氧化钡 【结束】 7【题文】已知有如下反应:①2Fe3++2I-===2Fe2++I2 ②2Fe2++Br2===2Fe3++2Br- ③2Fe(CN)+I2===2Fe(CN)+2I-,试判断氧化性强弱顺序正确的是
【答案】C 【解析】略 【题型】选择题 【适用】较易 【标题】2010年湖南浏阳一中高一上学期期中考试化学试卷 【关键字标签】氧化性,顺序 【结束】 8【题文】实验室制取少量N2常利用的反应是NaNO2+NH4ClNaCl+N2↑+2H2O,关于该反应的说法正确的是
【答案】A 【解析】略 【题型】选择题 【适用】较易 【标题】2010年湖南浏阳一中高一上学期期中考试化学试卷 【关键字标签】实验室,氧化剂 【结束】 9【题文】用托盘天平称量固体物质时,若将样品和砝码放在托盘上的位置颠倒,平衡时托盘上的砝码质量为10g,游码为0.5g,则样品的质量为
【答案】D 【解析】略 【题型】选择题 【适用】较易 【标题】2010年湖南浏阳一中高一上学期期中考试化学试卷 【关键字标签】托盘天平,砝码 【结束】 10【题文】将26克含有SiO2和CaCO3固体在高温下加热至质量不再改变,冷却后称重为17.2克。(已知:SiO2 + CaCO3 CaSiO3 + CO2↑,SiO2和CaSiO3均为固体) (1)求生成的CO2的体积(标准状况下) (2)求原混合物中所含SiO2的质量。 【答案】(1)4.48L (2)6克 【解析】略 【题型】计算题 【适用】较易 【标题】2010年湖南浏阳一中高一上学期期中考试化学试卷 【关键字标签】高温,体积 【结束】 |
查看习题详情和答案>>
右图为农夫山泉矿泉水瓶上的部分说明文字,列出了该饮用天然水理化指标。这里的钙、镁、钾、钠是指
| 饮用天然水理化指标 矿物元素 测定结果 钙≥4.0 mg/L 镁≥0.5 mg/L 钾≥0.35 mg/L 钠≥0.8 mg/L 偏硅酸≥1.8 mg/L pH (25℃) 7.1
【答案】D 【解析】略 【题型】选择题 【适用】较易 【标题】2010年湖南浏阳一中高一上学期期中考试化学试卷 【关键字标签】农夫山泉,指标 【结束】 3【题文】下列实验操作中,错误的是
【答案】D 【解析】略 【题型】选择题 【适用】较易 【标题】2010年湖南浏阳一中高一上学期期中考试化学试卷 【关键字标签】实验操作 【结束】 4【题文】下列说法中正确的是
【答案】B 【解析】略 【题型】选择题 【适用】较易 【标题】2010年湖南浏阳一中高一上学期期中考试化学试卷 【关键字标签】分子数,原子数 【结束】 5【题文】下列有关0.2mol·L-1 BaCl2溶液的说法不正确的是
【答案】A 【解析】略 【题型】选择题 【适用】较易 【标题】2010年湖南浏阳一中高一上学期期中考试化学试卷 【关键字标签】溶液,离子浓度 【结束】 6【题文】下列离子方程式中书写正确的是( )
【答案】B 【解析】略 【题型】选择题 【适用】较易 【标题】2010年湖南浏阳一中高一上学期期中考试化学试卷 【关键字标签】离子方程式,氢氧化钡 【结束】 7【题文】已知有如下反应:①2Fe3++2I-===2Fe2++I2 ②2Fe2++Br2===2Fe3++2Br- ③2Fe(CN)+I2===2Fe(CN)+2I-,试判断氧化性强弱顺序正确的是
【答案】C 【解析】略 【题型】选择题 【适用】较易 【标题】2010年湖南浏阳一中高一上学期期中考试化学试卷 【关键字标签】氧化性,顺序 【结束】 8【题文】实验室制取少量N2常利用的反应是NaNO2+NH4ClNaCl+N2↑+2H2O,关于该反应的说法正确的是
【答案】A 【解析】略 【题型】选择题 【适用】较易 【标题】2010年湖南浏阳一中高一上学期期中考试化学试卷 【关键字标签】实验室,氧化剂 【结束】 9【题文】用托盘天平称量固体物质时,若将样品和砝码放在托盘上的位置颠倒,平衡时托盘上的砝码质量为10g,游码为0.5g,则样品的质量为
【答案】D 【解析】略 【题型】选择题 【适用】较易 【标题】2010年湖南浏阳一中高一上学期期中考试化学试卷 【关键字标签】托盘天平,砝码 【结束】 10【题文】将26克含有SiO2和CaCO3固体在高温下加热至质量不再改变,冷却后称重为17.2克。(已知:SiO2 + CaCO3 CaSiO3 + CO2↑,SiO2和CaSiO3均为固体) (1)求生成的CO2的体积(标准状况下) (2)求原混合物中所含SiO2的质量。 【答案】(1)4.48L (2)6克 【解析】略 【题型】计算题 【适用】较易 【标题】2010年湖南浏阳一中高一上学期期中考试化学试卷 【关键字标签】高温,体积 【结束】 |
查看习题详情和答案>>